
科目: 来源:2012-2013学年山东省枣庄市高三4月模拟考试化学试卷(解析版) 题型:选择题
下列说法正确的是
A.镁、铝、铜、铁、钠五种元素中,铜和铁均为副族元素
B.10Be和9Be是中子数不同质子数相同的同种核素
C.元素X位于元素Y的上一周期,X原子得电子能力强于Y原子
D.短周期的同主族元素原子序数差值可能为2、8、10
查看答案和解析>>
科目: 来源:2012-2013学年山东省枣庄市高三4月模拟考试化学试卷(解析版) 题型:选择题
下列关于有机物的说法不正确的是
A.乙烯和苯可以用石油和煤为原料制得,它们均能使溴水褪色,但褪色的原理不同
B.糖类、油脂、蛋白质都能发生水解反应,且均属于高分子化合物
C.用饱和Na2CO3溶液能除去乙酸乙酯中混有的乙酸和乙醇杂质
D.研究表明禽流感病毒H7N9在沸水中两分钟就能被杀死,是因为病毒所含蛋白质受热变性
查看答案和解析>>
科目: 来源:2012-2013学年山东省枣庄市高三4月模拟考试化学试卷(解析版) 题型:选择题
下列有关实验的叙述正确的是
A.滴定管洗净后,直接注入标准液进行滴定
B.某溶液先加入稀盐酸无明显现象,再加入BaCl2溶液产生白色沉淀,说明原溶液中含有SO42-
C.配制一定物质的量浓度的稀硫酸时,向容量瓶中加入适量的水,再缓缓注入事先量取的浓硫酸
D.某气体能使湿润的蓝色石蕊试纸变为红色,则该气体为氨气
查看答案和解析>>
科目: 来源:2012-2013学年山东省枣庄市高三4月模拟考试化学试卷(解析版) 题型:选择题
下列说法正确的是
A.高纯度的二氧化硅能用于制光导纤维,光导纤维遇强碱会“断路”
B.向氨水中滴加Al2(SO4)3溶液和向Al2(SO4)3溶液中滴加氨水,现象不同
C.常温下,使湿润的KI淀粉试纸变蓝色的气体为氯气
D.标准状况下,11.2LNO2和11.2LN2O4的混合物中所含的分子数为9.03×1023个
查看答案和解析>>
科目: 来源:2012-2013学年山东省枣庄市高三4月模拟考试化学试卷(解析版) 题型:选择题
下列关于电化学知识说法正确的是
A.电解AlCl3、FeCl3、CuCl2的混合溶液,在阴极上依次析出Al、Fe、Cu
B.电解CuSO4溶液一段时间后,加入适量Cu(OH)2可以使溶液恢复至原状态
C.铅蓄电池在充电时,连接电源正极发生的电极反应为:PbSO4+2e-=Pb+SO42-
D.将钢闸门与直流电流的负极相连,可防止钢闸门腐蚀
查看答案和解析>>
科目: 来源:2012-2013学年山东省枣庄市高三4月模拟考试化学试卷(解析版) 题型:选择题
一定温度下的密闭容器中发生反应:X(g)+3Y(g) 2Z(g)
△H<
2Z(g)
△H< ,如图是反应达平衡及改变条件平衡移动的图像。下列说法错误的是
,如图是反应达平衡及改变条件平衡移动的图像。下列说法错误的是

A.c点和d点X的正逆反应速率相等
B.起始时,加入Y的物质的量为1.3mol
C.平衡状态由A变到B时,平衡常数:K(A)<K(B)
D.平衡状态由A变到B时,放出的热量:Q(A)<Q(B)
查看答案和解析>>
科目: 来源:2012-2013学年山东省枣庄市高三4月模拟考试化学试卷(解析版) 题型:简答题
运用化学反应原理研究碳、氮、硫、氯等单质及其化合物的反应,对生产、生活、环境保护等领域有着重要的意义。
(1)下列措施中,不利于环境保护的有 (填编号)。
a.大量开采使用化石燃料
b.使用无氟冰箱、空调
c.多步行多乘公交车,少用专车和私家车
d.将工业“废气”、“废液”、“废渣”直接排放
(2)工业上的“脱碳”指的是从“脱硝”、“脱硫”后的烟气用碱液吸收并得到浓缩的二氧化碳。利用二氧化碳合成甲醇是碳减排的新方向。
①写出吸收二氧化碳的离子方程式 。
②常温下,0.1mol/LNaHCO3溶液的pH>8,则溶液中c(H2CO3) _______c(CO32-) (填“>”、“<”或“=”)。
③合成的甲醇可以做为新型燃料电池的原料,若电解液是碱性的,则其负极的电极反应式为 。
(3)二氧化氯(ClO2),为一种黄绿色气体,是公认的高效、广谱安全的杀菌消毒剂。工业上制备ClO2的反应原理为:4HC1(浓)+2NaClO3=2ClO2↑+Cl2↑+2H2O+2NaCl。上述反应中,产生1 mol ClO2,则被氧化的HC1为 。
(4)SO2溶于水可以得到二元弱酸H2SO3(亚硫酸)。
①25℃时,将NaOH深液与亚硫酸混合至恰好中和,则混合液中各种离子浓度的大小关系为 。
②25℃时,当NaOH溶液与H2SO3等物质的量混合时,发现混合液pH<7,请你简要解释其原因 。
查看答案和解析>>
科目: 来源:2012-2013学年山东省枣庄市高三4月模拟考试化学试卷(解析版) 题型:填空题
某实验小组用工业废弃固体(主要成分为Cu2S和Fe2O3)制备有关物质,整个流程如下图所示。请回答:
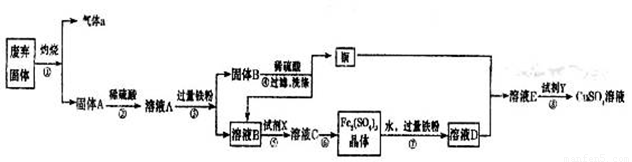
(1)气体a的化学式为 。
(2)溶液B加入硫酸酸化后再加入适宜氧化剂X得到溶液C,写出该反应的离子方程式 。
(3)制备硫酸铜溶液。常温下,O2、铜粉和稀硫酸三者在一起,几乎不反应,当加入溶液D后,随即生成硫酸铜。经理阅资料发现FeSO4对铜的氧化起催化作用。
A.第一步反应的离子方程式为:4Fe2++O2+4H+=4Fe3++2H2O,则第二步反应的郭子方程式为 。
B.⑦操作中,配制Fe2(SO4)3溶液时应注意 。
(4)操作⑧的目的是得到较纯的硫酸铜溶液。加入适宜试剂Y调节pH至铁元素全部沉淀(离子浓度小于10-5mol/L),然后再过滤,浓缩、结晶等,则pH至少调节为_____。
已知:Ksp[Cu(OH)2]≈1×10-22,Ksp[Fe(OH)2] ≈1×10-16,Ksp[Fe(OH)3] ≈1×10-38
(5)科学家发现纳米级的Cu2O在太阳光照射下可以催化分解水。
A.一定温度下,在2L密闭容器中加入纳米级Cu2O,通入2mol水蒸气,发生如下反应:
2H2O(g)=2H2(g)+O2(g) △H=+484kJ/mol
20min末测得n(O2)=0.16mol,则这段时间的反应速率υ(H2)=_________;该温度下,此反应的平衡常数表达式K=___________________。
B.已知:2Cu2O(s)+O2(g)=4CuO(s) △H=-292kJ/mol
2C(s)+O2(g)=2CO(g) △H=-221kJ/mol
请写出炭粉还原CuO(s)制备Cu2O(s)的热化学方程式_________________。
查看答案和解析>>
科目: 来源:2012-2013学年山东省枣庄市高三4月模拟考试化学试卷(解析版) 题型:实验题
实验室以工业碳酸钙(含少量Na+、Al3+、Fe3+等杂质)为原料制取CaCl2·H2O和CaO2的主要流程如下:
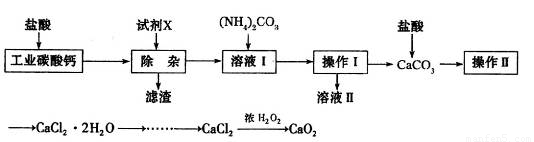
(1)加入试剂X,调节溶液pH为碱性环境,以除去溶液中Al3+和Fe3+,滤渣的主要成分是___________。试剂X可以选择下列的________(填编号)。
A.CaO B.CaCO3 C.NH3·H2O D.Ba(OH)2
(2)操作II中进行蒸发浓缩时,除三角架、酒精灯外,还需要的仪器有__________。
(3)由CaCl2制取CaO2的反应中,温度不宜太高的原因是_______________。
(4)用下列装置测定工业碳酸钙的质量分数
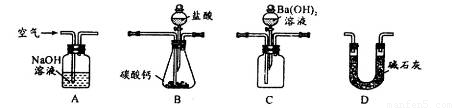
①检验装置B气密性良好的实验过程是__________________________。
②按A—B—C—D顺序连接,然后从A装置通入空气,目的是_______________。
③装置D的作用为______________________。
④实验时,准确称取10.00g工业碳酸钙3份,进行3次测定,测得BaCO3沉淀的平均质量为17.73g,则样品中CaCO3的质量分数为__________________。
查看答案和解析>>
科目: 来源:2012-2013学年山东省枣庄市高三4月模拟考试化学试卷(解析版) 题型:填空题
化工生产中涉及较多的化学原理、生产方法和工艺流程,请回答下列问题:
(1)工业上用硫铁矿生产硫酸的主要设备有__________、__________、__________。
(2)工业上制备硫酸,常采用__________(填编号)为吸收剂,以高效吸收三氧化硫。
a.自来水 b.蒸馏水 c.稀硫酸 d.98.3%硫酸
(3)侯氏制碱法中,用二氧化碳和氨气与饱和食盐水反应制碳酸氢钠,应先向饱和食盐水中通入_____。
(4)石油裂化分为热裂化、催化裂化和_______,其目的为__________________。
(5)为降低电解液熔点,工业上生产铝时需要加入的熔剂为____________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com