
科目: 来源:2009-2010学年河南省南阳市南召二中高三(上)期末化学模拟试卷(解析版) 题型:选择题
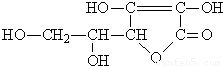 ,有关它的叙述正确的是( )
,有关它的叙述正确的是( )查看答案和解析>>
科目: 来源:2009-2010学年河南省南阳市南召二中高三(上)期末化学模拟试卷(解析版) 题型:选择题
查看答案和解析>>
科目: 来源:2009-2010学年河南省南阳市南召二中高三(上)期末化学模拟试卷(解析版) 题型:选择题
查看答案和解析>>
科目: 来源:2009-2010学年河南省南阳市南召二中高三(上)期末化学模拟试卷(解析版) 题型:选择题
查看答案和解析>>
科目: 来源:2009-2010学年河南省南阳市南召二中高三(上)期末化学模拟试卷(解析版) 题型:选择题
 W(g)+Z(g)(正反应是放热反应),在一体积不变的容器中反应达到平衡后,改变条件,反应速率(v)随时间变化的情况如下图所示:下列条件的改变与图中情况相符的是( )
W(g)+Z(g)(正反应是放热反应),在一体积不变的容器中反应达到平衡后,改变条件,反应速率(v)随时间变化的情况如下图所示:下列条件的改变与图中情况相符的是( )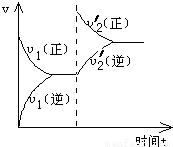
查看答案和解析>>
科目: 来源:2009-2010学年河南省南阳市南召二中高三(上)期末化学模拟试卷(解析版) 题型:解答题
查看答案和解析>>
科目: 来源:2009-2010学年河南省南阳市南召二中高三(上)期末化学模拟试卷(解析版) 题型:解答题

查看答案和解析>>
科目: 来源:2009-2010学年河南省南阳市南召二中高三(上)期末化学模拟试卷(解析版) 题型:解答题
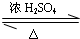 Z+H2O;写出该反应的化学方程式______,反应类型为______.
Z+H2O;写出该反应的化学方程式______,反应类型为______.查看答案和解析>>
科目: 来源:2009-2010学年河南省南阳市南召二中高三(上)期末化学模拟试卷(解析版) 题型:解答题
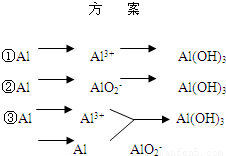
| 方 案 | 生成1mol Al(OH)3消耗H+ 或 OH- 的物质的量/mol | |
| 消耗H+ | 消耗OH- | |
| ① | 3 | ______ |
| ② | ______ | 1 |
| ③ | 3/4 | ______ |
查看答案和解析>>
科目: 来源:2009-2010学年河南省南阳市南召二中高三(上)期末化学模拟试卷(解析版) 题型:解答题
 2Fe2O3+8SO2;该反应中氧化剂和氧化产物的物质的量之比为______;标准状态下得到4.48升SO2时,一共转移了______mole-.
2Fe2O3+8SO2;该反应中氧化剂和氧化产物的物质的量之比为______;标准状态下得到4.48升SO2时,一共转移了______mole-.压强/MPa 转化率/% 温度/℃ | 0.1 | 0.5 | 1 | 10 |
| 400 | 99.2 | 99.6 | 99.7 | 99.9 |
| 500 | 93.5 | 96.9 | 97.8 | 99.3 |
| 600 | 73.7 | 85.8 | 89.5 | 96.4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com