相关习题
0 62975 62983 62989 62993 62999 63001 63005 63011 63013 63019 63025 63029 63031 63035 63041 63043 63049 63053 63055 63059 63061 63065 63067 63069 63070 63071 63073 63074 63075 63077 63079 63083 63085 63089 63091 63095 63101 63103 63109 63113 63115 63119 63125 63131 63133 63139 63143 63145 63151 63155 63161 63169 203614
科目:
来源:2012-2013学年安徽省宣城市、芜湖市七校联考高二(上)期中化学试卷(解析版)
题型:选择题
已知反应CO(g)=C(s)+1/2O2(g)的△H>0.设△H和△S都不随温度而变,下列说法中正确的是( )
A.任何温度下都是非自发变化
B.高温下是自发变化
C.任何温度下都是自发变化
D.低温下是自发变化
查看答案和解析>>
科目:
来源:2012-2013学年安徽省宣城市、芜湖市七校联考高二(上)期中化学试卷(解析版)
题型:选择题
下列各电离方程式中书写正确的是?( )
A.
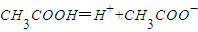
B.
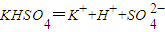
C.H
2CO
3?2H
++CO
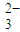
D.
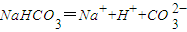
查看答案和解析>>
科目:
来源:2012-2013学年安徽省宣城市、芜湖市七校联考高二(上)期中化学试卷(解析版)
题型:选择题
在NH
3.H
2O?NH
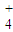
+OH
-形成的平衡中,要使NH
3?H
2O的电离程度及c(OH
-)都增大,可采取的措施是( )?
A.通入HCl?
B.加少量NaOH固体?
C.加少量氯化铵固体?
D.加热
查看答案和解析>>
科目:
来源:2012-2013学年安徽省宣城市、芜湖市七校联考高二(上)期中化学试卷(解析版)
题型:选择题
如图所示是298K时,N
2与H
2反应过程中能量变化的曲线图,下列叙述正确的是( )
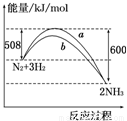
A.该反应的热化学方程式为:N
2+3H
2?2NH
3 △H=-92 kJ/mol
B.b曲线是加入催化剂时的能量变化曲线
C.升高温度,正反应速率减小,逆反应速率增大,平衡逆向移动
D.在温度、体积一定的条件下,通入1 mol N
2和3 mol H
2充分反应后放出的热量为92 kJ
查看答案和解析>>
科目:
来源:2012-2013学年安徽省宣城市、芜湖市七校联考高二(上)期中化学试卷(解析版)
题型:选择题
将5.0mol PCl3和2.5mol Cl2充入体积不变的密闭容器中,在一定条件下发生下述反应:PCl3(g)+Cl2(g)?PCl5(g),达到平衡时,PCl5为1mol,如果此时移走2.0mol PCl3和1.0mol Cl2,在相同温度下再达平衡时PCl5的物质的量是( )
A.<0.6 mol
B.0.6 mol
C.>0.6 mol
D.无法确定
查看答案和解析>>
科目:
来源:2012-2013学年安徽省宣城市、芜湖市七校联考高二(上)期中化学试卷(解析版)
题型:选择题
一定温度下,下列叙述不能作为可逆反应A(g)+3B(g)?2C(g)达到平衡标志的是( )
①恒压容器中,混合气体的密度保持不变;
②单位时间内生成a mol A,同时消耗2a mol C
③A、B、C的浓度不再变化;
④C的物质的量不再变化
⑤恒容容器中,混合气体的总压强不再变化;
⑥混合气体的总物质的量不再变化
⑦单位时间消耗a mol A,同时生成3a mol B;
⑧A、B、C的分子数之比为1:3:2.
A.②⑧
B.①②⑧
C.①②③
D.①⑤⑥
查看答案和解析>>
科目:
来源:2012-2013学年安徽省宣城市、芜湖市七校联考高二(上)期中化学试卷(解析版)
题型:选择题
已知:2CO(g)+O
2(g)=2CO
2(g);△H=-566kJ/mol,Na
2O
2(s)+CO
2(g)=Na
2CO
3(s)+1/2O
2(g);△H=-226kJ/mol根据以上热化学方程式判断,下列说法正确的是( )
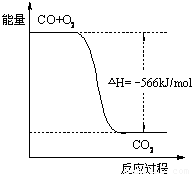
A.CO的燃烧热为283 kJ
B.如图可表示由CO生成CO
2的反应过程和能量关系
C.2Na
2O
2(s)+2CO
2(s)=2Na
2CO
3(s)+O
2(g);△H>-452 kJ/mol
D.CO(g)与Na
2O
2(s)反应放出509 kJ热量时,电子转移数为6.02×10
23
查看答案和解析>>
科目:
来源:2012-2013学年安徽省宣城市、芜湖市七校联考高二(上)期中化学试卷(解析版)
题型:选择题
现有下列四个图象,下列反应中全部符合上述图象的反应是( )

A.N
2(g)+3H
2(g)?2NH
3(g);△H<0
B.2SO
3(g)?2SO
2(g)+O
2(g);△H>0
C.4NH
3(g)+5O
2(g)?4NO+6H
2O(g);△H<0
D.H
2(g)+CO(g)?C(s)+H
2O(g);△H>0
查看答案和解析>>
科目:
来源:2012-2013学年安徽省宣城市、芜湖市七校联考高二(上)期中化学试卷(解析版)
题型:选择题
在相同温度和压强下,对反应CO
2(g)+H
2(g)?CO(g)+H
2O(g)进行甲、乙、丙、丁四组实验,实验起始时放入容器内各组分的物质的量见表:
| CO2 | H2 | CO | H2O |
| 甲 | a mol | a mol | 0 mol | 0 mol |
| 乙 | 2a mol | a mol | 0 mol | 0 mol |
| 丙 | 0 mol | 0 mol | a mol | a mol |
| 丁 | a mol | 0 mol | a mol | a mol |
上述四种情况达到平衡后,n(CO)的大小顺序是( )
A.丁>乙>丙=甲
B.乙>丁>甲>丙
C.乙=丁>丙=甲
D.丁>丙>乙>甲
查看答案和解析>>
科目:
来源:2012-2013学年安徽省宣城市、芜湖市七校联考高二(上)期中化学试卷(解析版)
题型:选择题
高氯酸、硫酸、硝酸和盐酸都是强酸,其酸性在水溶液中差别不大.以下是某温度下这四种酸在冰醋酸中的电离常数:
| 酸 | HClO4 | H2SO4 | HCl | HNO3 |
| Ka | 1.6×10-5 | 6.3×10-9 | 1.6×10-9 | 4.2×10-10 |
从以上表格中判断以下说明不正确的是( )
A.在冰醋酸中1mol/L的高氯酸的电离度约为0.4%
B.在冰醋酸中硝酸是这四种酸中最弱的酸
C.在冰醋酸中硫酸的电离方程式为:H
2SO
4═2H
++SO
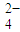
D.水对于这四种酸的强弱没有区分能力,但醋酸可以区分这四种酸的强弱
查看答案和解析>>

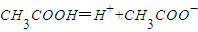
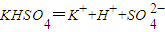
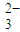
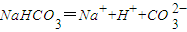
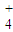 +OH-形成的平衡中,要使NH3?H2O的电离程度及c(OH-)都增大,可采取的措施是( )?
+OH-形成的平衡中,要使NH3?H2O的电离程度及c(OH-)都增大,可采取的措施是( )?