
科目: 来源:2010-2011学年广东省东莞市教研室高二(上)期末化学试卷(A)(解析版) 题型:解答题
 O2(g)═CO2(g)△H=-283kJ/mol
O2(g)═CO2(g)△H=-283kJ/mol查看答案和解析>>
科目: 来源:2010-2011学年广东省东莞市教研室高二(上)期末化学试卷(A)(解析版) 题型:解答题
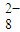 =I
=I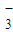 +2SO
+2SO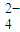 的反应速率可以用I
的反应速率可以用I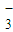 与加入的淀粉溶液显蓝色的时间t来度量,t越小,反应速率越大.某探究性学习小组在20℃时进行实验,得到的数据如下表:
与加入的淀粉溶液显蓝色的时间t来度量,t越小,反应速率越大.某探究性学习小组在20℃时进行实验,得到的数据如下表:| 实验编号 | ① | ② | ③ | ④ | ⑤ |
| c(I-)/mol?L | 0.040 | 0.080 | 0.080 | 0.160 | 0.160 |
| c(S2O82-)/mol?L | 0.040 | 0.040 | 0.080 | 0.020 | 0.040 |
| t/s | 88.0 | 44.0 | 22.0 | 44.0 | t2 |
查看答案和解析>>
科目: 来源:2010-2011学年广东省东莞市教研室高二(上)期末化学试卷(A)(解析版) 题型:解答题
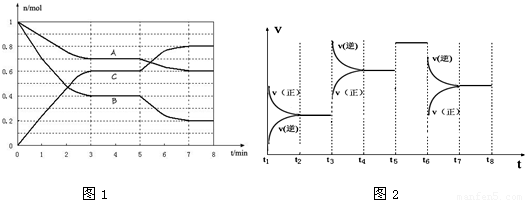
查看答案和解析>>
科目: 来源:2010-2011学年广东省东莞市教研室高二(上)期末化学试卷(A)(解析版) 题型:填空题
查看答案和解析>>
科目: 来源:2010-2011学年广东省东莞市教研室高二(上)期末化学试卷(A)(解析版) 题型:解答题
| 滴定次数 | 待测液体积(mL) | 标准硫酸体积(mL) | |
| 滴定前读数(mL) | 滴定后读数(mL) | ||
| 第一次 | 20.00 | 0.50 | 25.45 |
| 第二次 | 20.00 | 4.00 | 29.05 |
| 第三次 | 20.00 | 3.00 | 30.00 |
| 第四次 | 20.00 | 2.00 | 27.00 |

查看答案和解析>>
科目: 来源:2010-2011学年广东省东莞市教研室高二(上)期末化学试卷(A)(解析版) 题型:解答题
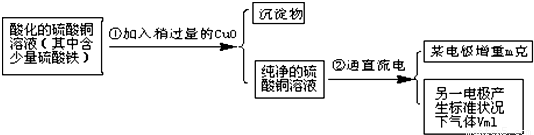
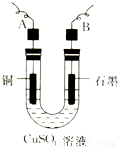
查看答案和解析>>
科目: 来源:2012-2013学年安徽省宣城市、芜湖市七校联考高二(上)期中化学试卷(解析版) 题型:选择题
查看答案和解析>>
科目: 来源:2012-2013学年安徽省宣城市、芜湖市七校联考高二(上)期中化学试卷(解析版) 题型:选择题
查看答案和解析>>
科目: 来源:2012-2013学年安徽省宣城市、芜湖市七校联考高二(上)期中化学试卷(解析版) 题型:选择题
查看答案和解析>>
科目: 来源:2012-2013学年安徽省宣城市、芜湖市七校联考高二(上)期中化学试卷(解析版) 题型:选择题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com