
科目: 来源:2009-2010学年山东省菏泽市高三(上)期末化学试卷(解析版) 题型:选择题
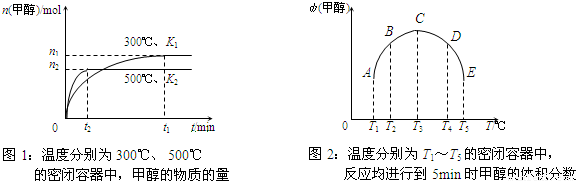
查看答案和解析>>
科目: 来源:2009-2010学年山东省菏泽市高三(上)期末化学试卷(解析版) 题型:选择题
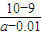 mol?L-1
mol?L-1查看答案和解析>>
科目: 来源:2009-2010学年山东省菏泽市高三(上)期末化学试卷(解析版) 题型:解答题

| 实验名称 | 选用的仪器(填字母) | C或D中所盛试剂(填名称) | C或D中的现象 |
| 区别固体Na2CO3和NaHCO3 | BD | 澄清石灰水 | ______ |
| 铜和浓硫酸反应 | AC | ______ | 溶液红色褪去 |
| 制备乙酸乙酯 | ______ | 饱和碳酸钠溶液 | 上层有透明油状液体产生并有香味 |
查看答案和解析>>
科目: 来源:2009-2010学年山东省菏泽市高三(上)期末化学试卷(解析版) 题型:填空题

 CuSO4溶液
CuSO4溶液 CuSO4?5H2O…CuO
CuSO4?5H2O…CuO查看答案和解析>>
科目: 来源:2009-2010学年山东省菏泽市高三(上)期末化学试卷(解析版) 题型:解答题
查看答案和解析>>
科目: 来源:2009-2010学年山东省菏泽市高三(上)期末化学试卷(解析版) 题型:解答题
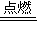 2H2O,设计出以稀硫酸为电解质溶液的燃料电池,其电极反应式为:负极______,正极______.
2H2O,设计出以稀硫酸为电解质溶液的燃料电池,其电极反应式为:负极______,正极______.
查看答案和解析>>
科目: 来源:2009-2010学年山东省菏泽市高三(上)期末化学试卷(解析版) 题型:解答题
查看答案和解析>>
科目: 来源:2009-2010学年山东省菏泽市高三(上)期末化学试卷(解析版) 题型:填空题
| 电离能/kJ?mol-1 | I1 | I2 | I3 | I4 |
| A | 578 | 1817 | 2745 | 11578 |
| B | 738 | 1451 | 7733 | 10540 |
| 共价键 | C-C | C-N | C-S |
| 键能/kJ?mol-1 | 347 | 305 | 259 |
| 离子晶体 | NaCl | KCl | CaO |
| 晶格能/kJ?mol-1 | 786 | 715 | 3401 |

查看答案和解析>>
科目: 来源:2009-2010学年山东省菏泽市高三(上)期末化学试卷(解析版) 题型:填空题

 C
C  …G
…G .
.查看答案和解析>>
科目: 来源:2010-2011学年湖北省武汉市武昌区高二(上)期末化学试卷(解析版) 题型:选择题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com