
科目: 来源: 题型:单选题
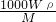
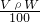
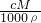
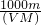
查看答案和解析>>
科目: 来源: 题型:单选题
 2Fe+3CO2
2Fe+3CO2 CaSiO3+CO2↑
CaSiO3+CO2↑查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:单选题
查看答案和解析>>
科目: 来源: 题型:单选题
| 纯净物 | 混合物 | 强电解质 | 弱电解质 | 非电解质 | |
| ① | 青铜 | 水煤气 | 硫酸 | 醋酸 | 干冰 |
| ② | 铁红 | 盐酸 | 硫酸钡 | 亚硫酸 | 二氧化硫 |
| ③ | 胆矾 | 碘酒 | 苛性钾 | 氢硫酸 | 碳酸钙 |
| ④ | 明矾 | 漂白粉 | 氯化钠 | 次氯酸 | 氯气 |
查看答案和解析>>
科目: 来源: 题型:单选题
查看答案和解析>>
科目: 来源: 题型:单选题
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
 O2(g)=H2O(l)△H2=-285.8KJ/mol
O2(g)=H2O(l)△H2=-285.8KJ/mol查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com