相关习题
0 63887 63895 63901 63905 63911 63913 63917 63923 63925 63931 63937 63941 63943 63947 63953 63955 63961 63965 63967 63971 63973 63977 63979 63981 63982 63983 63985 63986 63987 63989 63991 63995 63997 64001 64003 64007 64013 64015 64021 64025 64027 64031 64037 64043 64045 64051 64055 64057 64063 64067 64073 64081 203614
科目:
来源:2012-2013学年辽宁实验中学高二(上)期末化学试卷(解析版)
题型:选择题
当用已知浓度的氢氧化钠溶液滴定未知浓度的盐酸时,下列操作使测定结果(酸的浓度)偏低的是( )
A.碱式滴定管滴至终点,俯视读数
B.碱液移入锥形瓶后,加入10mL蒸馏水
C.碱式滴定管注入碱溶液后,尖嘴有气泡时便开始滴定,滴定后气泡消失
D.碱式滴定管用蒸馏水润洗后,未用标准液润洗
查看答案和解析>>
科目:
来源:2012-2013学年辽宁实验中学高二(上)期末化学试卷(解析版)
题型:选择题
已知室温时,0.1mo1/LCH3COOH在水中有0.1%发生电离,下列叙述正确的是( )
A.该溶液的pH=5
B.升高温度,溶液的pH增大
C.CH3COOH的电离平衡常数约为1×10-6
D.由CH3COOH电离出的c(H+)约为水电离出的c(H+)的106倍
查看答案和解析>>
科目:
来源:2012-2013学年辽宁实验中学高二(上)期末化学试卷(解析版)
题型:选择题
关于下列各装置图的叙述中,不正确的是( )
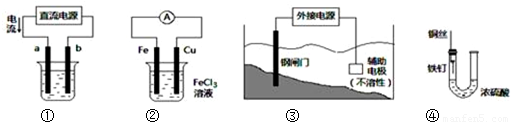
A.用装置①在铁件上镀铜,则a极为铜,电解质为CuSO
4溶液
B.装置②的总反应是:Fe+2Fe
3+=3Fe
2+C.装置③中钢闸门应与外接电源的正极相连
D.装置④中的铁钉几乎没被腐蚀
查看答案和解析>>
科目:
来源:2012-2013学年辽宁实验中学高二(上)期末化学试卷(解析版)
题型:选择题
已知:CaC
2O
4沉淀的Ksp=2.3×10
-9,将等体积的CaCl
2溶液与Na
2C
2O
4溶液混合,若起始CaCl
2的浓度为1×10
-2mo1?L
-1,则生成沉淀所需Na
2C
2O
4溶液的最小起始浓度为( )
A.2.3×10
-7mol?L
-1B.4.6×10
-7mol?L
-1C.9.2×10
-7mol?L
-1D.
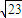
×10
-3mol?L
-1
查看答案和解析>>
科目:
来源:2012-2013学年辽宁实验中学高二(上)期末化学试卷(解析版)
题型:选择题
如图为某化学反应的速率与时间的关系示意图.在t
1时刻升高温度或增大压强,速率的变化都符合示意图的反应是( )
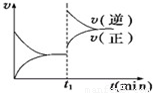
A.2SO
2(g)+O
2(g)?2SO
3(g)△H<0
B.4NH
3(g)+5O
2(g)?4NO(g)+6H
2O(g)△H<0
C.H
2(g)+I
2(g)?2HI(g)△H>0
D.2A(g)+B(g)?2C(g)△H>0
查看答案和解析>>
科目:
来源:2012-2013学年辽宁实验中学高二(上)期末化学试卷(解析版)
题型:选择题
常温下,下列各组离子在指定溶液中可能大量共存的是( )
A.滴入甲基橙显红色的溶液中:Na
+、NO
3ˉ、Iˉ、SO
32ˉ
B.水电离出的 c ( H
+)=10ˉ
12 mol/L 的溶液中:K
+、AlO
2ˉ、CH
3COOˉ、Clˉ
C.

=10ˉ
12 的溶液中:K
+、ClOˉ、S
2ˉ、Clˉ
D.c ( Fe
3+ )=0.1 mol/L 的溶液中:K
+、Clˉ、SO
42ˉ、SCNˉ
查看答案和解析>>
科目:
来源:2012-2013学年辽宁实验中学高二(上)期末化学试卷(解析版)
题型:选择题
铝电池性能优越,Al-AgO电池可用作水下动力电源,其原理如图所示.该电池反应的化学方程式为:2Al+3AgO+2NaOH=2NaAlO
2+3Ag+H
2O,下列说法正确的是( )
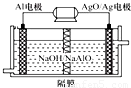
A.该隔膜是阳离子交换膜
B.当电极上析出1.08 g Ag时,电路中转移的电子为0.01 mol
C.Al电极的反应式为:Al-3e
-+4OH
-=AlO
2-+2H
2O
D.正极的电极反应式为:O
2+2H
2O+4e
-=4OH
-
查看答案和解析>>
科目:
来源:2012-2013学年辽宁实验中学高二(上)期末化学试卷(解析版)
题型:选择题
已知KHSO3溶液呈弱酸性.在0.1mol?L-1KHSO3溶液中,下列关系正确的是( )
A.c(K+)+c(H+)=c(HSO3-)+c(OH-)+c(SO32-)
B.c(HSO3-)+c(SO32-)=0.1mol?L-1
C.c(SO32-)<c(H2SO3)
D.c(K+)=c(H2SO3)+c(HSO3-)+c(SO32-)
查看答案和解析>>
科目:
来源:2012-2013学年辽宁实验中学高二(上)期末化学试卷(解析版)
题型:选择题
下列各表述与示意图一致的是( )
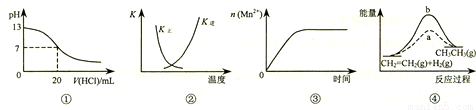
A.图①表示25℃时,用0.1 mol?L
-1盐酸滴定20 mL 0.1 mol?L
-1 NaOH溶液,溶液的pH随加入酸体积的变化
B.图②中曲线表示反应2SO
2(g)+O
2(g)?2SO
3(g)+Q(Q>0)正、逆反应的平衡常数K随温度的变化
C.图③表示10 mL 0.01 mol?L
-1 KMnO
4 酸性溶液与过量的0.1 mol?L
-1 H
2C
2O
4溶液混合时(Mn
2+是该反应的催化剂),n(Mn
2+) 随时间的变化
D.图④中a、b曲线分别表示反应CH
2=CH
2 (g)+H
2(g)→CH
3CH
3(g)+Q(Q>0),使用和未使用催化剂时,反应过程中的能量变化
查看答案和解析>>
科目:
来源:2012-2013学年辽宁实验中学高二(上)期末化学试卷(解析版)
题型:选择题
已知常温下:Ksp[Fe(OH)3]=2.6×10-39;Ksp[Cr(OH)3]=7.0×10-31;Ksp[Zn(OH)2]=1.0×10-17;Ksp[Mg(OH)2]=5.6×10-12.某溶液中有浓度均为0.0l mol/L的Fe3+、Cr3+、Zn2+、Mg2+等离子,加入氢氧化钠溶液,当溶液的pH=6时,下列叙述不正确的是( )
A.Fe3+ 已经沉淀完全
B.Cr3+已经沉淀完全
C.Zn2+ 已经开始沉淀
D.Mg2+还没开始沉淀
查看答案和解析>>


 ×10-3mol?L-1
×10-3mol?L-1
 =10ˉ12 的溶液中:K+、ClOˉ、S2ˉ、Clˉ
=10ˉ12 的溶液中:K+、ClOˉ、S2ˉ、Clˉ
