
科目: 来源:2012-2013学年江苏省泰州市兴化中学高二(上)期中化学试卷(解析版) 题型:选择题
 O2(g)═ZnO(s)△H=-351.1kJ?mol-1
O2(g)═ZnO(s)△H=-351.1kJ?mol-1 O2(g)═HgO(s)△H=-90.7kJ?mol-1由此可知反应
O2(g)═HgO(s)△H=-90.7kJ?mol-1由此可知反应查看答案和解析>>
科目: 来源:2012-2013学年江苏省泰州市兴化中学高二(上)期中化学试卷(解析版) 题型:解答题
| 电离能/kJ?mol-1 | I1 | I2 | I3 | I4 |
| A | 578 | 1817 | 2745 | 11578 |
| B | 738 | 1451 | 7733 | 10540 |
| 离子晶体 | KCl | MgO | CaO |
| 晶格能/kJ?mol-1 | 715 | 3791 | 3401 |
 与
与 互为等电子体,
互为等电子体, 的电子式可表示为______;1mol
的电子式可表示为______;1mol  中含有的π键数目为______.
中含有的π键数目为______.
查看答案和解析>>
科目: 来源:2012-2013学年江苏省泰州市兴化中学高二(上)期中化学试卷(解析版) 题型:解答题
查看答案和解析>>
科目: 来源:2012-2013学年江苏省泰州市兴化中学高二(上)期中化学试卷(解析版) 题型:解答题
查看答案和解析>>
科目: 来源:2012-2013学年江苏省泰州市兴化中学高二(上)期中化学试卷(解析版) 题型:解答题
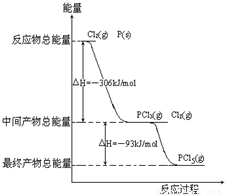
查看答案和解析>>
科目: 来源:2012-2013学年江苏省泰州市兴化中学高二(上)期中化学试卷(解析版) 题型:解答题
| 实验步骤 | 现象 | 结论 |
| ①分别取等体积的2mol/L的硫酸于试管中 ②______ | 反应速率镁>铁,铜不反应 | 金属的性质越活泼,反应速率越快 |
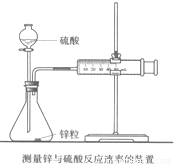
查看答案和解析>>
科目: 来源:2011-2012学年河南省平顶山市高二(上)期末化学试卷(解析版) 题型:选择题
查看答案和解析>>
科目: 来源:2011-2012学年河南省平顶山市高二(上)期末化学试卷(解析版) 题型:选择题
查看答案和解析>>
科目: 来源:2011-2012学年河南省平顶山市高二(上)期末化学试卷(解析版) 题型:选择题
查看答案和解析>>
科目: 来源:2011-2012学年河南省平顶山市高二(上)期末化学试卷(解析版) 题型:选择题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com