
科目: 来源:2012-2013学年广东省潮州市潮安县松昌中学高二(上)期中化学试卷(解析版) 题型:选择题
查看答案和解析>>
科目: 来源:2012-2013学年广东省潮州市潮安县松昌中学高二(上)期中化学试卷(解析版) 题型:选择题
查看答案和解析>>
科目: 来源:2012-2013学年广东省潮州市潮安县松昌中学高二(上)期中化学试卷(解析版) 题型:解答题
 O2(g)=FeO(s)△H=-272.0kJ?mol-1
O2(g)=FeO(s)△H=-272.0kJ?mol-1 O2(g)=Al2O3(s)△H=-1675.7kJ?mol-1
O2(g)=Al2O3(s)△H=-1675.7kJ?mol-1查看答案和解析>>
科目: 来源:2012-2013学年广东省潮州市潮安县松昌中学高二(上)期中化学试卷(解析版) 题型:解答题
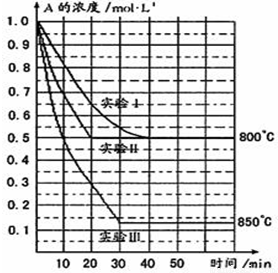
查看答案和解析>>
科目: 来源:2012-2013学年广东省潮州市潮安县松昌中学高二(上)期中化学试卷(解析版) 题型:解答题
| 物质 | CH3OH | CH3OCH3 | H2O |
| 浓度/ | 0.44 | 0.6 | 0.6 |
查看答案和解析>>
科目: 来源:2012-2013学年广东省潮州市潮安县松昌中学高二(上)期中化学试卷(解析版) 题型:解答题
| t℃ | 700 | 800 | 850 | 1000 | 1200 |
| K | 2.6 | 1.7 | 1.0 | 0.9 | 0.6 |
| 时间/min | CO2 (mol/L) | H2 (mol/L) | CO (mol/L) | H2O(mol/L) |
| 0.200 | 0.300 | |||
| 2 | 0.138 | 0.238 | 0.062 | 0.062 |
| 3 | c1 | c2 | c3 | c3 |
| 4 | c1 | c2 | c3 | c3 |
查看答案和解析>>
科目: 来源:2012-2013学年贵州省黔西南州晴隆民族中学高三(上)期中化学试卷(解析版) 题型:选择题
查看答案和解析>>
科目: 来源:2012-2013学年贵州省黔西南州晴隆民族中学高三(上)期中化学试卷(解析版) 题型:选择题
查看答案和解析>>
科目: 来源:2012-2013学年贵州省黔西南州晴隆民族中学高三(上)期中化学试卷(解析版) 题型:选择题
查看答案和解析>>
科目: 来源:2012-2013学年贵州省黔西南州晴隆民族中学高三(上)期中化学试卷(解析版) 题型:选择题
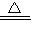 NaCl+NH3↑+H2O
NaCl+NH3↑+H2O查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com