
科目: 来源: 题型:解答题
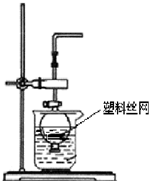 (1)实验是化学研究的基础,下列有关说法中,正确的是______(填序号字母).
(1)实验是化学研究的基础,下列有关说法中,正确的是______(填序号字母).查看答案和解析>>
科目: 来源: 题型:单选题
查看答案和解析>>
科目: 来源: 题型:单选题
查看答案和解析>>
科目: 来源: 题型:单选题
下列关于实验内容与结论相符合的是
| 实验内容 | 结论 | |
| A | 向某溶液中滴加BaCl2溶液,产生白色沉淀 | 溶液中有SO42- |
| B | 向某溶液中滴加AgNO3溶液,产生白色沉淀 | 溶液中有Cl- |
| C | 向某溶液中滴加少量KSCN溶液,溶液变红 | 溶液中有Fe3+ |
| D | 向某溶液中滴加一定量的NaOH溶液,生成白色沉淀 | 溶液中有Al3+ |
查看答案和解析>>
科目: 来源: 题型:单选题
查看答案和解析>>
科目: 来源: 题型:单选题
查看答案和解析>>
科目: 来源: 题型:解答题
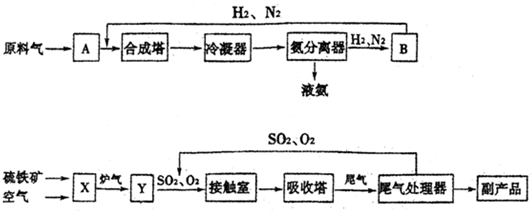
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:单选题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com