
科目: 来源:2011-2012学年江苏省南京三中高二(下)期末化学试卷(解析版) 题型:选择题
查看答案和解析>>
科目: 来源:2011-2012学年江苏省南京三中高二(下)期末化学试卷(解析版) 题型:选择题
查看答案和解析>>
科目: 来源:2011-2012学年江苏省南京三中高二(下)期末化学试卷(解析版) 题型:选择题
| 元素代号 | X | Y | Z | W |
| 原子半径 | 160 | 143 | 70 | 66 |
| 主要化合价 | +2 | +3 | +5、+3、-3 | -2 |
查看答案和解析>>
科目: 来源:2011-2012学年江苏省南京三中高二(下)期末化学试卷(解析版) 题型:选择题
查看答案和解析>>
科目: 来源:2011-2012学年江苏省南京三中高二(下)期末化学试卷(解析版) 题型:选择题
查看答案和解析>>
科目: 来源:2011-2012学年江苏省南京三中高二(下)期末化学试卷(解析版) 题型:选择题
查看答案和解析>>
科目: 来源:2011-2012学年江苏省南京三中高二(下)期末化学试卷(解析版) 题型:选择题
查看答案和解析>>
科目: 来源:2011-2012学年江苏省南京三中高二(下)期末化学试卷(解析版) 题型:选择题
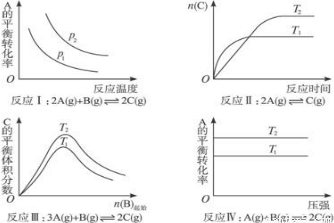
查看答案和解析>>
科目: 来源:2011-2012学年江苏省南京三中高二(下)期末化学试卷(解析版) 题型:选择题
| 容器 | 甲 | 乙 | 丙 |
| 反应物投入量 | 1mol N2、3mol H2 | 2mol NH3 | 4mol NH3 |
| NH3的浓度 | c1 | c2 | c3 |
| 反应的能量变化 | 放出akJ | 吸收bkJ | 吸收ckJ |
| 体系压强(Pa) | p1 | p2 | p3 |
| 反应物转化率 | α1 | α2 | α3 |
查看答案和解析>>
科目: 来源:2011-2012学年江苏省南京三中高二(下)期末化学试卷(解析版) 题型:解答题
 Fe2O3(s)+CO(g)=
Fe2O3(s)+CO(g)= Fe(s)+CO2(g)已知该反应在不同温度下的平衡常数如下:
Fe(s)+CO2(g)已知该反应在不同温度下的平衡常数如下:| 温度/℃ | 1000 | 1150 | 1300 |
| 平衡常数 | 4.0 | 3.7 | 3.5 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com