
科目: 来源:2012-2013学年江西师大附中高三(上)期中化学试卷(解析版) 题型:选择题
查看答案和解析>>
科目: 来源:2012-2013学年江西师大附中高三(上)期中化学试卷(解析版) 题型:选择题
查看答案和解析>>
科目: 来源:2012-2013学年江西师大附中高三(上)期中化学试卷(解析版) 题型:选择题
查看答案和解析>>
科目: 来源:2012-2013学年江西师大附中高三(上)期中化学试卷(解析版) 题型:选择题
查看答案和解析>>
科目: 来源:2012-2013学年江西师大附中高三(上)期中化学试卷(解析版) 题型:解答题
查看答案和解析>>
科目: 来源:2012-2013学年江西师大附中高三(上)期中化学试卷(解析版) 题型:解答题
查看答案和解析>>
科目: 来源:2012-2013学年江西师大附中高三(上)期中化学试卷(解析版) 题型:解答题
 C(s)=
C(s)= CO2(g)+2Fe (s)△H=+b KJ/mol
CO2(g)+2Fe (s)△H=+b KJ/mol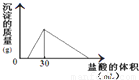
查看答案和解析>>
科目: 来源:2012-2013学年江西师大附中高三(上)期中化学试卷(解析版) 题型:解答题
查看答案和解析>>
科目: 来源:2012-2013学年江西师大附中高三(上)期中化学试卷(解析版) 题型:解答题

| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Al(OH)3 |
| 开始沉淀 | 2.3 | 7.5 | 3.4 |
| 完全沉淀 | 3.2 | 9.7 | 4.4 |
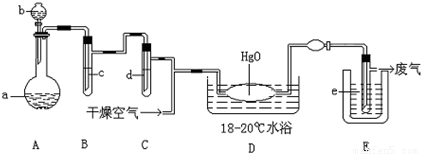
 LiFePO4,电池中的固体电解质可传导Li+.试写出该电池充电时的阳极反应式______.
LiFePO4,电池中的固体电解质可传导Li+.试写出该电池充电时的阳极反应式______.查看答案和解析>>
科目: 来源:2010-2011学年江西省上饶五中高一(下)期中化学试卷(解析版) 题型:选择题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com