相关习题
0 65244 65252 65258 65262 65268 65270 65274 65280 65282 65288 65294 65298 65300 65304 65310 65312 65318 65322 65324 65328 65330 65334 65336 65338 65339 65340 65342 65343 65344 65346 65348 65352 65354 65358 65360 65364 65370 65372 65378 65382 65384 65388 65394 65400 65402 65408 65412 65414 65420 65424 65430 65438 203614
科目:
来源:2012-2013学年四川省成都外国语学校高二(上)期中化学试卷(解析版)
题型:选择题
短周期元素W、X、Y、Z的原子序数依次增大,其中W的阴离子的核外电子数与X、Y、Z原子的核外内层电子数相同.X的一种核素在考古时常用来鉴定一些文物的年代,工业上采用液态空气分馏方法来生产Y的单质,而Z不能形成双原子分子.根据以上叙述,下列说法中正确的是( )
A.上述四种元素的原子半径大小为W<X<Y<Z
B.W、X、Y、Z原子的核外最外层电子数的总和为20
C.W与Y可形成既含极性共价键又含非极性共价键的化合物
D.由W与X组成的化合物的沸点总低于由W与Y组成的化合物的沸点
查看答案和解析>>
科目:
来源:2012-2013学年四川省成都外国语学校高二(上)期中化学试卷(解析版)
题型:选择题
下列关于晶体说法的正确组合是( )
①分子晶体中都存在共价键
②在晶体中只要有阳离子就一定有阴离子
③金刚石、SiC、NaF、NaCl、H
2O、H
2S晶体的熔点依次降低
④离子晶体中只有离子键没有共价键,分子晶体中肯定没有离子键
⑤CaTiO
3晶体中(晶胞结构如图所示)每个Ti
4+和12个O
2-紧邻
⑥60gSi0
2中含Si-O键的个数为2N
A⑦晶体中分子间作用力越大,分子越稳定
⑧氯化钠熔化时离子键被破坏
⑨124g P
4含有P-P键的个数为4N
A.

A.①②③⑥
B.①②④
C.③⑤⑦
D.③⑤⑧
查看答案和解析>>
科目:
来源:2012-2013学年四川省成都外国语学校高二(上)期中化学试卷(解析版)
题型:选择题
三氯化氮(NCl3)常温是一种淡黄色液体,其分子结构呈三角锥形,以下关于NCl3的说法中正确的是( )
A.它是一种非极性分子
B.它能以配位键与Cl-结合,生成NCl4-
C.NCl3中N原子采用SP2杂化
D.已知NCl3中N元素为-3价,所以NCl3水解产物为NH3和HClO
查看答案和解析>>
科目:
来源:2012-2013学年四川省成都外国语学校高二(上)期中化学试卷(解析版)
题型:选择题
X、Y两元素的质子数之和为22,X的原子核外电子数比Y少6个,下列说法中不正确的是( )
A.Y的单质是金属晶体
B.X的单质固态时为分子晶体
C.X与碳形成的化合物为分子晶体
D.X与Y形成的化合物固态时为分子晶体
查看答案和解析>>
科目:
来源:2012-2013学年四川省成都外国语学校高二(上)期中化学试卷(解析版)
题型:选择题
已知三角锥形分子E和直线形分子G反应,生成两种直线形分子L和M(组成E、G、L、M分子的元素原子序数均小于10)如图,则下列判断错误的是( )

A.G是电负性最大的元素
B.1个M分子中有2个σ键
C.E易液化是因为相对分子质量较大
D.L是极性分子
查看答案和解析>>
科目:
来源:2012-2013学年四川省成都外国语学校高二(上)期中化学试卷(解析版)
题型:选择题
原子间以共价单键相连的非金属单质中,一个原子与相邻原子的成键数为8-N,N为该非金属元素的族序数,化学家把这一现象称为8-N规则.某非金属单质的结构如图所示,则构成该单质的元素位于( )
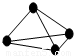
A.ⅢA
B.ⅣA
C.ⅤA
D.ⅥA
查看答案和解析>>
科目:
来源:2012-2013学年四川省成都外国语学校高二(上)期中化学试卷(解析版)
题型:选择题
“类推”是一种常用的学习方法,但有时会产生错误的结论,下列类推结论中正确的是( )
A.ⅣA族元素氢化物沸点顺序是:GeH4>SiH4>CH4;则ⅤA族元素氢化物沸点顺序也是:AsH3>PH3>NH3
B.第二周期元素氢化物的稳定性序是:HF>H2O>NH3;则第三周期元素氢化物的稳定性顺序也是:HCl>H2S>PH3
C.晶体中有阴离子,必有阳离子;则晶体中有阳离子,必有阴离子
D.干冰(CO2)是分子晶体,则SiO2也是分子晶体
查看答案和解析>>
科目:
来源:2012-2013学年四川省成都外国语学校高二(上)期中化学试卷(解析版)
题型:选择题
有X、Y、Z、W、M五种短周期元素,其中X、Y、Z、W同周期,Z、M同主族; X+与M2-具有相同的电子层结构;离子半径:Z2->W-;Y的单质晶体熔点高、硬度大,是一种重要的半导体材料.下列说法中,正确的是( )
A.X、M两种元素只能形成X2M型化合物
B.由于W、Z、M元素的氢化物相对分子质量依次减小,所以其沸点依次降低
C.元素Y、Z、W的单质晶体属于同种类型的晶体
D.元素W和M的某些单质可作为水处理中的消毒剂
查看答案和解析>>
科目:
来源:2012-2013学年四川省成都外国语学校高二(上)期中化学试卷(解析版)
题型:选择题
已知X、Y元素同周期,且电负性X>Y,下列说法错误的是( )
A.X与Y形成化合物是,X显负价,Y显正价
B.第一电离能可能Y大于X
C.当它们均为非金属时,气态氢化物的稳定性:X大于Y
D.当它们均为非金属时,最高价含氧酸的酸性:X小于Y
查看答案和解析>>
科目:
来源:2012-2013学年四川省成都外国语学校高二(上)期中化学试卷(解析版)
题型:选择题
人们常将在同一原子轨道上运动的,自旋方向相反的2个电子,称为“电子对”;将在同一原子轨道上运动的单个电子,称为“未成对电子”.以下有关主族元素原子的“未成对电子”的说法,错误的是( )
A.核外电子数为奇数的基态原子,其原子轨道中一定含有“未成对电子”
B.核外电子数为偶数的基态原子,其原子轨道中一定不含“未成对电子”
C.核外电子数为偶数的基态原子,其原子轨道中可能含有“未成对电子”
D.核外电子数为奇数的基态原子,其原子轨道中可能不含“未成对电子”
查看答案和解析>>



