相关习题
0 65880 65888 65894 65898 65904 65906 65910 65916 65918 65924 65930 65934 65936 65940 65946 65948 65954 65958 65960 65964 65966 65970 65972 65974 65975 65976 65978 65979 65980 65982 65984 65988 65990 65994 65996 66000 66006 66008 66014 66018 66020 66024 66030 66036 66038 66044 66048 66050 66056 66060 66066 66074 203614
科目:
来源:《第2章 化学反应与能量》2010年单元测试卷(开封一中)(解析版)
题型:选择题
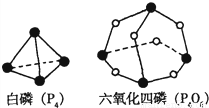
化学反应可视为旧键断裂和新键形成的过程.化学键的键能是形成(或拆开)1mol化学键时释放(或吸收)的能量.已知白磷(P
4)和P
4O
6的分子结构如图所示;
现提供以下化学键的键能:P-P 198KJ?mol
-1、P-O 360kJ?mol
-1、氧气分子内氧原子间的键能为498kJ?mol
-1则P
4+3O
2═P
4O
6的反应热△H为( )
A.+1638kJ?mol
-1B.-1638kJ?mol
-1C.-126kJ?mol
-1D.+126kJ?mol
-1
查看答案和解析>>
科目:
来源:《第2章 化学反应与能量》2010年单元测试卷(开封一中)(解析版)
题型:选择题
在36g 碳不完全燃烧所得气体中,CO占

体积,CO
2占

体积,且C(s)+

O
2(g)=CO(g)△H=-110.5kJ/mol;CO(g)+

O
2(g)=CO
2(g)△H=-283kJ/mol.与这些碳完全燃烧相比,损失的热量是( )
A.172.5kJ
B.1149kJ
C.283kJ
D.517.5kJ
查看答案和解析>>
科目:
来源:《第2章 化学反应与能量》2010年单元测试卷(开封一中)(解析版)
题型:选择题
充分燃烧一定量丁烷气体放出的热量为Q,完全吸收它生成的CO2生成正盐,需要5mol?L-1 的KOH溶液100mL,则丁烷的燃烧热为( )(单位:kJ/mol)
A.16Q
B.8Q
C.4Q
D.2Q
查看答案和解析>>
科目:
来源:《第2章 化学反应与能量》2010年单元测试卷(开封一中)(解析版)
题型:填空题
盖斯定律在生产和科学研究中有很重要的意义.有些反应的反应热虽然无法直接测得,但可通过间接的方法测定.现根据下列3个热化学反应方程式:
Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g)△H=-24.8kJ/mol
3Fe2O3(s)+CO(g)=2Fe3O4(s)+CO2(g)△H=-47.2kJ/mol
Fe3O4(s)+CO(g)=3FeO(s)+CO2(g)△H=+640.5kJ/mol
写出CO气体还原FeO固体得到Fe固体和CO2气体的热化学反应方程式: .
查看答案和解析>>
科目:
来源:《第2章 化学反应与能量》2010年单元测试卷(开封一中)(解析版)
题型:填空题
按照盖斯定律,结合下列反应方程式,回答问题.已知:
(1)NH3(g)+HCl(g)=NH4Cl(s)△H=-176KJ?mol-1
(2)NH3(g)+H2O(l)=NH3?H2O(aq)△H=-35.1KJ?mol-1
(3)HCl(g)+H2O(l)=HCl(aq)△H=-72.3KJ?mol-1
(4)NH3?H2O(aq)+HCl(aq)=NH4Cl(aq)+H2O(l)△H=-52.3KJ?mol-1
(5)NH4Cl(S)+H2O(l)=NH4Cl(aq)△H=Q
则第(5)个方程式中的反应热是 KJ?mol-1.
查看答案和解析>>
科目:
来源:《第2章 化学反应与能量》2010年单元测试卷(开封一中)(解析版)
题型:填空题
CH
3-CH
3→CH
2=CH
2+H
2,有关化学键的键能如下:
| 化学键 | C-H | C=C | C-C | H-H |
| 键能(kJ/mol) | 414.4 | 615.3 | 347.4 | 435.3 |
计算该反应的反应热.
kJ/mol.
查看答案和解析>>
科目:
来源:《第2章 化学反应与能量》2010年单元测试卷(开封一中)(解析版)
题型:填空题
10g硫磺在O2中完全燃烧生成气态SO2,放出的热量能量使500g H2O温度由18℃升至62.4℃,则硫磺的燃烧热为 ,热化学方程式为 .
查看答案和解析>>
科目:
来源:《第2章 化学反应与能量》2010年单元测试卷(开封一中)(解析版)
题型:填空题
硝化甘油(C3H5N3O9)分解时产物为N2、CO2、O2和液态水,它的分解反应的化学方程式是 .
已知20℃时,22.7g硝化甘油分解放出的热量为154KJ,则每生成1mol气体伴随放出的热量为 KJ.
查看答案和解析>>
科目:
来源:《第2章 化学反应与能量》2010年单元测试卷(开封一中)(解析版)
题型:填空题
已知下列两个热化学方程式:2H2(g)+O2(g)=2H2O(l);△H=-571.6kJ?mol-1
C3H8(g)+5O2(g)=3CO2(g)+4H2O(l);△H=-2220kJ?mol-1
根据上面两个热化学方程式,试回答下列问题:
(1)H2的燃烧热为 ,C3H8的燃烧热为 .
(2)1mol H2和2mol C3H8组成的混合气体完全燃烧释放的热量为 .
(3)现有H2和C3H8的混合气体共5mol,完全燃烧时放热3 847kJ,则在混合气体中H2和C3H8的体积比是 .
查看答案和解析>>
科目:
来源:《第2章 化学反应与能量》2010年单元测试卷(开封一中)(解析版)
题型:填空题
依据事实,写出下列反应的热化学方程式.
(1)在25℃、101kPa下,1g甲醇燃烧生成CO2和液态水时放热22.68kJ.则表示甲醇燃烧热的热化学方程式为
(2)若适量的N2和O2完全反应,每生成23克NO2需要吸收16.95kJ热量.
(3)用NA表示阿伏加德罗常数,在C2H2(气态)完全燃烧生成CO2和液态水的反应中,每有5NA个电子转移时,放出650kJ的热量.
(4)已知拆开1molH-H键,1molN-H键,1molN≡N键分别需要的能量是436kJ、391kJ、946kJ,则N2与H2反应生成NH3的热化学方程式为 .
查看答案和解析>>


 体积,CO2占
体积,CO2占 体积,且C(s)+
体积,且C(s)+ O2(g)=CO(g)△H=-110.5kJ/mol;CO(g)+
O2(g)=CO(g)△H=-110.5kJ/mol;CO(g)+ O2(g)=CO2(g)△H=-283kJ/mol.与这些碳完全燃烧相比,损失的热量是( )
O2(g)=CO2(g)△H=-283kJ/mol.与这些碳完全燃烧相比,损失的热量是( )