相关习题
0 66013 66021 66027 66031 66037 66039 66043 66049 66051 66057 66063 66067 66069 66073 66079 66081 66087 66091 66093 66097 66099 66103 66105 66107 66108 66109 66111 66112 66113 66115 66117 66121 66123 66127 66129 66133 66139 66141 66147 66151 66153 66157 66163 66169 66171 66177 66181 66183 66189 66193 66199 66207 203614
科目:
来源:2010-2011学年山东省临沂市费县一中高三(上)期末化学模拟试卷(解析版)
题型:填空题
将某一元酸HA与NaOH等体积混合,请根据题目要求回答下列问题:
(1)若c(HA)=c(NaOH)=O.lmol/L,测得混合后溶液的pH>7.
①HA是弱电解质,能证明HA是弱电解质的方法是 .
A测得0.1mol/L HA的pH>l B.测得NaA溶液的pH>7
C.pH=l的HA与盐酸,稀释10倍后,盐酸的pH变化大
D.用足量的锌分别与相同pH、相同体积的盐酸和HA反应,产生氢气一样多
②混合溶液中,关系式一定正确的是 .
A.c(A-)>c(Na+)c(OH-)>c(H+) B.c(A-)+c(OH-)=c(Na+)+c(H+)
C.c(HA)+c(A-)=0.1mol/L D.f( HA)+c( H+)=c(OH-)
③若HA(少量)+B2一═A一+HB-;H2B(少量)+2C-═B2-+2HC:HA+C-═A-十HC- 则相同pH的①NaA ②Na,B ③NaHB ④NaC的四种溶液,各物质的物质的量浓度从大到小的顺序为 (填序号).
(2)若c( HA)═c(NaOH)═0.1mol/L,测得混合后溶液的pH=7.
①现将一定浓度的HA稀释10倍后溶液的pH与该浓度的HA和0.1mol/L NaOH等体积混合后溶液的pH相等,则HA溶液的浓度为 .
②用标准的NaOH溶液滴定未知浓度的HA时,下列操作能引起所测HA浓度偏大的是 .
A.用蒸馏水洗涤锥形瓶后,用待测HA溶液进行润洗
B.滴定前发现滴定管的尖嘴部分有气泡,滴定后消失
C.装NaOH的碱式滴定管未用标准的NaOH溶液润洗
D.滴定前仰视,滴定后俯视读数.
查看答案和解析>>
科目:
来源:2011-2012学年吉林省长春二中高二(上)期末化学试卷(解析版)
题型:选择题
下列关于铜电极的叙述中正确的是( )
A.铜锌原电池中铜是负极
B.用电解法精炼粗铜时粗铜作阳极
C.在铁上电镀铜时用铜作阴极
D.电解稀硫酸时用铜作阳极,阳极产生氧气
查看答案和解析>>
科目:
来源:2011-2012学年吉林省长春二中高二(上)期末化学试卷(解析版)
题型:选择题
已知反应mX(g)+nY(g)?qZ(g);△H<0,m+n>q,在恒容密闭容器中反应达到平衡时,下列说法正确的是( )
A.通入稀有气体使压强增大,平衡将正向移动
B.X的正反应速率是Y的逆反应速率的m/n倍
C.降低温度,混合气体的平均相对分子质量变小
D.若平衡时X、Y的转化率相等,说明反应开始时X、Y的物质的量之比为n:m
查看答案和解析>>
科目:
来源:2011-2012学年吉林省长春二中高二(上)期末化学试卷(解析版)
题型:选择题
铁-镍蓄电池放电和充电时发生的反应为:Fe+NiO
2+2H
2O

Fe(OH)
2+Ni(OH)
2关于此蓄电池的下列说法中不正确的是( )
A.放电时铁为负极
B.充电时阴极的电极反应式为:Ni(OH)
2-2e
-=NiO
2+2H
+C.放电时NiO
2的反应为:NiO
2+2H
2O+2e
-=Ni(OH)
2+2OH
-D.蓄电池的电极必须浸在碱性电解质溶液中
查看答案和解析>>
科目:
来源:2011-2012学年吉林省长春二中高二(上)期末化学试卷(解析版)
题型:选择题
将2mol SO2,1mol O2 充入带活塞的密闭容器中,发生反应2SO2(g)+O2(g)?2SO3(g),达到平衡后,改变下列条件,SO3的平衡浓度不改变的是( )
A.保持温度和容器的压强不变,充入1mol SO3(g)
B.保持温度和容器的容积不变,充入1mol SO3(g)
C.保持温度和容器的压强不变,充入1mol O2(g)
D.保持温度和容器的压强不变,充入1mol Ar
查看答案和解析>>
科目:
来源:2011-2012学年吉林省长春二中高二(上)期末化学试卷(解析版)
题型:选择题
某烷烃的各种同分异构体中,主链上有4个碳原子的只有两种结构,则含有相同碳原子数且主链上也有4个碳原子的烯烃(只含一个碳碳双键)的同分异构体有( )
A.2种
B.3种
C.4种
D.5种
查看答案和解析>>
科目:
来源:2011-2012学年吉林省长春二中高二(上)期末化学试卷(解析版)
题型:选择题
已知N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ/mol.在一恒温恒压的密闭容器里充入2mol N2和8mol H2达到平衡时生成1mol NH3.现在相同条件下的同一容器中充入xmol N2,ymol H2和2mol NH3,达到平衡时,NH3的质量分数与原来相同,且放出热量46.2kJ.则x、y的值为( )
A.1.5,6.5
B.2,8
C.5,21
D.3,13
查看答案和解析>>
科目:
来源:2011-2012学年吉林省长春二中高二(上)期末化学试卷(解析版)
题型:选择题
如图所示,表示反应2SO
2(g)+O
2 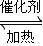
2SO
3(g),△H<0的正反应速率随时间的变化情况,试根据此曲线判断下列说法可能正确的是( )
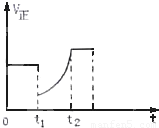
A.t
1时增加了SO
2和O
2的浓度,平衡向正反应方向移动
B.t
1降低了温度,平衡向正反应方向移动
C.t
1时减小了压强,平衡向逆反应方向移动
D.t
1时减小了SO
2的浓度,增加了SO
3的浓度,平衡向逆反应方向移动
查看答案和解析>>
科目:
来源:2011-2012学年吉林省长春二中高二(上)期末化学试卷(解析版)
题型:选择题
浓度为2mol?L-1的氢溴酸溶液VL,欲使其浓度变为4mol?L-1,以下列出的方法中,可行的为( )
A.通入标况下的HBr气体44.8L
B.加入10 mol?L-1氢溴酸0.6VL,再将溶液稀释至2VL
C.蒸发掉0.5L水
D.将溶液加热蒸发浓缩至0.5V
查看答案和解析>>
科目:
来源:2011-2012学年吉林省长春二中高二(上)期末化学试卷(解析版)
题型:选择题
已知25℃时,AgI饱和溶液中c(Ag+)为1.22×10-8mol/L,AgCl的饱和溶液中c(Ag+)为1.25×10-5mol/L.若在5mL含有KCl和KI各为0.01mol/L的溶液中,加入8mL0.01mol/LAgNO3溶液,这时溶液中所含溶质的离子浓度大小关系正确的是( )
A.c(K+)>c(NO3-)>c(Ag+)=c(Cl-)+c(I-)
B.c(K+)>c(NO3-)>c(Ag+)>c(Cl-)>c(I-)
C.c(NO3-)>c(K+)>c(Ag+)>c(Cl-)>c(I-)
D.c(K+)>c(NO3-)>c(Cl-)>c(Ag+)>c(I-)
查看答案和解析>>

 Fe(OH)2+Ni(OH)2关于此蓄电池的下列说法中不正确的是( )
Fe(OH)2+Ni(OH)2关于此蓄电池的下列说法中不正确的是( )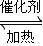 2SO3(g),△H<0的正反应速率随时间的变化情况,试根据此曲线判断下列说法可能正确的是( )
2SO3(g),△H<0的正反应速率随时间的变化情况,试根据此曲线判断下列说法可能正确的是( )