
科目: 来源:2013年安徽省高考化学试卷(解析版) 题型:选择题
 CO2+H2O.下列有关说法正确的是( )
CO2+H2O.下列有关说法正确的是( )查看答案和解析>>
科目: 来源:2013年安徽省高考化学试卷(解析版) 题型:选择题
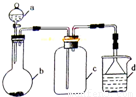
| 选项 | a中的物质 | b中的物质 | c中收集的气体 | d中的物质 |
| A | 浓氨水 | CaO | NH3 | H2O |
| B | 浓硫酸 | Na2SO3 | SO2 | NaOH溶液 |
| C | 稀硝酸 | Cu | NO2 | H2O |
| D | 浓盐酸 | MnO2 | Cl2 | NaOH溶液 |
查看答案和解析>>
科目: 来源:2013年安徽省高考化学试卷(解析版) 题型:选择题
 、NH3?H2O
、NH3?H2O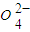 、葡萄糖分子
、葡萄糖分子查看答案和解析>>
科目: 来源:2013年安徽省高考化学试卷(解析版) 题型:选择题
查看答案和解析>>
科目: 来源:2013年安徽省高考化学试卷(解析版) 题型:选择题
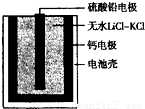
| 选项 | x | y |
| A | 温度 | 容器内混合气体的密度 |
| B | CO的物质的量 | CO2与CO的物质的量之比 |
| C | SO2的浓度 | 平衡常数K |
| D | MgSO4的质量(忽略体积) | CO的转化率 |

查看答案和解析>>
科目: 来源:2013年安徽省高考化学试卷(解析版) 题型:选择题
查看答案和解析>>
科目: 来源:2013年安徽省高考化学试卷(解析版) 题型:选择题
 +H2O?H2SO3+OH-①
+H2O?H2SO3+OH-①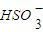 ?H++
?H++ ②,向0.1mol?L-1的NaHSO3溶液中分别加入以下物质,下列有关说法正确的是( )
②,向0.1mol?L-1的NaHSO3溶液中分别加入以下物质,下列有关说法正确的是( ) )增大
)增大 )+c(OH-)+
)+c(OH-)+ c(
c( )
) 的值均增大
的值均增大 )>c(H+)=c(OH-)
)>c(H+)=c(OH-)查看答案和解析>>
科目: 来源:2013年安徽省高考化学试卷(解析版) 题型:解答题
| 元素 | 相关信息 |
| X | X的最高价氧化物对应的水化物化学式为H2XO3 |
| Y | Y是地壳中含量最高的元素 |
| Z | Z的基态原子最外层电子排布式为3s23p1 |
| W | W的一种核素的质量数为28,中子数为14 |
查看答案和解析>>
科目: 来源:2013年安徽省高考化学试卷(解析版) 题型:解答题
查看答案和解析>>
科目: 来源:2013年安徽省高考化学试卷(解析版) 题型:解答题
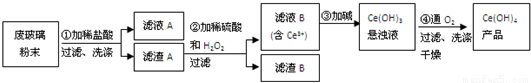
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com