
科目: 来源:2013年上海市闸北区高考化学二模试卷(解析版) 题型:选择题
查看答案和解析>>
科目: 来源:2013年上海市闸北区高考化学二模试卷(解析版) 题型:填空题
 4AlCl3+3O2↑.请回答下列问题:
4AlCl3+3O2↑.请回答下列问题: Ga,其原子在天然同位素原子中所占的百分比为60%.实验测得溴化镓(GaBr3)的摩尔质量为309.8g/mol,则由此推知镓的另一种同位素是 .
Ga,其原子在天然同位素原子中所占的百分比为60%.实验测得溴化镓(GaBr3)的摩尔质量为309.8g/mol,则由此推知镓的另一种同位素是 .查看答案和解析>>
科目: 来源:2013年上海市闸北区高考化学二模试卷(解析版) 题型:填空题
查看答案和解析>>
科目: 来源:2013年上海市闸北区高考化学二模试卷(解析版) 题型:填空题
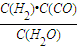 ,它所对应反应的化学方程式是 .
,它所对应反应的化学方程式是 .| 物质 | H2 | CO | CH3OH |
| 浓度(mol/L) | 0.2 | 0.1 | 0.4 |
| 反应 | 大气固氮 | 工业固氮 | ||||
| 温度/℃ | 27 | 2000 | 25 | 350 | 400 | 450 |
| K | 3.84×10-31 | 0.1 | 5×108 | 1.847 | 0.507 | 0.152 |
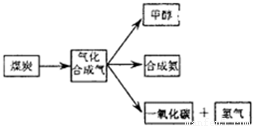
查看答案和解析>>
科目: 来源:2013年上海市闸北区高考化学二模试卷(解析版) 题型:填空题
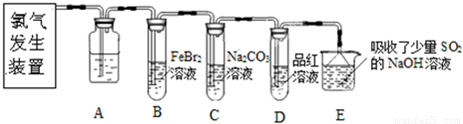
查看答案和解析>>
科目: 来源:2013年上海市闸北区高考化学二模试卷(解析版) 题型:填空题

查看答案和解析>>
科目: 来源:2013年上海市闸北区高考化学二模试卷(解析版) 题型:填空题
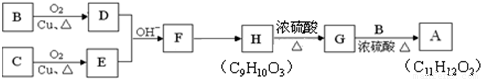

查看答案和解析>>
科目: 来源:2013年上海市闸北区高考化学二模试卷(解析版) 题型:填空题


查看答案和解析>>
科目: 来源:2013年上海市闸北区高考化学二模试卷(解析版) 题型:解答题
| 装置 | A (试管+粉末) | B | C |
| 反应前 | 42.0g | 75.0g | 140.0g |
| 反应后 | 37.0g | 79.0g | 140.5g |
 Na2S+4CO ②Na2SO4+4CO
Na2S+4CO ②Na2SO4+4CO Na2S+4CO2
Na2S+4CO2
查看答案和解析>>
科目: 来源:2013年高考化学备考复习卷C9:有机化学(一)(解析版) 题型:选择题
 2-甲基丁烷
2-甲基丁烷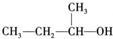 2-甲基-1-丙醇
2-甲基-1-丙醇查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com