
科目: 来源:2009年江苏省南通市通州区平潮高级中学高考化学模拟试卷(十)(解析版) 题型:解答题

查看答案和解析>>
科目: 来源:2009年江苏省南通市通州区平潮高级中学高考化学模拟试卷(十)(解析版) 题型:填空题
 12Na2CrO4+3Fe2O3+7KCl+12H2O,然后将铬酸钠转化为K2Cr2O7.其主要工艺如下:
12Na2CrO4+3Fe2O3+7KCl+12H2O,然后将铬酸钠转化为K2Cr2O7.其主要工艺如下:
查看答案和解析>>
科目: 来源:2009年江苏省南通市通州区平潮高级中学高考化学模拟试卷(十)(解析版) 题型:解答题

 由甲苯与氯气在光照条件下反应生成,甲苯在工业上可通过下列流程获得:
由甲苯与氯气在光照条件下反应生成,甲苯在工业上可通过下列流程获得: 请在括号中填写加工方法或操作名称______、______.
请在括号中填写加工方法或操作名称______、______.查看答案和解析>>
科目: 来源:2009年江苏省南通市通州区平潮高级中学高考化学模拟试卷(十)(解析版) 题型:解答题
| 乙炔水化法 | 乙烯氧化法 | |
| 原料 | 乙炔、水 | 乙烯、空气 |
| 反应条件 | HgSO4、100~125℃ | PdCl2-CuCl2、100~125℃ |
| 平衡转化率 | 乙炔平衡转化率90%左右 | 乙烯平衡转化率80%左右 |
| 日产量 | 2.5吨(某设备条件下) | 3.6吨(相同设备条件下) |
| 原料生产工艺过程 | |
| 乙炔 | CaCO3 CaO CaO CaC2 CaC2 C2H2 C2H2 |
| 乙烯 | 来源于石油裂解气 |
查看答案和解析>>
科目: 来源:2009年江苏省南通市通州区平潮高级中学高考化学模拟试卷(十)(解析版) 题型:解答题
| 元素 | A | B | C | D |
| 性质 结构 信息 | 原子核外有两个电子层,最外层有3个未成对的电子 | 原子的M层有1对成对的p电子 | 原子核外电子排布为[Ar]3d104sx, 有+1、+2两种常见化合价 | 有两种常见氧化物,其中有一种是冶金工业常用的还原剂 |
 ”表示上述相关元素的原子中除去最外层电子的剩余部分,“
”表示上述相关元素的原子中除去最外层电子的剩余部分,“ ”表示氢原子,小黑点“?”表示没有形成共价键的最外层电子,短线表示共价键.
”表示氢原子,小黑点“?”表示没有形成共价键的最外层电子,短线表示共价键.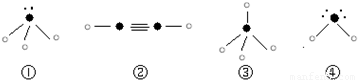
查看答案和解析>>
科目: 来源:2009年湖北省黄冈市黄州中学高考化学二模试卷(解析版) 题型:选择题
查看答案和解析>>
科目: 来源:2009年湖北省黄冈市黄州中学高考化学二模试卷(解析版) 题型:选择题



查看答案和解析>>
科目: 来源:2009年湖北省黄冈市黄州中学高考化学二模试卷(解析版) 题型:选择题
查看答案和解析>>
科目: 来源:2009年湖北省黄冈市黄州中学高考化学二模试卷(解析版) 题型:选择题
| 选项 | 实验操作 | 实验目的 |
| A | 向沸腾的NaOH溶液中滴加FeCl3饱和溶液 | 制备Fe(OH)3胶体 |
| B | 检验NaHCO3固体中是否含Na2CO3 | 试样加水溶解后,再加入足量CaCl2溶液,有白色沉淀 |
| C | 向丙烯醛中滴加酸性高锰酸钾溶液,振荡后观察溶液是否褪色 | 确定丙烯醛中是否含有碳碳双键 |
| D | C2H5Br和NaOH溶液混合后振荡再加入AgNO3溶液 | 检验C2H5Br中的Br元素 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com