
科目: 来源:2010年江苏省苏州中学高考化学三模试卷(解析版) 题型:选择题

查看答案和解析>>
科目: 来源:2010年江苏省苏州中学高考化学三模试卷(解析版) 题型:选择题
| 反应 | △E |
| CH3C≡CCH3+2H2→CH3CH2CH2CH3 | 278kJ/mol |
| CH2═CH-CH═CH2+2H2→CH3CH2CH2CH3 | 239kJ/mol |

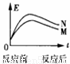 已知消去反应是吸热反应,则CH3CHBrCHBrCH3与NaOH的醇溶液共热生成M、N时能量变化的示意图为:
已知消去反应是吸热反应,则CH3CHBrCHBrCH3与NaOH的醇溶液共热生成M、N时能量变化的示意图为:查看答案和解析>>
科目: 来源:2010年江苏省苏州中学高考化学三模试卷(解析版) 题型:选择题
查看答案和解析>>
科目: 来源:2010年江苏省苏州中学高考化学三模试卷(解析版) 题型:选择题
 、NH4Cl溶液中c(H+)分别为c1、c2、c3、c4,则c4>c3>c2>c1
、NH4Cl溶液中c(H+)分别为c1、c2、c3、c4,则c4>c3>c2>c1查看答案和解析>>
科目: 来源:2010年江苏省苏州中学高考化学三模试卷(解析版) 题型:选择题
 4Na+O2↑+2H2O;后来盖?吕萨克用铁与熔融氢氧化钠作用也制得钠,反应原理为:3Fe+4NaOH
4Na+O2↑+2H2O;后来盖?吕萨克用铁与熔融氢氧化钠作用也制得钠,反应原理为:3Fe+4NaOH  Fe3O4+2H2↑十4Na↑.下列有关说法正确的是( )
Fe3O4+2H2↑十4Na↑.下列有关说法正确的是( )
查看答案和解析>>
科目: 来源:2010年江苏省苏州中学高考化学三模试卷(解析版) 题型:选择题
查看答案和解析>>
科目: 来源:2010年江苏省苏州中学高考化学三模试卷(解析版) 题型:选择题

查看答案和解析>>
科目: 来源:2010年江苏省苏州中学高考化学三模试卷(解析版) 题型:选择题

查看答案和解析>>
科目: 来源:2010年江苏省苏州中学高考化学三模试卷(解析版) 题型:解答题



查看答案和解析>>
科目: 来源:2010年江苏省苏州中学高考化学三模试卷(解析版) 题型:解答题

 BaS+CO↑
BaS+CO↑ BaS溶液
BaS溶液查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com