
科目: 来源:2011年浙江省杭州市萧山区高考化学模拟试卷(十九)(解析版) 题型:填空题
 ;六种元素在周期表中的位置关系是:A、B同主族,C、D也同主族;C、E相邻,B、F也相邻.
;六种元素在周期表中的位置关系是:A、B同主族,C、D也同主族;C、E相邻,B、F也相邻.查看答案和解析>>
科目: 来源:2011年浙江省杭州市萧山区高考化学模拟试卷(十九)(解析版) 题型:填空题
 CO(g)+H2(g)△H=+131.3kJ?mol-1,
CO(g)+H2(g)△H=+131.3kJ?mol-1,| 化学键 | C-O | C-H | H-H | C≡O | O-H |
| 键能 kg/mol-1 | 358 | 413 | 436 | 1072 | 463 |
 2NH3(g)△H=-92.4kJ/mol
2NH3(g)△H=-92.4kJ/mol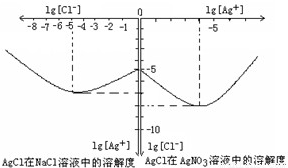
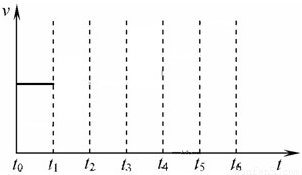
查看答案和解析>>
科目: 来源:2011年浙江省杭州市萧山区高考化学模拟试卷(十九)(解析版) 题型:填空题


查看答案和解析>>
科目: 来源:2011年浙江省杭州市萧山区高考化学模拟试卷(十九)(解析版) 题型:填空题


查看答案和解析>>
科目: 来源:2011年山东省枣庄一中高考化学模拟试卷(二)(解析版) 题型:选择题
查看答案和解析>>
科目: 来源:2011年山东省枣庄一中高考化学模拟试卷(二)(解析版) 题型:选择题
查看答案和解析>>
科目: 来源:2011年山东省枣庄一中高考化学模拟试卷(二)(解析版) 题型:选择题
查看答案和解析>>
科目: 来源:2011年山东省枣庄一中高考化学模拟试卷(二)(解析版) 题型:选择题
 Si+2CO↑的反应中,每当有1mol气体生成,就有4N4个电子转移
Si+2CO↑的反应中,每当有1mol气体生成,就有4N4个电子转移 )>0.4mol?L-1
)>0.4mol?L-1查看答案和解析>>
科目: 来源:2011年山东省枣庄一中高考化学模拟试卷(二)(解析版) 题型:选择题

查看答案和解析>>
科目: 来源:2011年山东省枣庄一中高考化学模拟试卷(二)(解析版) 题型:选择题
 (aq)+H2O(l)△H=-57.3kJ?mol-1
(aq)+H2O(l)△H=-57.3kJ?mol-1 +Ba2++2OH-=BaSO4↓+2H2O
+Ba2++2OH-=BaSO4↓+2H2O查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com