
科目: 来源:2012-2013学年广东省清远市高三上学期期末检测理综化学试卷(解析版) 题型:实验题
不久前,一则“食用撒了鱼浮灵的鱼虾可能致癌”的微博在网上热传。“鱼浮灵”的化学成分实为过碳酸钠,使用不当会让鱼损伤,过碳酸钠本身无毒无害,对人体不会有危害。过碳酸钠,俗称固体双氧水,化学式为2Na2CO3·3H2O2,是一种无机盐,是白色颗粒状粉末,可以分解为碳酸钠和过氧化氢。某探究小组制备过碳酸钠并测定样品中H2O2的含量,其制备流程和装置示意图如下:

已知:50 °C时 2Na2CO3·3H2O2 (s) 开始分解
主反应 2Na2CO3
(aq) + 3H2O2 (aq) 2Na2CO3·3H2O2
(s) ΔH < 0
2Na2CO3·3H2O2
(s) ΔH < 0
副反应 2H2O2 = 2H2O + O2↑
滴定反应 6KMnO4 + 5(2Na2CO3·3H2O2) +19H2SO4 = 3K2SO4 + 6MnSO4+10Na2SO4 + 10CO2 ↑ + 15O2↑ + 34H2O

根据以上信息回答下列问题:
(1)推测图中支管的作用可能是 。
(2)步骤①的关键是控制温度,结合装置图归纳其措施有 、
和 。
(3)在滤液X中加入适量NaCl固体或无水乙醇均可析出过碳酸钠,原因是 。
(4)步骤③中选用无水乙醇洗涤产品的目的是 。
(5)测定样品中H2O2的质量分数的方法是:准确称取0.2000g过碳酸钠样品于250 mL 锥形瓶中,加50 mL 蒸馏水溶解,再加50 mL 2.000 mol·L-1 H2SO4 (H2SO4过量),用0.002000mol·L-1 KMnO4 标准溶液滴定至终点时消耗30.00 mL。
①滴定前,滴定管需用KMnO4标准溶液润洗2~3次,润洗的操作方法是:关闭酸式滴定管活塞,向滴定管中注入少量KMnO4标准 。
②上述样品中H2O2的质量分数计算表达式为 (只列出算式,不作任何运算!H2O2的式量为34.00)。
查看答案和解析>>
科目: 来源:2012-2013学年广东省清远市高三上学期期末检测理综化学试卷(解析版) 题型:实验题
阿司匹林是一种历史悠久的解热镇痛药,学名为乙酰水杨酸,结构简式为 。某探究小组在实验室探究阿司匹林的合成,主要原料是水杨酸(邻羟基苯甲酸)与醋酸酐[(CH3CO)2O],制备基本实验流程如下:
。某探究小组在实验室探究阿司匹林的合成,主要原料是水杨酸(邻羟基苯甲酸)与醋酸酐[(CH3CO)2O],制备基本实验流程如下:
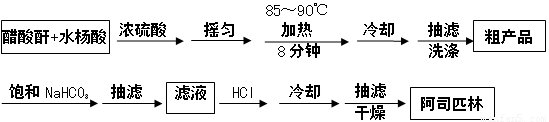
已知:1、乙酰水杨酸是白色晶体,易溶于乙醇、乙醚,在128~135℃易分解。
2、主要试剂和产品的其它物理常数
|
名称 |
相对分子质量 |
熔点或沸点(℃) |
水溶性 |
|
水杨酸 |
132 |
158(熔点) |
微溶 |
|
醋酸酐 |
102 |
139.4(沸点) |
与水反应 |
|
乙酰水杨酸 |
180 |
135(熔点) |
微溶 |
请根据以上信息回答下列问题:
(1)写出水杨酸与醋酸酐制备阿司匹林的化学方程式 。
(2)制备阿司匹林主反应时,仪器必须干燥的原因是 。
(3)合成阿司匹林主反应时,最合适的加热方法是 ,除酒精灯外,该加热装置还需要的玻璃仪器有 。
(4)提纯粗产品时加入饱和NaHCO3溶液至没有CO2产生为止,再抽滤(即减压过滤),结合提纯流程回答加饱和NaHCO3溶液的目的是 。
(5)最终所得产品可能仍含有少量水杨酸,检验含有水杨酸的操作和现象是
。
查看答案和解析>>
科目: 来源:2012-2013学年广东省湛江市普通高考测试(二)理综化学试卷(解析版) 题型:选择题
化学与生活息息相关,下列说法正确的是
A.稀的双氧水可用于清洗伤口,以达到杀菌、消毒的目的
B.动物体内葡萄糖被氧化成CO2是热能转变成化学能的过程
C.冰醋酸可用于医学消毒
D.蚕丝、羊毛和淀粉分别属于纤维素、蛋白质和多糖
查看答案和解析>>
科目: 来源:2012-2013学年广东省湛江市普通高考测试(二)理综化学试卷(解析版) 题型:选择题
在水溶液中能大量共存的一组是
A.Ba2+、Na+、SO42-、Cl- B.MnO4-、SO32-、H+、K+
C.AlO2-、Mg2+、K+、HCO3- D.K+、Na+、NO3-、SO42-
查看答案和解析>>
科目: 来源:2012-2013学年广东省湛江市普通高考测试(二)理综化学试卷(解析版) 题型:选择题
设NA 为阿伏加德罗常数的数值,下列说法正确的是
A.1mol NO2与足量H2O反应,转移电子数为2NA
B.22.4L2H2O中所含的中子数为10NA
C.100mL 1mol•L-1AlCl3溶液中含的阳离子数大于0.1NA
D.78g的Na2O2含阴离子2NA
查看答案和解析>>
科目: 来源:2012-2013学年广东省湛江市普通高考测试(二)理综化学试卷(解析版) 题型:选择题
下列物质的应用不涉及氧化还原反应的是
A.用稀硝酸洗去附在试管内壁的银镜
B.用热的纯碱溶液清洗油污
C.用新制的氢氧化铜悬浊液与病人的尿液混和加热,来检验病人是否患糖尿病
D.在铁质镀件上镀铜
查看答案和解析>>
科目: 来源:2012-2013学年广东省湛江市普通高考测试(二)理综化学试卷(解析版) 题型:选择题
如下实验操作正确且能达到实验目的的是
A.用铁粉与稀硝酸反应,制取少量氢气,用排水法收集
B.在蒸发皿中给十水碳酸钠加热脱水
C.用酸式滴定管量取6.55mL的KMnO4溶液
D.用分液漏斗分离溴乙烷与氢氧化钠溶液发生反应后的生成物
查看答案和解析>>
科目: 来源:2012-2013学年广东省湛江市普通高考测试(二)理综化学试卷(解析版) 题型:选择题
下列陈述I、II正确并且有因果关系的是
选项 陈述I 陈述II
A H2O2、SO2都能使酸性高锰酸钾褪色 前者表现出还原性后者表现出漂白性
B 纯银器表面在空气中渐渐变暗 发生了化学腐蚀
C SiO2能与氢氟酸及碱反应 SiO2是两性氧化物
D BaSO4饱和溶液中加入饱和Na2CO3溶液有白色沉淀 说明Ksp(BaSO4)大于Ksp(BaCO3)
查看答案和解析>>
科目: 来源:2012-2013学年广东省湛江市普通高考测试(二)理综化学试卷(解析版) 题型:选择题
元素周期表和元素周期律可以指导人们进行规律性的推测和判断。下列说法不合理的是
A.若X+和Y2-的核外电子层结构相同,则原子序数:X > Y
B.由水溶液的酸性:HCl>H2S,可推断出元素的非金属性:Cl>S
C.硅、锗都位于金属与非金属的交界处,都可以做半导体材料
D.Cs和Ba分别位于第六周期IA和IIA族,碱性:CsOH﹤Ba(OH)2
查看答案和解析>>
科目: 来源:2012-2013学年广东省湛江市普通高考测试(二)理综化学试卷(解析版) 题型:选择题
在25℃时,将0.2molCH3COONa晶体和0.1molHCl气体同时溶解于同一烧杯的水中,制得1L溶液,若此溶液中c(CH3COO-)>c(Cl-),则下列判断不正确的是
A.该溶液的pH大于7
B.c(CH3COOH)+c(CH3COO-)=0.20mol·L-1
C.c(CH3COOH)<c(CH3COO-)
D.c(CH3COO-)+c(OH-)=0.10mol·L-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com