
科目: 来源:2012-2013学年四川省德阳市“一诊”考试化学试卷(解析版) 题型:填空题
氮是地球上含量丰富的原子元素,氮及其化合物在工农业生产、生活中有着重要作用。
(1)25℃时,0.1mol/LNH4NO3溶液中水的电离程度 (填“大于”、“等于”或“小于”) 0.1mol/L NaOH溶液中水的电离程度。
(2)若将0.1mol/L NaOH溶液和0.2mol/LNH4NO3溶液等体积混合,混合溶液中2c(NH4+)>c(NO3-),所得溶液中离子浓度由大到小的顺序是 。
(3)发射火箭时肼(N2H4)为燃料,二氧化氮作氧化剂,两者反应生成氮气和气态水。经测定16g气体在上述反应中放出284kJ的热量。则该反应的热化学方程式是 。
(4)下图是1mol NO2和1mol CO反应生成CO2和NO过程中能量变化示意图。
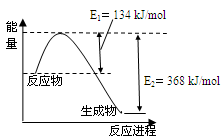
已知:N2(g)+O2(g)=2NO(g) △H=+180kJ/mol
2NO (g)+O2(g)=2NO2(g) △H=-112.3kJ/mol
则反应:2NO(g)+2CO(g) N2(g)+2CO2(g)的△H是
。
N2(g)+2CO2(g)的△H是
。
查看答案和解析>>
科目: 来源:2012-2013学年四川省德阳市“一诊”考试化学试卷(解析版) 题型:填空题
一定温度时,在容积一定的密闭容器中,反应A(?)+B(g)  C(g)+D(g)达到平衡后,升高温度容器内气体的密度增大。请回答下列问题:
C(g)+D(g)达到平衡后,升高温度容器内气体的密度增大。请回答下列问题:
(1)正反应是 (填“放热”或“吸热”)反应;该反应的化学平衡常数的表达式是 。
(2)能判断该反应一定达到平衡状态的依据是 。(填写字母编号)
A.体积分数组成C%=D%
B.单位时间内生成n molA的同时生成n molC
C.温度和体积一定时,某一生成物浓度不再变化
D.温度和体积一定时,容器内压强不再变化
(3)该反应的正反应速率随时间变化的关系如图所示。t2时改了某种条件,改变的条件是 。(填写字母编号)

A.升温 B.加压 C.催化剂 D.增加A的量
(4)升高温度到T℃时,在一密闭容器中充入2mol A和3mol B,发生上述反应。平衡后测得K=1。然后在温度不变的情况下,扩大容器容积至原来的10倍,结果A的百分含量始终未改变,则此时B的转化率是 。
查看答案和解析>>
科目: 来源:2012-2013学年四川省德阳市“一诊”考试化学试卷(解析版) 题型:实验题
未来生活中金属钛的运用越来越广泛,如可在催化剂TiO2作用下,先用NaClO将CN-(毒性很强)氧化成CNO-,再在酸性条件下继续被NaClO氧化成N2和CO2。环保工作人员在密闭系统中用下图装置进行实验,以证明处理方法的有效性,并通过测定二氧化碳的量确定CN-被处理的百分率。

将浓缩后含CN-离子的污水与过量NaClO溶液的混合液共200mL(其中CN-的浓度为0.05mol·L-1)倒入甲中,塞上橡皮塞,一段时间后,打开橡皮塞和活塞,使溶液全部放入乙中,关闭活塞。回答下列问题:
(1)乙中反应的离子方程式为__________________________________。
(2)乙中生成的气体除N2和CO2外,还有HCl及副产物Cl2等,上述实验是通过测定二氧化碳的量来确定对CN-的处理效果。则丙中加入的除杂试剂是______(填字母)。
a.饱和食盐水 b.饱和NaHCO3溶液 c.浓NaOH溶液 d.浓硫酸
(3)丁在实验中的作用是____________________________ ,装有碱石灰的干燥管的作用是____________________________。
(4)戊中盛有含Ca(OH)20.02mol的石灰水,若实验中戊中共生成0.82 g沉淀,则该实验中测得CN-被处理的百分率等于________,请说明该测得值与实际处理的百分率相比偏高还是偏低_________?简要说明可能的原因________________________________________________________。
(5)请提出一个能提高准确度的建议(要有可操作性,不宜使操作变得过于复杂)
_________________________________________________________________________
查看答案和解析>>
科目: 来源:2012-2013学年四川省德阳市“一诊”考试化学试卷(解析版) 题型:实验题
重铬酸钠(Na2Cr2O7•2H2O)俗称红矾钠,在工业方面有广泛用途.我国目前主要是以铬铁矿(主要成份为FeO•Cr2O3,还含有Al2O3、MgO、SiO2等杂质)为主要原料进行生产,其主要工艺流程如下:
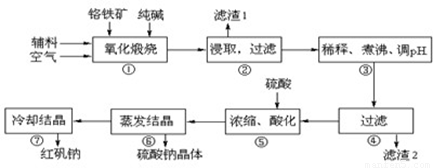
中涉及的主要反应有:
主反应:4FeO•Cr2O3+8Na2CO3+7O2  8Na2CrO4+2Fe2O3+8CO2
8Na2CrO4+2Fe2O3+8CO2
副反应: SiO2+Na2CO3 Na2SiO3+CO2↑
Al2O3+Na2CO3
Na2SiO3+CO2↑
Al2O3+Na2CO3 2NaAlO2+CO2↑
2NaAlO2+CO2↑
部分阳离子以氢氧化物形式完全沉淀时溶液的pH:
|
沉淀物 |
Al(OH)3 |
Fe(OH)3 |
Mg(OH)2 |
Cr(OH)3 |
|
完全沉淀时溶液pH |
4.7 |
3.7 |
11.2 |
5.6 |
试回答下列问题:
(1)“①”中反应是在回转窑中进行,反应时需不断搅拌,其作用是 ;
(2)“③”中调节pH至4.7,目的是 ;
(3)“⑤”中加硫酸酸化的目的是使CrO42-转化为Cr2O72-,请写出该平衡转化的离子方程式: ;
(4)称取重铬酸钠试样2.5000g配成250mL溶液,取出25.00mL于碘量瓶中,加入10mL 2mol•L-1H2SO4和足量碘化钠(铬的还原产物为Cr3+),放于暗处5min,然后加入100mL水,加入3mL淀粉指示剂,用0.1200mol•L-1Na2S2O3标准溶液滴定(I2+2S2O32-=2I-+S4O62-)
①判断达到滴定终点的依据是: 。
②若实验中共用去Na2S2O3标准溶液40.00ml,所得产品的中重铬酸钠的纯度 (设整个过程中其它杂质不参与反应) 。
查看答案和解析>>
科目: 来源:2012-2013学年四川省成都市高三第二次诊断性考试理综化学试卷(解析版) 题型:选择题
下列说法不正确的是
A.天然油脂含酯基属于酯类物质
B.麦芽糖和蔗糖的水解产物相同
C.酚醛树脂是酚与醛的缩聚产物
D.石油裂化和裂解都可制得烯烃
查看答案和解析>>
科目: 来源:2012-2013学年四川省成都市高三第二次诊断性考试理综化学试卷(解析版) 题型:选择题
若NA为阿伏加德罗常数的值,下列叙述正确的是
A.1 mol-OH中含有的质子数为9NA
B.lmol2,3—丁二醇分子中含C一C数目为4NA
C.1 L 1 mol.L-1 FeCl3 溶液中含有 Fe3 + 数为 NA
D.71 g氯气参与反应,电子转移数目一定为2NA
查看答案和解析>>
科目: 来源:2012-2013学年四川省成都市高三第二次诊断性考试理综化学试卷(解析版) 题型:选择题
已知A、B、C、D为短周期主族元素,其相对位置关系如图。C与B可形成离子化合 物C3B2。下列分析正确的是

A.电负性:C>A
B.离子氧化性:C>D
C.氢化物稳定性:A> B
D.原子半径:r(C)> r(B)
查看答案和解析>>
科目: 来源:2012-2013学年四川省成都市高三第二次诊断性考试理综化学试卷(解析版) 题型:选择题
已知HF酸性强于CH3COOH,常温下有下列三种溶液。有关叙述不正确的是

A.②、③混合后:C(H+)=C(F-)+C(CH3COO-)+ c(OH-)
B.①、②等体积混合后:c(CH3COO-)>c(Na+)>C(H+)>c(OH-)
C.中和相同体积的②、③,需消耗相同体积的①
D.向②加入NaF固体,CH3C00H电离平衡正向移动
查看答案和解析>>
科目: 来源:2012-2013学年四川省成都市高三第二次诊断性考试理综化学试卷(解析版) 题型:选择题
已知250C时某溶液中含有大量Na+、H+、Fe3+、HC03-、OH-、I-中的几种,并且水 电离出的c(H+) = 1×10-13 mol/L。当向该溶液中缓慢通入一定量的Cl2后,溶液由无色 变为黄色。下列有关分析正确的是
A.溶液的PH=1或13
B.溶液中一定没有Fe3+,Na+
c.溶液中阴离子有I-,不能确定HCO3-
D.当Cl2过量,所得溶液只含有两种盐
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com