
科目: 来源:2012-2013学年湖北省高三10月月考化学试卷(解析版) 题型:实验题
(5分)利用下列实验仪器:①铁架台(含铁圈、各种铁夹);②锥形瓶;③滴定管(酸式与碱式);④烧杯(若干个);⑤玻璃棒;⑥天平(含砝码);⑦滤纸;⑧量筒;⑨漏斗
试剂:Na2CO3固体;标准NaOH溶液;未知浓度盐酸;Na2CO3溶液;蒸馏水。
进行下列实验或操作:
(1)做酸碱中和滴定时,还缺少的试剂是:
(2)配制250mL 0.1mol•L-1某溶液时,还缺少的仪器是:
(3)过滤时,应选用上述仪器中的 (填编号)
查看答案和解析>>
科目: 来源:2012-2013学年湖北省高三10月月考化学试卷(解析版) 题型:实验题
(12分)为探究亚硫酸钠的热稳定性,某研究性学习小组将无水亚硫酸钠隔绝空气加热,并利用受热后的固体试样和下图所示的实验装置进行实验。请回答下列有关问题:
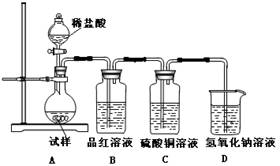
(1)查阅资料:无水亚硫酸钠隔绝空气受热到600℃才开始分解,且分解产物只有硫化钠和另外一种固体。如果加热温度低于600℃,向所得冷却后固体试样中缓缓滴加稀盐酸至足量,在滴加稀盐酸的整个过程中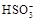 的物质的量浓度变化趋势为
;
的物质的量浓度变化趋势为
;
(2)如果加热温度为700℃,向所得冷却后固体试样中缓缓滴加稀盐酸至足量,观察到烧瓶中出现淡黄色沉淀,且有大量气泡产生,则反应生成淡黄色沉淀的离子方程式为 ;此时在B、C两装置中可能观察到得现象为 。
(3)在(2)中滴加足量盐酸后,烧瓶内除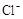 外,还存在另一种浓度较大的阴离子(X)。为检验该阴离子(X),先取固体试样溶于水配成溶液,为了加速固体试样的溶解,可采取措施。以下是检验阴离子(X)的两种实验方案,你认为合理的方案是 (填“甲”或“乙”),
外,还存在另一种浓度较大的阴离子(X)。为检验该阴离子(X),先取固体试样溶于水配成溶液,为了加速固体试样的溶解,可采取措施。以下是检验阴离子(X)的两种实验方案,你认为合理的方案是 (填“甲”或“乙”),
请说明另一方案不合理的原因 。方案甲:取少量试样溶液于试管中,先加稀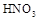 ,再加
,再加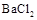 溶液,有白色沉淀生成,证明该离子存在。
溶液,有白色沉淀生成,证明该离子存在。
方案乙:取少量试样溶液于试管中,先加稀HCl,再加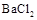 溶液,有白色沉淀生成,证明该离子存在。
溶液,有白色沉淀生成,证明该离子存在。
(4)写出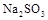 固体加热到600℃以上分解的化学方程式
。
固体加热到600℃以上分解的化学方程式
。
查看答案和解析>>
科目: 来源:2012-2013学年湖北省高三10月月考化学试卷(解析版) 题型:填空题
(8分)磷是生物体中不可缺少的元素之一,在自然界中磷总是以磷酸盐的形式出现的,例如磷酸钙矿Ca3(PO4)2、磷灰石Ca5F(PO4)3等。
(1)磷的某种核素中,中子数比质子数多1,则表示该核素的原子符号为____________。
(2)磷酸钙与焦炭、石英砂混合,在电炉中加热到1500℃生成白磷,反应为:
2Ca3(PO4)2+6SiO2 = 6CaSiO3+P4O10 10C+P4O10 = P4↑+10CO↑
上述反应中的各种物质,属于酸性氧化物的有 。
(3)白磷有剧毒,不慎沾到皮肤上,可用CuSO4溶液冲洗解毒。白磷可与热的CuSO4溶液反应生成磷化亚铜,与冷溶液则析出铜,反应方程式分别(均未配平)为:
① P4+CuSO4+H2O→Cu3P+H3PO4+H2SO4
② P4+CuSO4+H2O→Cu+H3PO4+H2SO4
反应①中,氧化剂为 ,若上述两反应中被氧化的P4的物质的量相等,则消耗的CuSO4的物质的量之比为 。
查看答案和解析>>
科目: 来源:2012-2013学年湖北省高三10月月考化学试卷(解析版) 题型:填空题
(9分)化学实验室通常用粗锌和稀硫酸反应制氢气,因此在制氢废液中含有大量的硫酸锌。同时,由于粗锌中还含有铁等杂质,使得溶液中混有一定量的硫酸亚铁,为了充分利用制氢废液,常用其制备皓矾(ZnSO4·7H2O)。某校化学兴趣小组的同学以制氢气的废液为原料来制取皓矾。制备皓矾的实验流程如下图所示。
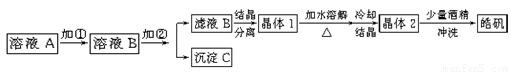
已知:开始生成氢氧化物沉淀到沉淀完全的pH范围分别为:Fe(OH)3:2.7-3.7 Fe(OH)2:7.6-9.6 Zn(OH)2:5.7-8.0试回答下列问题:?
(1)加入的试剂①,供选择使用的有:氨水、NaClO溶液、20%的H2O2、浓硫酸、浓硝酸等,最好选用 ,其理由是 ;
(2)加入的试剂②,供选择使用的有:a、Zn粉,b、ZnO,c、Zn(OH)2,d、ZnCO3,e、ZnSO4等,可选用 ;
(3)从晶体1→晶体2,该过程的名称是 ;
(4)在得到皓矾时,向晶体中加入少量酒精洗涤而不用水的原因是 。
查看答案和解析>>
科目: 来源:2012-2013学年湖北省高三10月月考化学试卷(解析版) 题型:填空题
(9分)目前世界上比较先进的电解制碱技术是离子交换膜法。
(1)电解前,如果粗盐中SO42ˉ含量较高,必须添加试剂除去SO42ˉ,则按添加试剂顺序,依次发生反应的离子方程式为 。
(2)补齐下列电解饱和食盐水制烧碱的离子方程式:
______________________
 __________________________________
__________________________________
(反应物) (阴极产物) (阳极产物)
(3)在电解制得的NaOH中往往还含有一定量的NaCl,因此必需进行脱盐工序,脱盐工序中利用NaOH和NaCl在溶解度上的差异,通过 、冷却、 (填写操作名称)除去NaCl。
(4)已知NaCl在60℃的溶解度为37.1 g,现电解60℃精制饱和食盐水1371 g 。经分析,电解后溶液密度为1.37 g·cm-3,其中含有20gNaCl,则电解后NaOH的物质的量浓度为__________mo1·L-1(保留小数点后1位)。
查看答案和解析>>
科目: 来源:2012-2013学年湖北省高三10月月考化学试卷(解析版) 题型:计算题
(9分)10 mL含有a mol HCl的稀盐酸和10 mL含有b molNa2CO3的稀溶液,按下图方式分别缓慢向对方溶液中滴加,并不断摇动试管,试分析下表并完成各题:(题中气体体积均在标准状况下测定,且不考虑气体在水中的溶解)
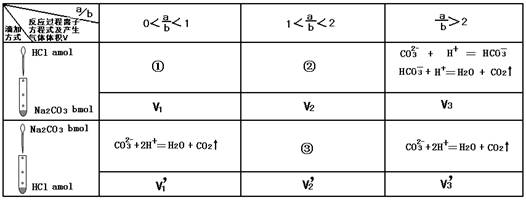
(1)表中对应过程的离子反应方程式:
① ;③ 。
(2)上述所测六种情况下气体体积V1、V1'、V2、V2'、V3、V3'中为0的有 。
(3)V3与V3'的大小关系为V3 V3'(用“<” 、“>” 或“=”填空)
(4)若a=0.01,b=0.008,则V2= mL、V2'= mL。
查看答案和解析>>
科目: 来源:2012-2013学年湖南望城一中、长沙县实验中学高三10月联考化学试卷(解析版) 题型:选择题
实验室里有4个药品橱,已经存放以下物品:
|
药品橱 |
甲橱 |
乙橱 |
丙橱 |
丁橱 |
|
药品 |
盐酸、硫酸 |
氢氧化钠、氢氧化钙 |
红磷、硫 |
铜、锌 |
实验室新购进一些石墨,应该将这些石墨放在 ( )
A.甲橱 B.乙橱 C.丙橱 D.丁橱
查看答案和解析>>
科目: 来源:2012-2013学年湖南望城一中、长沙县实验中学高三10月联考化学试卷(解析版) 题型:选择题
下列叙述正确的是 ( )
A.胶体区别于其他分散系的根本原因是胶体有丁达尔现象
B.分散系中分散质粒子直径由小到大的正确顺序是:溶液<胶体<浊液
C.光束通过胶体和浊液时都可以看到一条光亮的通路,而溶液不能
D.胶体的分散质可以通过过滤从分散剂中分离出来
查看答案和解析>>
科目: 来源:2012-2013学年湖南望城一中、长沙县实验中学高三10月联考化学试卷(解析版) 题型:选择题
下列说法正确的是 ( )
A、可逆反应的特征是正反应速率和逆反应速率相等
B、在其他条件不变时,使用催化剂只能改变反应速率,而不能改变化学平衡状态
C、在其他条件不变时,升高温度可以使平衡向放热反应方向移动
D、在其他条件不变时,增大压强一定会破坏气体反应的平衡状态
查看答案和解析>>
科目: 来源:2012-2013学年湖南望城一中、长沙县实验中学高三10月联考化学试卷(解析版) 题型:选择题
设NA为阿伏加德罗常数的数值。下列说法错误的是( )
A. 20g重水(D2O)中含有10NA个电子
B. 标准状况下,22.4L一氯甲烷的分子数约为NA
C. 4.6 g Na在氧气中完全反应生成Na2O和Na2O2,转移电子数为0.2NA
D. 25℃时,1L pH = 14的Ba(OH)2溶液中,Ba2+ 数为NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com