
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
 某新型洗涤剂是由一白色粉末和H2O2混合而成(该白色粉末不和H2O2发生反应),但该白色粉末的试剂瓶标签破损了(如图).请完成对该白色粉末成分的探究:
某新型洗涤剂是由一白色粉末和H2O2混合而成(该白色粉末不和H2O2发生反应),但该白色粉末的试剂瓶标签破损了(如图).请完成对该白色粉末成分的探究:| 编号 | 物质的化学式 | 检验需要的试剂 | 操作、现象和结论 |
| 1 | Na2CO3 | ______ | ______ |
| 2 | ______ | ______ | ______ |
| 3 | ______ | ______ | ______ |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题

查看答案和解析>>
科目: 来源: 题型:单选题
查看答案和解析>>
科目: 来源: 题型:解答题

查看答案和解析>>
科目: 来源: 题型:单选题
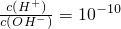 的溶液中:K+、Na+、CO32-、[Al(OH)4]-
的溶液中:K+、Na+、CO32-、[Al(OH)4]-查看答案和解析>>
科目: 来源: 题型:单选题
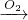 乙
乙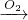 丙
丙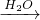 丁”实现转化的组合是
丁”实现转化的组合是| ① | ② | ③ | ④ | |
| 甲 | Na | Cu | S | NH3 |
| 丁 | NaOH | Cu(OH)2 | H2SO4 | HNO3 |
查看答案和解析>>
科目: 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com