
科目: 来源:2014届四川省高二10月阶段性考试化学试卷(解析版) 题型:选择题
最近,中国科大的科学家们将C60分子组装在一单层分子膜表面,在-268℃时冻结分子的热振荡,并利用扫描隧道显微镜首次“拍摄”到能清楚分辨碳原子间单、双键的分子图像。下列化合物分子中一定既含单键又含双键的是( )
A.CO2 B.CH4O C.COCl2 D.H2O2
查看答案和解析>>
科目: 来源:2014届四川省高二10月阶段性考试化学试卷(解析版) 题型:选择题
科学家最近研制出可望成为高效火箭推进剂的 N (NO2)3,如下图:
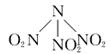 。已知该分子中 N-N-N 键角都是 108.1°,下列有关 N(NO2)3
的说法正确的是(
)
。已知该分子中 N-N-N 键角都是 108.1°,下列有关 N(NO2)3
的说法正确的是(
)
A.分子中 N、O 间形成的共价键是非极性键 B.分子中四个氮原子共平面
C.该物质既有氧化性又有还原性 D.15.2g 该物质含有 6.02×1022个原子
查看答案和解析>>
科目: 来源:2014届四川省高二10月阶段性考试化学试卷(解析版) 题型:选择题
在乙烯分子中有5个σ键和1个π键,下列说法正确的是( )
A.乙烯与氢气发生加成反应,断裂的是σ键
B.sp2杂化轨道形成π键,未杂化的2p轨道形成σ键
C.C—H之间是sp2杂化轨道形成σ键,C—C之间是未杂化的2p轨道形成π键
D.乙烯分子中所有原子不共平面
查看答案和解析>>
科目: 来源:2014届四川省高二10月阶段性考试化学试卷(解析版) 题型:选择题
下列中心原子的杂化轨道类型和分子几何构型不正确的是( )
A.PCl3中P原子sp3杂化,为三角锥形 B.BCl3中B原子sp2杂化,为平面三角形
C.CS2中C原子sp杂化,为直线形 D.H2S分子中,S为sp杂化,为直线形
查看答案和解析>>
科目: 来源:2014届四川省高二10月阶段性考试化学试卷(解析版) 题型:选择题
有A、B、C三种主族元素,已知A元素原子的价电子构型为nsn,B元素原子的M层上有两个未成对电子,C元素原子L层的p轨道上有一对成对电子,由这三种元素组成的化合物的化学式不可能是( )
A.A3BC4 B.A2BC4 C.A2BC3 D.ABC4
查看答案和解析>>
科目: 来源:2014届四川省高二10月阶段性考试化学试卷(解析版) 题型:填空题
(15分)(1)某元素的基态原子最外层电子排布为3s23p2,它的次外层上电子云形状有______种,原子中所有电子占有______个轨道,核外共有_________个不同运动状态的电子。
(2)E原子核外占有9个轨道,且具有1个未成对电子,E离子结构示意图是_____________。
(3)F、G都是短周期元素,F2-与G3+的电子层结构相同,则G元素的原子序数是______,F2-的电子排布式是_______________________________。
(4)M能层上有____个能级,有____个轨道,作为内层最多可容纳______个电子,作为最外层时,最多可含有______个未成对电子。
(5)在元素周期表中,最外层只有1个未成对电子的主族元素原子处于________________族;最外层有2个未成对电子的主族元素原子处于__________________族。
查看答案和解析>>
科目: 来源:2014届四川省高二10月阶段性考试化学试卷(解析版) 题型:填空题
(7分)(1)中国古代四大发明之一——黑火药,它的爆炸反应为:
2KNO3+ 3C+S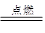 A+N2↑+3CO2↑(已配平)
A+N2↑+3CO2↑(已配平)
①除 S 外,上列元素的电负性从大到小依次为_________________________;
②生成物中,A 的电子式为__________________,含极性共价键的分子的中心原子轨道杂化类型____________;
③已知CN-与N2结构相似,推算HCN分子中σ键与π键数目之比为____________。
(2)原子序数小于36的元素Q和T,在周期表中既处于同一周期又位于同一族,且原子序数T比Q多2。T的基态原子外围电子(价电子)排布式为_______________________________,Q2+的未成对电子数是________。
查看答案和解析>>
科目: 来源:2014届四川省高二10月阶段性考试化学试卷(解析版) 题型:填空题
(5分)生物质能是一种洁净、可再生能源。生物质气(主要成分为 CO、CO2、H2 等)与 H2 混合,催化合成甲醇是生物质能利用的方法之一。
(1)上述反应的催化剂含有 Cu、Zn、Al 等元素。写出基态 Cu2+离子的核外电子排布式_______________________________________;
(2)根据等电子原理,写出 CO 分子的结构式______________________;
(3)甲醇催化氧化可得到甲醛,甲醛与新制 Cu(OH)2 的碱性溶液反应生成 Cu2O 沉淀。
①甲醛分子中碳原子轨道的杂化类型为_____________________;
②甲醛分子的空间构型是__________________;
③ 1 mol 甲醛分子中 σ 键的数目为__________________。
查看答案和解析>>
科目: 来源:2014届四川省高二10月阶段性考试化学试卷(解析版) 题型:填空题
(9分)(1)CH3+、—CH3、CH3— 都是重要的有机反应中间体,有关它们的说法正确的是_________________
A.它们均由甲烷去掉一个氢原子所得
B.它们互为等电子体,碳原子均采取sp2杂化
C.CH3—与NH3、H3O+互为等电子体,几何构型均为三角锥形
D.CH3+中的碳原子采取sp2杂化,所有原子均共面
E.两个—CH3或一个CH3+和一个CH3—结合均可得到CH3CH3
(2)锌是一种重要的金属,锌及其化合物有着广泛的应用。
①指出锌在周期表中的位置:第________周期,第________族,属于________区。
②葡萄糖酸锌[CH2OH(CHOH)4COO]2Zn是目前市场上流行的补锌剂。葡萄糖分子中碳原子杂化方式有___________;写出基态Zn原子的电子排布式_____________________________。
查看答案和解析>>
科目: 来源:2014届四川省高二10月阶段性考试化学试卷(解析版) 题型:填空题
(9分)下表是元素周期表前五周期的一部分,X、Y、Z、R、W、J是6种元素的代号。
|
X |
Y |
Z |
|
|
|
R |
|
|
|
|
|
W |
|
|
|
|
|
J |
请回答下列问题(除特别说明外,凡涉及用元素回答的问题均用具体元素符号表示):
(1) 在化合物YZ2中Y的化合价为________;Y2-与Na+的半径大小为_______________;
(2) R原子的电子轨道排布图为___________________________________;
(3)在X、Y、Z三种元素中,电负性由大到小的顺序是______________________;X与Y的第一电离能:X___Y(填“<”、“>”或“=”),其理由是__________________________________。
(4)有一种酸HX3的酸性与醋酸相近,HX3溶液与NaOH溶液反应的离子方程式为:___________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com