
科目: 来源:2012-2013学年浙江省温州八校高三9月期初联考化学试卷(解析版) 题型:选择题
a mol FeS与b mol FeO投入到v L、c mol•L-1的硝酸溶液中充分反应,产生NO气体,所得澄清溶液的成分可看作是Fe(NO3)3、H2SO4的混合液,则反应中未被还原的硝酸可能为
①(a+b)×63g ②(a+b)×189g ③(a+b)mol ④[cV-(9a+b)/3 ]mol
A.①④ B.②③ C.①③ D.②④
查看答案和解析>>
科目: 来源:2012-2013学年浙江省温州八校高三9月期初联考化学试卷(解析版) 题型:填空题
(10分)NaNO2俗称“工业盐”,其外观与食盐相似,易误食而中毒,可通过化学实验加以鉴别。如向NaNO2的酸性溶液中加入KI固体,析出的碘可以使淀粉溶液变蓝色,据此检验NO2—。
请回答下列问题:
(1)写出上述反应的离子方程式 。
(2)日常生活中若需鉴别工业盐和食盐,现有碘化钾淀粉试纸,则还需选用的生活中常见物质的名称为 。[来源:Zxxk.Com]
(3)某工厂废切削液中含有2%—5%的NaNO2,直接排放会造成水污染,但加入下列物质中的某一种就能使NaNO2转化为不引起污染的N2,该物质是 ,
a.NaCl b.H2O2 c.NH4Cl d.浓H2SO4
所发生反应的离子方程式为: 。
查看答案和解析>>
科目: 来源:2012-2013学年浙江省温州八校高三9月期初联考化学试卷(解析版) 题型:填空题
(14分)短周期的五种元素A、B、C、D、E,原子序数依次增大。A、B、C三种元素电子层数之和是5。A、B两元素原子最外层电子数之和等于C元素原子最外层电子数;B元素原子最外电子层上的电子数是它的电子层数的2倍, A与D可以形成原子个数比分别为1:1和2:1的两种液态化合物;E单质用于净化水质。
请回答:
(1)写出D在元素周期表中的位置 ,E的原子结构示意图是__ ___ 。
下列可以验证C与D两元素原子得电子能力强弱的实验事实是___ _______(填写编号);
A.比较这两种元素的气态氢化物的沸点
B.比较只有这两种元素所形成的化合物中的化合价
C.比较这两种元素的气态氢化物的稳定性
D.比较这两种元素的单质与氢气化合的难易
(2)由A、B两种元素组成的最简单的化合物,写出其电子式 。
(3)均由A、B、C、D四种元素组成的甲、乙两种化合物,都既可以与盐酸反应又可以与NaOH溶液反应,甲为无机盐,其化学式为 ,乙为天然高分子化合物的水解产物,且是同类物质中相对分子质量最小的,其结构简式为 。
(4)胶态磁流体在医学上有重要的用途,而纳米级Fe3O4是磁流体中的重要粒子,其制备过程可简单表示如下:
①将化合物CA3通入等物质的量的FeSO4、Fe2(SO4)3的混合溶液中,生成两种碱,写出该反应过程的总的离子方程式____ ____ ____ ____ ____ ____ 。
②上述反应生成的两种碱继续作用,得到Fe3O4
(5)已知下表数据:
|
物质 |
Fe(OH)2 |
Fe(OH)3 |
|
Ksp/25℃ |
2.0×10-16 |
4.0×10-36 |
若使混合液中FeSO4、Fe2(SO4)3的浓度均为2.0mol·L-1,则混合液中c(OH-)不得大于 mol·L-1。
查看答案和解析>>
科目: 来源:2012-2013学年浙江省温州八校高三9月期初联考化学试卷(解析版) 题型:填空题
(12分)一定温度下2升的恒容容器甲中,加入2moL碳和2moLCO2发生如下反应: C(s)+CO2(g)
 2CO(g)
△H>0,测得容器中CO2的物质的量随时间t的变化关系如图所示。
2CO(g)
△H>0,测得容器中CO2的物质的量随时间t的变化关系如图所示。

(1)该反应的ΔS 0(填“>”、“<”或“=”)。在 (填“较高”或“较低”)温度下有利于该反应自发进行。
(2)列式并计算上述温度下此反应的平衡常数K 。
(结果保留一位小数)
(3)向上述平衡体系中再通入CO2,则CO2的转化率 (填增大、减小、不变、无法确定)。
(4)相同温度下,2升的恒容容器乙中加入4moL碳和4moLCO2,达到平衡。请在图中画出乙容器中CO2的物质的量随时间t变化关系的预期结果示意图。(注明平衡时CO2的物质的量)
(5)相同温度下,2升的恒容容器丙中加入4moL碳、4moLCO2和4moLCO。开始反应时
V(正) V(逆)(填>、 <、﹦)。
查看答案和解析>>
科目: 来源:2012-2013学年浙江省温州八校高三9月期初联考化学试卷(解析版) 题型:实验题
(12分)实验室常用准确称量的邻苯二甲酸氢钾(结构简式如图所示)来准确测定NaOH标准溶液的浓度,即分析化学实验中常称为“标定”的一种方法。
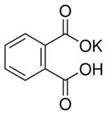
已知:①NaOH溶液的浓度在0.1 mol·L-1左右,滴定终点时溶液的pH应为9.1。
②邻苯二甲酸氢钾相对分子质量为204
(1)写出邻苯二甲酸氢钾与NaOH反应的离子方程式________________________。
(2)将用托盘天平称好的邻苯二甲酸氢钾放于锥形瓶中,加适量的水溶解,溶液呈无色,
再加入指示剂______(从甲基橙、酚酞中选择),用NaOH溶液滴定到终点时,现象是____________。
某学生进行了四次实验,实验数据如下表:
|
实验编号 |
邻苯二甲酸氢钾的质量(g) |
待测NaOH溶液的体积(mL) |
|
1 |
0.4080 |
18.20 |
|
2 |
17.10 |
|
|
3 |
16.90 |
|
|
4 |
17.00 |
(3)滴定中误差较大的是第________次实验,造成这种误差的可能原因是____________。
A.碱式滴定管在装液前未用待测NaOH溶液润洗2~3次
B.滴定开始前碱式滴定管尖嘴部分有气泡,在滴定终点读数时未发现气泡
C.盛有邻苯二甲酸氢钾溶液的锥形瓶中有少量水
D.达到滴定终点时,俯视溶液凹液面最低点读数
E.滴定过程中,锥形瓶摇荡得太剧烈,以至有些液滴飞溅出来
F.滴定到终点时,溶液颜色由无色变到了红色
(4)该同学所测得的NaOH溶液的物质的量浓度为________ mol·L-1(结果保留三位小数)。
查看答案和解析>>
科目: 来源:2012-2013学年浙江省温州八校高三9月期初联考化学试卷(解析版) 题型:填空题
(12分)相对分子质量为92的某芳香烃X是一种重要的有机化工原料,研究部门以它为初始原料设计出如下转化关系图(部分产物、合成路线、反应条件略去)。其中A是一氯代物,H是一种功能高分子,链节组成为C7H5NO。
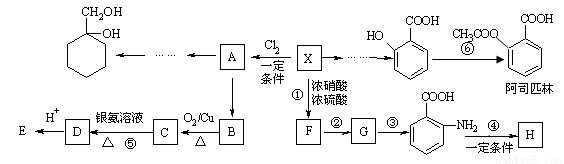
已知:
Ⅰ
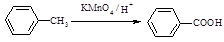
Ⅱ
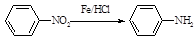 (苯胺,易被氧化)
(苯胺,易被氧化)
请根据所学知识与本题所给信息回答下列问题:
(1)H的结构简式是______________;(2)反应②的类型是______________;
(3)反应⑤的化学方程式是____________________________________________;
反应⑥的化学方程式是____________________________________________;
(4)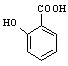 有多种同分异构体,其中符合下列条件的共有__________种
有多种同分异构体,其中符合下列条件的共有__________种
①能发生银镜反应但不能水解
②每摩尔同分异构体最多消耗2mol NaOH
③苯环上一氯代物只有两种
查看答案和解析>>
科目: 来源:2012-2013学年浙江省温州市十校联合体高三上学期期初考试化学试卷(解析版) 题型:选择题
2009年11月25日,我国提出控制温室气体排放的措施和近期指标,旨在 “善待地球——科学发展”。下列不符合这一主题的是
A.发展循环经济,构建资源节约型社会
B.加高工厂的烟囱,使烟尘和废气远离地表,减少污染
C.减少直至不使用对大气臭氧层起破坏作用的氟氯烃
D.采用“绿色化学”工艺,建立环境友好型化工体系
查看答案和解析>>
科目: 来源:2012-2013学年浙江省温州市十校联合体高三上学期期初考试化学试卷(解析版) 题型:选择题
随着科学技术的不断进步,研究物质的手段和途径越来越多,N5+、H3、O4、C60等已被发现。下列有关说法中,正确的是
A.N5+离子中含有36个电子 B.O2与O4属于同位素
C.C60是原子晶体 D.H2与H3属于同素异形体
查看答案和解析>>
科目: 来源:2012-2013学年浙江省温州市十校联合体高三上学期期初考试化学试卷(解析版) 题型:选择题
下列表示正确的是
A. CO2的比例模型: B. 铝离子的结构示意图:
B. 铝离子的结构示意图: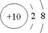
C. 次氯酸的结构式: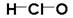 D. 甲基的电子式:
D. 甲基的电子式: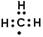
查看答案和解析>>
科目: 来源:2012-2013学年浙江省温州市十校联合体高三上学期期初考试化学试卷(解析版) 题型:选择题
NA为阿伏加德罗常数,下列有关叙述正确的是
A.标准状况下,2.24 L C6H14中含有的共用电子对数为1.9NA
B.同温同压下,原子数均为NA的氢气和氦气具有相同的体积
C.0.50 mol的亚硫酸钠中含有的钠离子数为NA
D.常温下,7.1gCl2与足量NaOH溶液作用,转移电子的数目为0.2NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com