
科目: 来源:2014届海南省高一下学期期末考试化学试卷(解析版) 题型:选择题
下列对有机物结构的叙述中不正确的是 ( )
A、硝基、羟基、氯原子、苯环、甲基都是官能团
B、邻二甲苯不存在同分异构体,说明苯分子中所有的碳碳键都是完全相同的
C、乙烯、苯分子中所有原子共平面
D、CH2Cl2有两种同分异构体
查看答案和解析>>
科目: 来源:2014届海南省高一下学期期末考试化学试卷(解析版) 题型:选择题
下列叙述中涉及的反应属于取代反应的是 ( )
A、一定条件下,苯与浓硫酸和浓硝酸的混合液生成硝基苯
B、乙烯在催化剂作用下水化成乙醇
C、钠在乙醇中生成乙醇钠
D、水壶中的水垢通常用醋洗去
查看答案和解析>>
科目: 来源:2014届海南省高一下学期期末考试化学试卷(解析版) 题型:选择题
下列各组物质中,可用溴水溶液来鉴别的是 ( )
A、乙烯与乙炔 B、乙烯与甲烷
C、苯与直馏汽油 D、苯与CCl4
查看答案和解析>>
科目: 来源:2014届海南省高一下学期期末考试化学试卷(解析版) 题型:填空题
(6分)某温度时,在2L密闭容器中,X、Y、Z三种气态物质的物质的量随时间变化的曲线如图所示。由图中数据分析:

(1)该反应的化学方程式: ;
(2)0~2min末,X的平均反应速率为 mol·L-1·min-1;
(3)3min后图中曲线所表示的含义是
。
查看答案和解析>>
科目: 来源:2014届海南省高一下学期期末考试化学试卷(解析版) 题型:实验题
(13分)图2是研究甲烷取代反应实验装置图,具体的实验方法是:
取一个100 mL的大量筒,先后收集20 mL CH4和80 mL Cl2,进行实验。
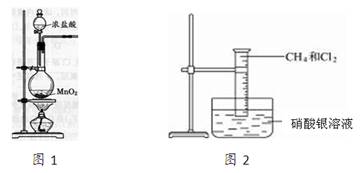
(1)实验室制取氯气的装置如上图1所示,请写出烧瓶中的反应方程式为:
。浓盐酸在反应中体现了
性和 性。
(2)下列常用的干燥剂中,不能干燥氯气的是 。
A、浓硫酸 B、P2O5 C、无水氯化钙 D、碱石灰
(3)氯气是 色的有毒气体,实验中剩余的氯气可用NaOH溶液吸收,请写出发生的离子方程式: 。
(4)若研究甲烷与氯气的取代反应,还需要的条件是___________。若将如图2所示装置放在强光下照射会有_________________(填可能发生的不良后果)。
(5)若量筒中的甲烷和氯气的量比较大,放在光亮的地方足够长的时间,下方水槽中的现象是_________________________________,产生此现象的原因是:_____ _____________________ (用简要的文字和方程式说明)。
查看答案和解析>>
科目: 来源:2014届海南省高一下学期期末考试化学试卷(解析版) 题型:推断题
(14分)下图是几种有机物的转换关系,请按要求填空:

已知:A是来自石油的重要有机化工原料,对水果有催熟作用;75%的B可用于医用消毒;E是具有果香味的有机物;F是一种高聚物,可制成多种包装材料。
(1)A的分子式为 ,A和酸性高锰酸钾溶液作用的现象是: 。
(2)C的名称 ,F的结构简式为 。
(3)D分子中的官能团名称是 ,请设计一种实验来验证D物质存在该官能团的方法是
。
(4)请写出反应⑤的方程式: 。
(5)请填写反应类型:A生成F ;
(6)下列关于A和F的叙述正确的是 。
A、A常温下是气体,为纯净物;F常温下是固体,为混合物
B、A与F的化学性质完全相同
C、取等质量的A和F完全燃烧后,生成的CO2和H2O的质量分别相等
D、取等物质的量的A和F完全燃烧后,生成的CO2和H2O的物质的量分别相等
查看答案和解析>>
科目: 来源:2014届海南省高一下学期期末考试化学试卷(解析版) 题型:填空题
(10分)已知NO2转化为N2O4的反应是放热反应且是可逆反应:2NO2 (g) N2O4(g)。如下图1所示,烧瓶A、B中装有相同浓度的NO2和N2O4的混合气体,中间用止水夹K夹紧,烧杯甲、乙分别盛放100mL冷水和热水。
N2O4(g)。如下图1所示,烧瓶A、B中装有相同浓度的NO2和N2O4的混合气体,中间用止水夹K夹紧,烧杯甲、乙分别盛放100mL冷水和热水。


图1
图2
(1)图1中___________瓶中气体颜色更深?(填“A”或“B”)。请比较平衡时反应速率:A瓶__________B瓶;(填“>”“<”或“=”)
(2)在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化的曲线如上图2所示。请比较图2中A、B两点混合气体的平均相对分子质量:A点_________B点。(填“>”“<”或“=” )
(3)平衡常数定义为一定条件下,可逆反应平衡时产物浓度系数次幂的乘积与反应物浓度系数次幂的乘积比。 即aA(g)+bB(g) pC(g)+qD(g)中K=
pC(g)+qD(g)中K= 
下如:N2(g)+3H2 (g) 2NH3 (g)的平衡常数表示式K=
2NH3 (g)的平衡常数表示式K=
①2NO2 (g) N2O4(g)的平衡常数表达式K=
N2O4(g)的平衡常数表达式K=
②平衡常数K的具体值会随温度而改变。请比较上图2中A点和B点所对应的平衡常数数值。A点____________B点(填“>”“<”或“=”)。
查看答案和解析>>
科目: 来源:2014届海南省高一下学期期末考试化学试卷(解析版) 题型:填空题
(10分)河南的郑州、洛阳及南阳市率先使部分汽车采用封闭运行方式,试用新的汽车燃料——车用乙醇汽油。乙醇,俗名酒精,它是以玉米、小麦、薯类等为原料经发酵、蒸馏而制成的。乙醇进一步脱水,再加上适量汽油后形成变性燃料乙醇。而车用乙醇汽油就是把变性燃料乙醇和汽油按一定比例混配形成的车用燃料。结合有关知识,完成以下问题:
(1)乙醇的结构简式为_________________。汽油是由石油分馏所得的低沸点烷烃,其分子中的碳原子数一般在C5—C11范围内,如戊烷,其分子式为_________________,其同分异构体结构简式分别为_______________________、________________________、_______________________。
(2)乙醇可由含淀粉〔(C6H10O5)n〕的农产品(如玉米、小麦、薯类等)经发酵、蒸馏而得,这就是酿酒。酿酒主要有两步:①淀粉+水 葡萄糖(C6H12O6)
②葡萄糖
葡萄糖(C6H12O6)
②葡萄糖 乙醇。
乙醇。
请写出淀粉生成葡萄糖的化学方程式:___________________________________。
(3)乙醇充分燃烧的产物为_____________和_____________。
(4)车用乙醇汽油称为环保燃料,其原因是________________________________。
查看答案和解析>>
科目: 来源:2014届海南省高一下学期期末考试化学试卷(解析版) 题型:实验题
(11分) “酒是陈的香”,就是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用如图所示的装置制取乙酸乙酯。回答下列问题:

(1)写出制取乙酸乙酯的化学反应方程式:
(2)试管B中盛放的溶液是 ,其主要作用是
。
(3)装置中通蒸气的导管不能插入试管B的溶液中,目的是 。
(4)若要把制得的乙酸乙酯分离出来,应采用的实验操作是 。
(5)做此实验时,往往还向大试管A中加入几块碎瓷片,其目的是 。
(6)用30g乙酸与46g乙醇反应,如果实际产量是理论产量的67%,则实际得到乙酸乙酯的质量是 。
A.44g B. 29.5g C.74.8g D.88g
查看答案和解析>>
科目: 来源:2014届福建省高一下学期期末联考化学试卷(解析版) 题型:选择题
现代科技将20984Po涂于飞机表面,可以吸收和屏蔽雷达波和红外线辐射,从而达到隐形目的。下面列出该原子核内中子数与核外电子数之差的数据正确的是
A.41 B.84 C.125 D.209
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com