
科目: 来源:2013届福建省高二下学期期末联考化学试卷(解析版) 题型:选择题
在水溶液中,YO3n-和S2-发生如下反应:YO3n- + 3S2- +6H+ = Y- + 3S↓+ 3H2O,则YO3n-中Y元素的化合价和原子最外层电子数分别为( )
A.+4、6 B.+7、7 C.+5、7 D.+5、5
查看答案和解析>>
科目: 来源:2013届福建省高二下学期期末联考化学试卷(解析版) 题型:选择题
下列离子方程式书写正确的是( )
A.NaHSO4溶液与Ba(OH)2溶液反应至中性: H++SO42—+Ba2++OH— = BaSO4↓+H2O
B.NaClO溶液与FeCl2溶液混合:Fe2+ + 2ClO- + 2H2O = Fe(OH)2↓ + 2HClO
C.NH4HSO3溶液与足量NaOH溶液反应:NH4+ + OH-= NH3↑ + H2O
D.将1mol/L NaAlO2溶液和1.5mol/L的HCl溶液等体积互相均匀混合:
6AlO2-+9H++3H2O=5Al(OH)3↓+Al3+
查看答案和解析>>
科目: 来源:2013届福建省高二下学期期末联考化学试卷(解析版) 题型:选择题
有一无色溶液,可能含有K+、Al3+、Mg2+、NH4+、Cl-、SO42-、HCO3-、MnO4-中的一种或几种。为确定其成分,进行如下实验:①取部分溶液,逐滴滴入NaOH溶液至过量,只观察到白色沉淀先增多后又部分溶解,无其它明显现象;②另取部分溶液,加入HNO3酸化的Ba(NO3)2溶液,无沉淀产生。下列推断正确的是( )
A.肯定有Al3+、Mg2+、Cl-,可能有K+
B.肯定有Al3+、Mg2+、Cl-,可能有NH4+
C.肯定有Al3+、Mg2+、HCO3-,肯定没有MnO4-
D.肯定有K+、Al3+、MnO4-,可能有HCO3-
查看答案和解析>>
科目: 来源:2013届福建省高二下学期期末联考化学试卷(解析版) 题型:选择题
已知常温下可用Co2O3制备Cl2,反应前后存在六种微粒:Co2O3﹑H2O﹑Cl2、H+ 、Cl-和Co2+ 。下列叙述不正确的是( )
A.氧化产物为Cl2
B.氧化剂与还原剂的物质的量之比为1∶2
C.若有3mol H2O生成,则反应中有2mol电子转移
D.当该反应生成2.24L Cl2时,则反应中有0.1mol电子转移
查看答案和解析>>
科目: 来源:2013届福建省高二下学期期末联考化学试卷(解析版) 题型:选择题
水热法制备纳米颗粒Y(化合物)的反应为:
3Fe2++2S2O2-3+O2+aOH-==Y+S4O2-6+2H2O下列说法中,不正确的是( )
A.S2O2-3是还原剂
B.Y的化学式为Fe2O3
C.a =4
D.每有1molO2参加反应,转移的电子总数为4mol
查看答案和解析>>
科目: 来源:2013届福建省高二下学期期末联考化学试卷(解析版) 题型:选择题
继科学家发现C3O2是金星大气成分之后,2004年,美国科学家通过“勇气”号太空车探测出水星大气中含有一种称为硫化羰(化学式为COS)的物质。已知硫化羰与二氧化碳的结构相似,但在氧气中会燃烧,下列有关C3O2与硫化羰的说法中正确的是( )
A.C3O2可以在氧气中完全燃烧生成CO2
B.C3O2和CO2都是碳的氧化物,它们互为同分异构体
C.COS是由极性键构成的非极性分子,分子中所有原子都满足8电子稳定结构
D.COS在氧气中完全燃烧后,生成物是CO2和SO3
查看答案和解析>>
科目: 来源:2013届福建省高二下学期期末联考化学试卷(解析版) 题型:选择题
短周期元素W、X、Y和Z的原子序数依次增大。其中W的阴离子的核外电子数与X、Y、Z原子的核外内层电子数相同。X的一种核素在考古时常用来鉴定一些文物的年代,工业上采用液态空气分馏方法来生产Y的单质,而Z不能形成双原子分子。根据以上叙述,下列说法中正确的是( )
A.以上四种元素的原子半径大小为W<X<Y<Z
B.W、X、Y、Z原子的核外最外层电子数的总和为20
C.W与Y可形成既含极性共价键又含非极性共价键的化合物
D.由W与X组成的化合物的沸点总低于由W与Y组成的化合物的沸点
查看答案和解析>>
科目: 来源:2013届福建省高二下学期期末联考化学试卷(解析版) 题型:填空题
(9分)根据下列变化关系:

请填空:
(1)A物质的名称_____ 。B溶液为____________.作用为_________________________
(2)写出④、⑥两步反应的化学方程式,在( )号中标明反应类型。
④ ________________________________________( )
⑥_______________________________________( )
查看答案和解析>>
科目: 来源:2013届福建省高二下学期期末联考化学试卷(解析版) 题型:填空题
(12分)CuCl和CuCl2都是重要的化工原料,常用作催化剂、颜料、防腐剂和消毒剂等。已知:
①CuCl可以由CuCl2用适当的还原剂如SO2、SnCl2等还原制得:
2Cu2++2Cl-+SO2+2H2O=2CuCl↓+4H++SO42-
2CuCl+SnCl2=2CuCl↓+SnCl4
②CuCl2溶液与乙二胺(H2N—CH2—CH2—NH2)可形成配离子[Cu(En)2]2+(En是乙二胺的简写):

请回答下列问题:
(1)配离子[Cu(En)2]2+的中心原子基态外围电子排布式为 ,
H、N、O三种元素的电负性由大到小的顺序是 ;
(2)SO2分子的空间构型为 ;
(3)乙二胺分子中氮原子轨道的杂化类型为 ,乙二胺和三甲胺[N(CH3)3]均属于胺,但乙二胺比三甲胺的沸点高的多,原因是 。
(4)配离子[Cu(En)2]2+的配位数为 ,该微粒含有的微粒间的作用力类型有 (填字母);
A.配位键 B.极性键 C.离子键 D.非极性键
E.氢键 F.金属键
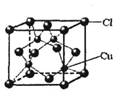
(5)CuCl的晶胞结构如右图所示,其中Cl-的配位数(即与Cl-最近距离的Cu+的个数)为 。
查看答案和解析>>
科目: 来源:2013届福建省高二下学期期末联考化学试卷(解析版) 题型:填空题
(8分)A、B、D、E是短周期中构成蛋白质的重要元素,其性质见下表。Fe、Co元素的常见化合价为+2、+3,能形成各种有色配离子。
|
|
A |
B |
D |
E |
|
化合价 |
-4 |
-2 |
-3 |
-2 |
|
电负性 |
2.5 |
2.5 |
3.0 |
3.5 |
(1)基态Fe原子的电子排布式为 。
(2)Fe、Co两元素的第三电离能I3(Fe) I3(Co)(填“<”或“>”)。
(3)B、D、E的气态氢化物的沸点由高到低的顺序为 (填化学式)。
(4)Co与E形成的化合物晶胞如右图所示,则该化合物的化学式为 。(用元素符号表示)

(5)Co的离子能与AD-离子生成各种配合物。紫色的配离子[Co(AD)6]4- 是一种相当强的还原剂,在加热时能与水反应生成[Co(AD)6]3-。
①HAD分子中A元素的杂化类型为 ,D元素的化合价为 。
②写出[Co(AD)6]4-在加热时与水反应生成[Co(AD)6]3-的离子方程式: 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com