
科目: 来源:2013届河南省高二第一次月选4考化学试卷(解析版) 题型:填空题
(6分)铅蓄电池是典型的可充型电池,它的正负极板是惰性材料,电池总反应式为:Pb+PbO2+4H++2SO42-  2PbSO4+2H2O回答下列问题(不考虑氢、氧的氧化还原)
2PbSO4+2H2O回答下列问题(不考虑氢、氧的氧化还原)
(1)放电时:正极的电极反应式是 ;当外电路通过1mol电子时,电解液中消耗H2SO4 mol。
(2)充电时,Pb 和电源的 极相连,此时发生的电极反应式为 。
查看答案和解析>>
科目: 来源:2013届河南省高二第一次月选4考化学试卷(解析版) 题型:填空题
(5分)(1) 已知1 g丙烷完全燃烧生成气态水,放出的热量是47 kJ,又知:
H2O(l)== H2O(g) ΔH=+ 44 kJ·mol-1,则表示丙烷燃烧热的热化学方程式为
(2)下图中能较准确地反映丙烷燃烧时能量变化的曲线是________。

(3)已知在298K时下列反应的反应热为:
①CH3COOH(l) + 2O2 (g)=2CO2(g)+2H2O (l) △H1 =-870.3KJ/mol
②C(s)+O2 (g)=CO2 (g) △H2=-393.5KJ/mol
③H2(g)+1/2O2 (g)=H2O (l) △H3=-285.8KJ/mol
则反应:2C(s) +2H2(g) +O2(g) =CH3COOH(l)的反应热
△H= KJ/mol
查看答案和解析>>
科目: 来源:2013届河南省高二第一次月选4考化学试卷(解析版) 题型:填空题
(10分)如图所示:已知甲池的总反应式为:2CH3OH+3O2+4KOH
2K2CO3+6H2O
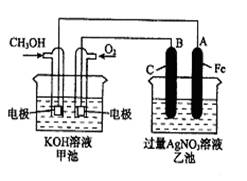
(1)请回答图中甲、乙两池的名称。甲池是 装置,乙池是 装置。
(2)B(石墨)电极的名称是 。 在图中标明电子移动的方向。
(3)通入O2的电极的电极反应式是 。
(4)乙池中反应的化学方程式为 。
(5)当乙池中A(Fe)极的质量增加5.40g时,甲池中理论上消耗O2 mL(标准状况下)
查看答案和解析>>
科目: 来源:2013届河南省高二第一次月选4考化学试卷(解析版) 题型:填空题
(共7分)有七种金属:钾、锌、铁、锡、铜、银、铂,它们的标号分别为A、B、C、D、E、F、G。①常温下,只有A和水反应生成氢气;②D、E、G都能和稀硫酸反应生成氢气,B、C、F无此性质;③C、F组成原电池时,F为正极;④在G的硫酸盐溶液中加入D,发现D溶解,G析出;⑤将G、E接触放置,E不易锈蚀;⑥以铂作电极,电解相同浓度的B和C的硝酸盐溶液时,在阴极上首先得到C,G在空气中放置极易生锈。则A是___ _,B是___ _,C是__ __,D是_ ___,E是_ ___,F是____ ,G是____
查看答案和解析>>
科目: 来源:2013届河南省高二第一次月选4考化学试卷(解析版) 题型:实验题
100ml0.50mol·L-1盐酸与100mL0.55mol·L-1NaOH溶液在如下图所示的装置中进行中和反应。通过测定反应过程中放出的热量可计算中和热。回答下列问题:

(1)从实验装置上看,图中尚缺少的一种玻璃仪器是
(2)烧杯间填满碎纸条的作用是 。
(3)实验中若改用110mL0.50mol·L-1盐酸跟100mL0.55mol·L-1NaOH溶液进行反应,与上述实验相比,所放出的热量 (填“相等”或“不相等”),所求中和热 (填“相等”或“不相等”)。
(4)用相同浓度和体积的氨水代替NaOH溶液进行上述实验,测得的中和热数值会 ;(填“偏大”“偏小”或“无影响”)。
(5)在量热计中将22.3℃、100ml 1.0mol/L的盐酸与等体积等温度的1.00mol/L的氢氧化钠溶液混合,温度最高升高到29.00℃。已知量热计的热容是46.1J/K,此条件下的NaCl溶液的比热容为4.03J/(g.K),溶液的密度为1.02g/ml,试计算生成每摩NaCl的
反应热(直接写答案) KJ/mol。
查看答案和解析>>
科目: 来源:2013届河南省高二第一次月选4考化学试卷(解析版) 题型:计算题
(8分)氢氧燃料电池是将H2通入负极,O2通入正极而发生电池反应的,其能量转换率高。
(1)若电解质溶液为KOH,负极反应为_________________________________________
(2)若电解质溶液为硫酸,其正极反应为______________________ ,若在常温下转移2mol电子,可产生水质量为_________g。
(3)若用氢氧燃料电池电解由NaCl和CuSO4组成的混合溶液,其中c(Na+)=3c(Cu2+)=3mol·L—1,取该混合液100mL用石墨做电极进行电解,通电一段时间后,在阴极收集到1.12L (标准状况)气体。此时氢氧燃料电池中消耗H2和O2的物质的量各是多少?(写出计算过程)(保留2位小数)
查看答案和解析>>
科目: 来源:2013届河南省高二第一次月选4考化学试卷(解析版) 题型:计算题
(6分)有一硝酸盐晶体,分子式为M(NO3)x·nH2O,经测定其摩尔质量为
242g / mol。取1.21 g此晶体溶于水,配制成100 mL溶液。 将其置于电解池中用惰性材料为电极进行电解。经测定,当有0.01 mol电子通过电极时,溶液中全部金属离子即在阴极上析出,电极增重0.32 g。计算:(写出计算过程)
(1) 1.21 g此盐晶体的物质的量是多少?x值是多少?
(2) 求M的相对原子质量和n值。
查看答案和解析>>
科目: 来源:2013届河南省商丘市高二上期月考化学试卷(解析版) 题型:选择题
下列说法正确的是
①需要加热方能发生的反应一定是吸热反应
②放热的反应在常温下一定很容易发生
③反应是放热还是吸热必须看反应物和生成物所具有的总能量的相对大小
④放热反应加热到一定温度引发后,停止加热反应也能继续进行
A.①②③④ B.只有①② C.只有③④ D.②③④
查看答案和解析>>
科目: 来源:2013届河南省商丘市高二上期月考化学试卷(解析版) 题型:选择题
2007年3月,温家宝指出“优化结构、提高效益和降低消耗、保护环境”,这是我国国民经济和社会发展的基础性要求。你认为下列行为不符合这个要求的是
A. 大力发展农村沼气,将废弃的秸轩转化为清洁高效的能源
B. 加快太阳能、风能、生物质能、海洋能等清洁能源的开发利用
C. 研制开发以水代替有机溶剂的化工涂料
D. 将煤转化成气体燃料可以有效地减少“温室效应”的气体产生
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com