
科目: 来源:2013届河北省高二9月月考化学试卷(解析版) 题型:选择题
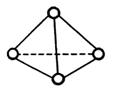
科学家已获得了极具理论研究意义的N4分子,其结构为正四面体(如右图所示),与白磷分子相似。已知断裂1molN—N键吸收193kJ热量,断裂1molN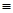 N键吸收941kJ热量,则( )
N键吸收941kJ热量,则( )
A. N4与N2互称为同位素
B. 1molN4气体转化为N2时要吸收748kJ能量
C. N4是N2的同系物
D. 1molN4气体转化为N2时要放出724kJ能量
查看答案和解析>>
科目: 来源:2013届河北省高二9月月考化学试卷(解析版) 题型:选择题
一定条件下将2mol SO2和2mol SO3气体混合于一固定容积的密闭容器中,发生反应:
2SO2+O2 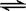 2SO3,平衡时SO3体积分数为n %,在相同温度下,分别按下列配比在上述容器中放入起始物质,平衡时SO3的体积分数大于n %的是
( )
2SO3,平衡时SO3体积分数为n %,在相同温度下,分别按下列配比在上述容器中放入起始物质,平衡时SO3的体积分数大于n %的是
( )
A.2 mol SO2 +0.5mol O2 B.6 mol SO2 + 1 mo+l O2 + 2 SO3
C.4 mol SO2 + 1 mol O2 D.3 mol SO2 + 0.5 mol O2 + 1 SO3
查看答案和解析>>
科目: 来源:2013届河北省高二9月月考化学试卷(解析版) 题型:填空题
(5分)将0.3mol的气态高能燃料乙硼烷(B2H6)在氧气中燃烧,生成固态三氧化二硼和液态水,放出649.5kJ热量,表示乙硼烷燃烧热的热化学方程式为______ __________。又已知:H2O(g)=H2O(l);△H2=-44.0kJ/mol,则11.2L(标准状况)乙硼烷完全燃烧生成气态水时放出的热量是_____________kJ。
查看答案和解析>>
科目: 来源:2013届河北省高二9月月考化学试卷(解析版) 题型:填空题
.(21分)合成氨工业对国民经济和社会发展具有重要的意义。其原理为:
N2(g)+3H2(g)
 2NH3(g) △H= -92.4KJ/mol ,据此回答以下问题:
2NH3(g) △H= -92.4KJ/mol ,据此回答以下问题:
(1)下列有关该反应速率的叙述,正确的是(选填序号) 。
a.升高温度可以增大活化分子百分数,加快反应速率
b.增大压强不能增大活化分子百分数,所以不可以加快反应速率
c.使用催化剂可以使反应的活化能降低,加快反应速率
d.活化分子间所发生的碰撞为有效碰撞
e.降低温度, V正、V逆均减小且V正减小的倍数小于V逆减小的倍数。
f.在质量一定的情况下,催化剂颗粒的表面积大小,对反应速率有显著影响
(2)①该反应的化学平衡常数表达式为K=_______________________。
②根据温度对化学平衡影响规律知,对于该反应,温度越高,其平衡常数的值越_____ 。
(3)某温度下,若把10 mol N2与30 mol H2 置于体积为10 L的密闭容器内,反应达到平衡状态时,测得平衡混合气体中氨的体积分数为20%,则该温度下反应的K=___________(可用分数表示)。能说明该反应达到化学平衡状态的是 (填字母)。
a.容器内的密度保持不变
b.容器内压强保持不变
c.υ正(N2)=2υ逆(NH3)
d.混合气体中 c(NH3)不变
e.容器内混合气体的平均摩尔质量保持不变
(4)对于合成氨反应而言,下列有关图象一定正确的是(选填序号)_____________。

(5)相同温度下,有恒容密闭容器A和恒压密闭容器B,两容器中均充入1mol N2和3 molH2,此时两容器的体积相等。在一定条件下反应达到平衡状态,A中NH3的体积分数为a,放出热量Q1 kJ;B中NH3的体积分数为b,放出热量Q2 kJ。则:a_____b(填>、=、<), Q1_____ Q2(填>、=、<), Q1_____92.4(填>、=、<)。
查看答案和解析>>
科目: 来源:2013届河北省高二9月月考化学试卷(解析版) 题型:实验题
(14分)50 mL 1.0 mol·L-1盐酸跟50 mL 1.1 mol·L-1氢氧化钠溶液在下图装置中进行中和反应,并通过测定反应过程中所放出的热量来计算中和热。试回答下列问题:

⑴大小烧杯间填满碎泡沫塑料的作用___ 。
⑵ (填“能”或“不能”)将环形玻璃搅拌棒改为环形铜棒。其原因是 。
⑶大烧杯上如不盖硬纸板,对求得中和热数值的影响是 (填“偏高”或“偏低”或“无影响”)。
⑷如果改用60 mL 1.0 mol·L-1盐酸跟50 mL 1.1 mol·L-1氢氧化钠溶液进行反应,则与上述实验相比,所放热量 (“增加”、 “减少”或“不变”),理由是 ;所求中和热数值 (“增加”、 “减少”或“不变”),理由是 。
查看答案和解析>>
科目: 来源:2013届河北省高二9月月考化学试卷(解析版) 题型:实验题
(14分)某同学在用稀硫酸与锌制取氢气的实验中,发现加入少量硫酸铜溶液可加快氢气的生成速率。请回答下列问题:
(1)上述实验中发生反应的化学方程式有 ;
(2)硫酸铜溶液可以加快氢气生成速率的原因是 ;
(3)实验室中现有 、
、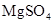 、
、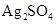 、
、 等4中溶液,可与实验中
等4中溶液,可与实验中 溶液起相似作用的是
;
溶液起相似作用的是
;
(4)要加快上述实验中气体产生的速率,还可采取的措施有 (答两种);
|
|

①请完成此实验设计,其中:V1= ,V6= ,V9= ;
②实验E中的金属呈 色;
③该同学最后得出的结论为:当加入少量 溶液时,生成氢气的速率会大大提高。但当加入的
溶液时,生成氢气的速率会大大提高。但当加入的 溶液超过一定量时,生成氢气的速率反而会下降。请分析氢气生成速率下降的主要原因
。
溶液超过一定量时,生成氢气的速率反而会下降。请分析氢气生成速率下降的主要原因
。
查看答案和解析>>
科目: 来源:2013届河北省高二9月月考化学试卷(解析版) 题型:计算题
(6分)PCl5的热分解反应如下:PCl5(g) 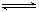 PCl3(g)
+ Cl2(g)。
PCl3(g)
+ Cl2(g)。
(1)写出反应的平衡常数表达式;
(2)已知某温度下,在容积为10.0L的密闭容器中充入2.00mol PCl5,达到平衡后,测得容器内PCl3的浓度为0.150mol/L。求该温度下的平衡常数。
(3)在相同的容器中起始充入5.00mol PCl5,达平衡后, PCl5的分解率是多少?
查看答案和解析>>
科目: 来源:2013届河北省高二化学选修四期中试卷(解析版) 题型:选择题
下列反应中生成物总能量高于反应物总能量的是
A.碳酸钙受热分解 B.乙醇燃烧
C.铝粉与氧化铁粉末反应 D.氧化钙溶于水
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com