
科目: 来源:2011-2012学年上海市松江区高三上学期期末(1月)考试化学试卷(解析版) 题型:填空题
用于金属焊接的某种焊条,其药皮由大理石、硅酸盐、硅铁等配制而成。根据题意回答:
1.Al原子的核外电子排布式为_____________________;Al与NaOH溶液反应的离子方程式为________________________________________________。
2.Si原子核外有 种不同能量的电子。硅铁属于合金,它的熔点比纯铁
(填“高”、“低”或“不一定”)。
3.Al3+与Yn-的电子数相同,Y所在族的各元素的氢化物的水溶液均显酸性,则该族氢化物中沸点最低的是________,最不稳定的是 。
4.焊接过程中,药皮在高温下产生了熔渣和一种气体,该气体是_________,该气体在固态时属于 晶体。
查看答案和解析>>
科目: 来源:2011-2012学年上海市松江区高三上学期期末(1月)考试化学试卷(解析版) 题型:填空题
(本题共8分)
白磷(P4)是一种常见的晶体,可用于制备较纯的磷酸。根据题意回答:
1.31g白磷与足量的氧气完全燃烧生成P2O5固体,释放出745.5 kJ的热量,请写出白磷燃烧的热化学反应方程式: ;
2.完成并配平白磷和氯酸溶液反应的化学方程式:
P4 + HClO3 + → HCl + H3PO4
3.白磷有毒,在实验室可采用CuSO4溶液进行处理,其反应为:
11P4 + 60CuSO4 + 96H2O → 20Cu3P + 24H3PO4 + 60H2SO4
该反应的氧化产物是 ,若有1.1 mol P4反应,则有 mol电子转移。
4.磷的一种化合物叫亚磷酸(H3PO3)。已知:⑴0.1 mol/L H3PO3溶液的pH = 1.7;⑵H3PO3与NaOH反应只生成Na2HPO3和NaH2PO3两种盐;⑶H3PO3和碘水反应,碘水棕黄色褪去,再加AgNO3有黄色沉淀生成。关于H3PO3的说法:①强酸;②弱酸;③二元酸;④三元酸;⑤氧化性酸;⑥还原性酸,其中正确的是 .
A.②④⑥ B.②③⑥ C.①④⑤ D.②③⑤
查看答案和解析>>
科目: 来源:2011-2012学年上海市松江区高三上学期期末(1月)考试化学试卷(解析版) 题型:填空题
(本题共8分)
NO和CO都是有毒的气体,利用催化技术能够将它们转变成无毒的CO2和N2。一定量的NO和CO进行如下反应:2NO+2CO 2CO2+N2,其部分化学平衡常数如下表:
2CO2+N2,其部分化学平衡常数如下表:
|
T(℃) |
0 |
50 |
100 |
|
K |
0.5 |
1.05 |
2.56 |
根据题意回答(均不考虑温度变化对催化剂催化效率的影响):
1.若把化学方程式写为NO+CO CO2+1/2N2,则100℃时,K的值=
。
CO2+1/2N2,则100℃时,K的值=
。
2.上述反应达到化学平衡后,下列措施能提高NO转化率的是________。
A.选用更有效的催化剂 B.升高反应体系的温度
C.降低反应体系的温度 D.缩小容器的体积
3.若上述反应在容积不变的密闭容器中进行,该可逆反应达到平衡的标志是____
A.气体的密度不再变化
B.单位时间内消耗的CO与生成的CO2的物质的量之比为1︰1
C.气体的压强不再变化
D.各气体的浓度相等
4.某温度下,将0.02 mol的NO和0.02 mol的CO的混合气体充入一装有催化剂的容器中,充分反应后,测得混合气体中CO的体积分数为0.125,则CO的转化率为 。
查看答案和解析>>
科目: 来源:2011-2012学年上海市松江区高三上学期期末(1月)考试化学试卷(解析版) 题型:实验题
(本题共12分)
下图是模拟工业制硝酸原理的实验装置。先用酒精灯对硬质玻璃管里的三氧化二铬加热,然后把空气鼓入盛有浓氨水的锥形瓶,当三氧化二铬保持红热状态时,移去酒精灯。根据题意回答:
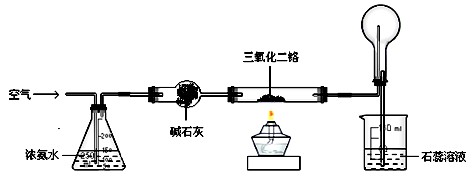
1.硬质玻璃管里发生反应的化学方程式为 。
当三氧化二铬红热时,要移去酒精灯,原因是: 。
2.圆底烧瓶里的实验现象是 ,鼓入空气的作用是 。
3.实验过程中,如果慢慢地鼓入空气,石蕊溶液的颜色 。
4.实验结束后,在圆底烧瓶内壁上有时会看到少量无色晶体,写出生成该晶体的化学方程式: 。
5.新制的三氧化二铬催化效果较好。实验室一般用加热分解(NH4)2Cr2O7的方法制三氧化二铬,反应的化学方程式为 。
6.工业上要获得浓度较大的硝酸,往往在稀硝酸中加入吸水剂硝酸镁或浓硫酸,然后 (填一种操作名称)。实验室里保存浓硝酸的方法是 。
查看答案和解析>>
科目: 来源:2011-2012学年上海市松江区高三上学期期末(1月)考试化学试卷(解析版) 题型:填空题
(本题共12分)
硼镁泥是一种工业废料,主要成份是MgO(占40%),还有CaO、MnO、Fe2O3、FeO、Al2O3、SiO2等杂质,以此为原料制取的硫酸镁,可用于印染、造纸、医药等工业。从硼镁泥中提取MgSO4·7H2O的流程如下:

根据题意回答:
1.实验中需用0.8mol/L的硫酸800 mL,若用98%的浓硫酸(ρ= 1.84 g/mL)来配制,量取浓硫酸时,需使用的量筒的规格为
A.10 mL B.20 mL C.50 mL D.100 mL
2.加入的NaClO可与Mn2+反应:Mn2+ + ClO- + H2O → MnO2↓ + 2H+ + Cl-,还有一种离子也会被NaClO氧化,该反应的离子方程式为 。
3.滤渣的主要成份除含有Fe(OH)3、Al(OH)3外,还有 。
4.在“除钙”前,需检验滤液中Fe3+是否被除尽,简述检验方法 。
5.已知MgSO4、CaSO4的溶解度如下表:
|
温度(℃) |
40 |
50 |
60 |
70 |
|
MgSO4 |
30.9 |
33.4 |
35.6 |
36.9 |
|
CaSO4 |
0.210 |
0.207 |
0.201 |
0.193 |
“除钙”是将MgSO4和CaSO4混合溶液中的CaSO4除去,根据上表数据,简要说明操作步骤 。“操作I”是将滤液继续蒸发浓缩,冷却结晶, ,便得到了MgSO4·7H2O。
6.实验中提供的硼镁泥共100 g,得到的MgSO4·7H2O为172.2 g,则MgSO4·7H2O的产率为 。
查看答案和解析>>
科目: 来源:2011-2012学年上海市松江区高三上学期期末(1月)考试化学试卷(解析版) 题型:填空题
(本题共8分)
已知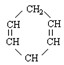 可简写为
可简写为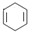 。现有某化合物W的分子结构可表示为
。现有某化合物W的分子结构可表示为 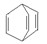 。根据题意回答:
。根据题意回答:
1.W属于
A.芳香烃 B.环烃 C.不饱和烃 D.炔烃
2.W的分子式为 ,它的一氯代物有 种。
3.有关W的说法错误的是
A.能发生还原反应 B.能发生氧化反应
C.易溶于水 D.等质量的W与苯分别完全燃烧,前者消耗的氧气多
4.W有一种芳香族的同分异构体,该物质能在一定条件下发生聚合反应,相应的化学方程式为 。
查看答案和解析>>
科目: 来源:2011-2012学年上海市松江区高三上学期期末(1月)考试化学试卷(解析版) 题型:填空题
(本题共12分)
A是石油化学工业最重要的基础原料,以A为有机原料,无机试剂任选,按下列途径合成一种常见的医用胶(结构简式为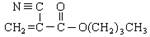 )
)
已知两个醛分子在一定条件下可以发生如下反应;
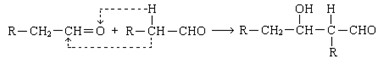
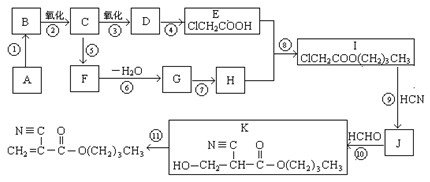
根据题意回答:
1.A的结构简式是_________________,D的官能团名称是 。
2.⑥的反应条件是 ,I→J的另一生成物是 。
3.属于取代反应的有(填反应序号)____________,⑩的反应类型是 。
4.写出⑤的化学方程式:_____________________________________________________。
5.F有多种同分异构体,其中能够在NaOH溶液中发生反应的同分异构体有 种。
6.如果以F为原料经过三步合成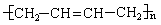 ,对应的反应类型分别为
,对应的反应类型分别为
。
查看答案和解析>>
科目: 来源:2011-2012学年上海市松江区高三上学期期末(1月)考试化学试卷(解析版) 题型:计算题
(本题共16分)铁氧体是一类磁性材料,通式为MO·xFe2O3(M为二价金属离子),如Fe3O4可表示为FeO·Fe2O3,制备流程为:

根据题意回答:
1.现称取2.8 g铁粉,加入一定量的稀硫酸使其完全溶解后,再加入 g的FeCl3固体,经上述反应后,方可得到纯净的Fe3O4。
2.如果以MgSO4和FeCl3为原料,要获得18.0克MgO·2Fe2O3,在制取过程中至少需要1 mol/L的NaOH溶液 mL。
3.在一次制备Fe3O4的实验中,由于反应物比例控制不当,获得了另一种产品。取一定量该产品溶于足量盐酸中,还需通入标准状况下672 mLCl2才能把溶液中的Fe2+全部氧化为Fe3+,然后把所得溶液蒸干,灼烧至恒重,得9.6 g固体。该产品的化学式为 。
4.有一种在电子工业上应用广泛的含铬铁氧体,其组成可表示为: ,现有15.2
g
FeSO4,经Cr2O72-、H2O2等物质处理后(不再引入含铁物质),可得到含铬铁氧体的质量范围为
。
,现有15.2
g
FeSO4,经Cr2O72-、H2O2等物质处理后(不再引入含铁物质),可得到含铬铁氧体的质量范围为
。
查看答案和解析>>
科目: 来源:2011-2012学年四川省乐山市高三上学期期末教学质量检测化学试卷(解析版) 题型:选择题
下列各组物质中,常温下能起反应产生气体的是
A.铜跟稀硫酸 B.铁跟浓硫酸 C.铝跟浓硝酸 D.铜跟浓硝酸
查看答案和解析>>
科目: 来源:2011-2012学年四川省乐山市高三上学期期末教学质量检测化学试卷(解析版) 题型:选择题
一定条件下,在一体积恒定的容器中发生CO+NO2 CO2+NO反应,达到化学平衡后,降低温度,混合物的颜色变浅,下列有关该反应的说法中正确的是
CO2+NO反应,达到化学平衡后,降低温度,混合物的颜色变浅,下列有关该反应的说法中正确的是
A.正反应为吸热反应 B.正反应为放热反应
C.降温后CO的浓度增大 D.降温后各物质的浓度不变
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com