
科目: 来源:2014届浙江省宁波市八校高一下学期期末联考化学试卷(解析版) 题型:选择题
在25℃、1.01×105Pa下,将22gCO2通入到750mL 1.0mol·L-1的NaOH溶液中充分反应,放出x kJ热量。在该条件下1molCO2通入到2L 1.0mol·L-1的NaOH溶液中充分反应,放出ykJ热量,则CO2与NaOH反应生成NaHCO3的热化学反应方程式为
A.CO2(g) + NaOH(aq) = NaHCO3(aq) △H= - (2y-x) kJ·mol-1
B.CO2(g) + NaOH(aq) = NaHCO3(aq) △H= - (4x-y) kJ·mol-1
C.CO2(g) + NaOH(aq) = NaHCO3(aq) △H= - (2x-y) kJ·mol-1
D.CO2(g) + NaOH(aq) = NaHCO3(aq) △H= - (8x-2y) kJ·mol-1
查看答案和解析>>
科目: 来源:2014届浙江省宁波市八校高一下学期期末联考化学试卷(解析版) 题型:选择题
如图所示装置,两玻璃管中盛有含酚酞的NaCl饱和溶液,C(Ⅰ)、C(Ⅱ)为多孔石墨电极。接通S1后,C(Ⅰ)附近溶液变红,两玻璃管中有气体生成。一段时间后(两玻璃管中液面未脱离电极),若断开S1,接通S2,电流表的指针发生偏转。下列说法不正确的是
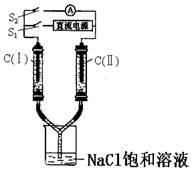
A.接通S1时,C(Ⅰ)的电极名称为阴极
B.接通S1时,直流电源的右边为正极
C.接通S2时,C(Ⅰ)电极反应式为H2-2e-+2OH-=2H2O
D.若将原来的电解质溶液换成含酚酞的MgCl2溶液,接通S1后现象相同
查看答案和解析>>
科目: 来源:2014届浙江省宁波市八校高一下学期期末联考化学试卷(解析版) 题型:选择题
等质量且完全相同的三份铁a、b和c,分别加入到足量稀H2SO4中,a中同时加入适量CuSO4溶液, c中同时加入适量CH3COONa。下列各图中表示其产生氢气总体积(V)与时间(t)的关系,其中正确的是
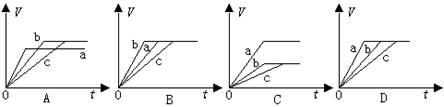
查看答案和解析>>
科目: 来源:2014届浙江省宁波市八校高一下学期期末联考化学试卷(解析版) 题型:选择题
在一定条件下,萘可与浓硝酸、浓硫酸两种混酸反应生成二硝基化合物,它是1,5-二硝基萘和1,8-二硝基萘的混合物。
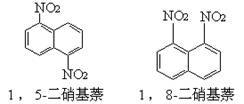
后者可溶于质量分数大于98%的硫酸,而前者不能。利用这一性质可以将这二种异构体分离。在上述硝化产物中加入适量的98.3%硫酸,充分搅拌,用耐酸漏斗过滤,欲从滤液中得到固体1,8-二硝基萘,应采用的方法是
A.对所得的滤液蒸发浓缩冷却结晶 B.向滤液中缓缓加入水后过滤
C.向滤液中缓缓加入Na2CO3溶液后过滤 D.将滤液缓缓加入水中后过滤
查看答案和解析>>
科目: 来源:2014届浙江省宁波市八校高一下学期期末联考化学试卷(解析版) 题型:填空题
(6分)下图每一个字母代表一种反应物或生成物。已知在常温下A是固体,B、C、E、F、G均为气态化合物,其中B、E为气态氢化物,X为空气中的常见成分之一。根据下列反应框图填空(有些反应条件已略去)。

(1)工业上C→D的设备名称是 ;
(2)当小心加热H与E化合生成的物质时,分解得到一种与CO2具有相同原子数目和相同电子数目的气体,同时还有一种无色无味的液体生成。试写出相应的化学方程式
_______ ___ ;
(3)I的浓溶液有许多重要的性质,在与含有水分的蔗糖作用过程中不能显示的性质是 ;
A.酸性 B.脱水性 C.强氧化性 D.吸水性
(4)在铁和铜的混合物中,加入一定量的H的稀溶液,充分反应后剩余m1 g金属,再向其中加入一定量的I的稀溶液,充分振荡后,剩余m2 g金属,则m1 与m2之间的关系是 。
A.m1 一定大于m2 B.m1 可能等于m2
C.m1 一定等于m2 D.m1 可能大于m2
查看答案和解析>>
科目: 来源:2014届浙江省宁波市八校高一下学期期末联考化学试卷(解析版) 题型:填空题
(11分)(Ⅰ)A、B、C和D代表原子序数依次增大的四种短周期元素,它们满足以下条件:
①C的原子序数是A、B的原子序数之和,A、C、D的最外层电子数和为13;
②D的原子序数是C的2倍,D的最高价氧化物对应的水化物是二元强酸。
试根据以上叙述回答:
(1)B单质的电子式为 ,画出C元素的原子结构示意图 ;
(2)下列环境问题与B与C形成的化合物有关的是 ;
A.温室效应 B.光化学烟雾 C.酸雨 D.PM2.5
(3)A、B、C和D四种元素可形成一化合物,其原子个数之比为8∶2∶4∶1。该化合物属于 (填晶体类型)。
(Ⅱ)现有下列短周期元素相关性质的数据:
|
元素编号 元素性质 |
① |
② |
③ |
④ |
⑤ |
⑥ |
⑦ |
|
原子半径(10-10m) |
0.74 |
1.60 |
1.52 |
1.10 |
0.99 |
1.86 |
0.75 |
|
最高正化合价 |
|
+2 |
+1 |
+5 |
+7 |
+1 |
+5 |
|
最低负化合价 |
-2 |
|
|
-3 |
-1 |
|
-3 |
试回答下列问题:
(1)元素⑤在周期表中的位置 ;元素②的单质与CO2反应的化学方程式 ,该单质可通过电解法制得,下列金属中人类最早开发和利用的是 ;
A.铁 B.铝 C.金 D.铜
(2)元素④与元素⑦相比较,气态氢化物较稳定的是 (填结构式);
(3)元素④形成的+3和+5价的氯化物中,各原子均达到8电子稳定结构的化合物是 。(写化学式)
查看答案和解析>>
科目: 来源:2014届浙江省宁波市八校高一下学期期末联考化学试卷(解析版) 题型:填空题
(6分)2008年北京奥运会所用火炬燃料为丙烷(C3H8),悉尼奥运会所用火炬燃料为65%丁烷(C4H10)和35%丙烷(C3H8),已知常温下1mol丙烷燃烧放出2220kJ热量,1mol正丁烷燃烧放出2878kJ热量,1mol异丁烷燃烧放出2869.6kJ热量。试回答下列问题:
(1)表示正丁烷燃烧的热化学反应方程式 ;
(2)下列有关说法正确的是 ;
A.奥运火炬燃烧时的能量转化主要是由化学能转变为热能
B.相同条件下,正丁烷的热值比丙烷大
C.正丁烷比异丁烷不稳定
D.异丁烷分子中的碳氢键比正丁烷的多
(3)已知1mol H2燃烧生成液态水放出热量是285.8 kJ,现有5mol 氢气和丙烷的混合气体,完全燃烧时放热3847kJ,则氢气和丙烷的体积比为 。
查看答案和解析>>
科目: 来源:2014届浙江省宁波市八校高一下学期期末联考化学试卷(解析版) 题型:填空题
(5分)随着世界粮食需求量的增长,农业对化学肥料的需求量越来越大,其中氮肥是需求量最大的一种化肥。而氨的合成为氮肥的生产工业奠定了基础,其原理为:N2+3H2 2NH3
2NH3
(1)在N2+3H2 2NH3的反应中,一段时间后,NH3的浓度增加了0.9mol·L-1。用N2表示其反应速率为0.15 mol·L-1·s-1,则所经过的时间为
;
2NH3的反应中,一段时间后,NH3的浓度增加了0.9mol·L-1。用N2表示其反应速率为0.15 mol·L-1·s-1,则所经过的时间为
;
A.2 s B.3 s C.4 s D.6 s
(2)下列4个数据是在不同条件下测得的合成氨反应的速率,其中反应最快的是 ;
A.v(H2)=0.1 mol·L-1·min-1 B.v(N2)=0.1 mol·L-1·min-1
C.v(NH3)=0.15 mol·L-1·min-1 D.v(N2)=0.002mol·L-1·min-1
(3)在一个绝热、容积不变的密闭容器中发生可逆反应:N2(g)+3H2(g) 2NH3(g) △H<0。下列各项能说明该反应已经达到平衡状态的是
。
2NH3(g) △H<0。下列各项能说明该反应已经达到平衡状态的是
。
A.容器内气体密度保持不变
B.容器内温度不再变化
C.断裂1mol N≡N键的同时,断裂6 mol N—H键
D.反应消耗N2、H2与产生NH3的速率之比1︰3︰2
查看答案和解析>>
科目: 来源:2014届浙江省宁波市八校高一下学期期末联考化学试卷(解析版) 题型:填空题
(9分)(1)下表为烯类化合物与溴发生加成反应的相对速率(以乙烯为标准)。
|
烯类化合物 |
相对速率 |
|
(CH3)2C=CHCH3 |
10.4 |
|
CH3CH=CH2 |
2.03 |
|
CH2=CH2 |
1.00 |
|
CH2=CHBr |
0.04 |
下列化合物与溴加成时,取代基对速率的影响与表中规律类似,其中反应速率最快的是_______________(填序号);
A.(CH3)2C=C(CH3)2 B.CH3CH=CHCH2CH3 C.CH2=CH CH3 D.CH2=CHBr
(2)0.5mol某炔烃最多能与1molHCl发生加成反应得到氯代烃,生成的氯代烃最多能与3mol Cl2发生取代反应,生成只含C、Cl两种元素的化合物。则该烃的结构简式是 ;
(3)某芳香烃A,其相对分子质量为104,碳的质量分数为92.3%。
①A分子中可能共平面的碳原子最多有 个;
②芳香烃A在一定条件下可生成加聚高分子,该高分子结构中的链节为 ;
③一定条件下,A与氢气反应,得到的化合物中碳的质量分数为85.7%,写出形成该化合物的有机反应方程式 ;
④已知 。请写出A与稀、冷的KMnO4溶液在碱性条件下反应生成物的结构简式 。
。请写出A与稀、冷的KMnO4溶液在碱性条件下反应生成物的结构简式 。
查看答案和解析>>
科目: 来源:2014届浙江省宁波市八校高一下学期期末联考化学试卷(解析版) 题型:实验题
(12分)实验室采用不同的实验装置研究苯与液溴的反应类型并制取少量溴苯。试回答下列各小题:Ⅰ.若用图甲装置进行进行制备实验,回答下列问题:
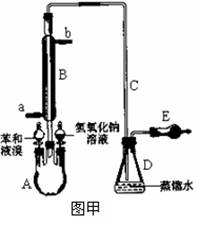
(1)写出下列仪器的名称:A 、B 。
(2)A中预先需加入的试剂是 ,E中需加入的试剂是 。
(3)仪器B除导气外的作用是 ,进水口为 (选填字母“a”或“b”)。
Ⅱ.若用图乙装置进行制备实验,回答下列问题:
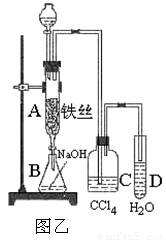
(1)C中盛放CCl4的作用是 ;
(2)实验结束时,打开A下端的活塞,让反应液流入B中,充分振荡,写出有关的离子方程式 ,然后用 仪器分离出溴苯(仍含有少量苯);
(3)反应完毕后,向试管D中滴加AgNO3溶液有 (填现象)生成,此现象说明这种获得溴苯的反应属于 (填有机反应类型)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com