
科目: 来源:2013届浙江省高二下学期期中考试化学试卷(解析版) 题型:选择题
某温度下,H2(g)+CO2(g)  H2O(g)+CO(g)的平衡常数K=9/4 。该温度下在甲、乙、丙三个恒容密闭容器中,投入H2(g)和CO2(g),其起始浓度如下表所示:
H2O(g)+CO(g)的平衡常数K=9/4 。该温度下在甲、乙、丙三个恒容密闭容器中,投入H2(g)和CO2(g),其起始浓度如下表所示:
|
起始浓度 |
甲 |
乙 |
丙 |
|
c(H2)/ mol·L-1 |
0.010 |
0.020 |
0.020 |
|
c(CO2) / mol·L-1 |
0.010 |
0.010 |
0.020 |
下列判断不正确的是( )
A.平衡时,乙中CO2的转化率大于60%
B.平衡时,甲中和丙中CO2的转化率均是60%
C.平衡时,丙中c(CO2)是甲中的2倍,是0.012 mol·L-1
D.反应开始时,丙中的反应速率最快,甲中的反应速率最慢
查看答案和解析>>
科目: 来源:2013届浙江省高二下学期期中考试化学试卷(解析版) 题型:选择题
某温度下,将2 mol A和3 mol B充入一密闭的容器中发生反应: aA(g)+B(g)
C(g)+D(g),5 min后达平衡。已知该反应在此温度下平衡常数K=1,若温度不变的情况下将容器的体积扩大为原来的10倍,A的转化率不发生变化,则B的转化率为( )
A.40% B.60% C.24% D.4%
查看答案和解析>>
科目: 来源:2013届浙江省高二下学期期中考试化学试卷(解析版) 题型:选择题
已知25℃时,电离常数Ka(HF)=3.6×10-4 mol·L-1,溶度积常数KSP(CaF2)=1.46×10-10 mol3·L-3。现向1L 0.2 mol·L-1HF溶液中加入1L 0.2 mol·L-1CaCl2溶液,则下列说法中,正确的是( )
A.25℃时,0.1 mol·L-1HF溶液中pH=1 B.该体系中有CaF2沉淀产生
C.该体系中KSP(CaF2)= 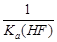 D.KSP(CaF2)随温度和浓度的变化而变化
D.KSP(CaF2)随温度和浓度的变化而变化
查看答案和解析>>
科目: 来源:2013届浙江省高二下学期期中考试化学试卷(解析版) 题型:填空题
(8分)在6份0.01 mol·L-1氨水中分别加入下列各物质:
A.浓氨水 B.纯水 C.少量K2CO3固体
D.少量浓H2SO4 E.少量NaOH固体 F.少量Al2(SO4)3固体
(1)能使c(OH-)减小、c(NH4+)增大的是 ;
(2)能使(OH-)增大、c(NH4+)减小的是 ;
(3)能使c(OH-)和c(NH4+)都增大的是 ;
(4)能使c(OH-)和c(NH4+)都减小的是 。
查看答案和解析>>
科目: 来源:2013届浙江省高二下学期期中考试化学试卷(解析版) 题型:填空题
(9分)依据氧化还原反应:2Ag+(aq) + Cu(s) = Cu2+(aq) + 2Ag(s)设计的原电池如图所示。
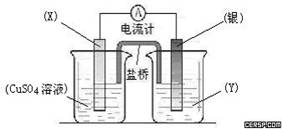
请回答下列问题:
(1)电极X的材料是 ;电解质溶液Y是 ;
(2)银电极为电池的 极,发生的电极反应为 ;X电极上发生的电极反应为 ;
(3)外电路中的电子是从 电极流向 电极。
查看答案和解析>>
科目: 来源:2013届浙江省高二下学期期中考试化学试卷(解析版) 题型:填空题
(5分)高炉炼铁中发生的基本反应如下:FeO(s)+CO(g)  Fe(s)+CO2(g)(正反应为吸热反应),已知1100℃时,该反应的化学平衡常数为0.263。
Fe(s)+CO2(g)(正反应为吸热反应),已知1100℃时,该反应的化学平衡常数为0.263。
若在1100℃时,测得高炉中c(CO2)=0.025mol·L-1,c(CO)=0.1mol·L-1,在这种情况下该反应是否处于平衡状态 (填“是”或“否”),此时化学反应速率是V正 V逆(填“>”、“<”或“=”),其原因是 。
查看答案和解析>>
科目: 来源:2013届浙江省高二下学期期中考试化学试卷(解析版) 题型:填空题
(10分)为了合理利用化学能,确保安全生产,化工设计需要充分考虑化学反应的反应热,并采取相应措施。化学反应的反应热通常用实验进行测定,也可进行理论推算。
(1) 实验测得,5g甲醇在氧气中充分燃烧生成二氧化碳气体和液态水时释放出113.5kJ的热量,则甲醇的标准燃烧热ΔH= 。
(2)今有如下两个热化学方程式:?则a b(填“>”、“=”或“<”)
H2(g)+ 1/2O2(g)=H2O(g) ΔH1=a kJ·mol-1?
H2(g)+ 1/2O2(g)=H2O(l) ΔH2=b kJ·mol-1?
(3)拆开1mol气态物质中某种共价键需要吸收的能量叫键能。从化学键的角度分析,化学反应的过程就是反应物的化学键的破坏和生成物的化学键的形成过程。在化学反应过程中,拆开化学键需要消耗能量,形成化学键又会释放能量。
|
化学键 |
H-H |
N-H |
N≡N |
|
键能/kJ·mol-1 |
436 |
391 |
945 |
已知反应N2(g)+3H2(g)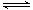 2NH3(g) △H=a
kJ·mol-1。试根据表中所列键能数据估算a
的值:_______________(注明“+”或“-”)。
2NH3(g) △H=a
kJ·mol-1。试根据表中所列键能数据估算a
的值:_______________(注明“+”或“-”)。
(4)依据盖斯定律可以对某些难以通过实验直接测定的化学反应的反应热进行推算。利用水煤气合成二甲醚的三步反应如下:
① 2H2(g) + CO(g)  CH3OH(g);ΔH =-90.8 kJ·mol-1
CH3OH(g);ΔH =-90.8 kJ·mol-1
② 2CH3OH(g)
 CH3OCH3(g) + H2O(g);ΔH=-23.5 kJ·mol-1
CH3OCH3(g) + H2O(g);ΔH=-23.5 kJ·mol-1
③
CO(g) + H2O(g)  CO2(g)
+ H2(g);ΔH=-41.3 kJ·mol-1
CO2(g)
+ H2(g);ΔH=-41.3 kJ·mol-1
总反应:3H2(g)
+ 3CO(g)  CH3OCH3(g) + CO2 (g)的ΔH= ;
CH3OCH3(g) + CO2 (g)的ΔH= ;
查看答案和解析>>
科目: 来源:2013届浙江省高二下学期期中考试化学试卷(解析版) 题型:填空题
(10分)室温下取0.2 mol·L-1HA溶液与0.2 mol·L-1 NaOH溶液等体积混合(忽略混合后溶液体积的变化),测得混合溶液的pH=8,试回答以下问题:
(1)①混合溶液中水电离出的c(OH-) 0.1mol·L-1NaOH溶液中水电离出的c(OH-);(填“>”、“<”、或“=”)
②求出混合溶液中下列算式的精确计算结果(填具体数字):
c(Na+) - c(A-)= mol·L-1
c(OH-)-c(HA) = mol·L-1
(2)室温下如果取0.2 mol·L-1 HA溶液与0.1 mol·L-1 NaOH溶液等体积混合,测得混合溶液的pH>7,则说明HA的电离程度 NaA的水解程度。(填“>”、“<”、或“=”),溶液中各离子浓度由大到小的顺序为 。
查看答案和解析>>
科目: 来源:2013届浙江省高二下学期期中考试化学试卷(解析版) 题型:计算题
(8分) 25℃时,若体积为Va、pH=a 的某一元强酸与体积为Vb、pH=b 的某一元强碱混合,恰好中和,且已知Va>Vb和 a=0.5b。则:
(1) a值可否等于3 (填“可”或“否”) ,其理由是 。
(2) a值可否等于5(填“可”或“否”) ,其理由是 。
(3)a 的取值范围 。
查看答案和解析>>
科目: 来源:2013届浙江省高二下学期期中考试实验班化学试卷(解析版) 题型:选择题
2010年上海世博会将实现环保世博、生态世博目标,下列做法中不符合这一目标的是( )
A.部分国家的展馆使用可降解的建筑材料
B.把世博会期间产生的垃圾焚烧或深埋处理
C.某些馆的外壳使用非晶硅薄膜,以充分利用太阳能
D.停车场安装了催化光解设施,用于处理汽车尾气
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com