
科目: 来源:2014届浙江省高一下学期期中考试理科化学试卷(解析版) 题型:选择题
X、Y、Z、W四种主族元素,若X的阳离子与Y的阴离子具有相同的电子层结构;W的阳离子的氧化性强于等电荷数的X阳离子的氧化性;Z阴离子半径大于等电荷数的Y的阴离子半径,则四种元素的原子序数由大到小的顺序是
A.W>X>Y>Z B.Z>X>Y>W
C.X>Y>Z>W D.Z>Y>X>W
查看答案和解析>>
科目: 来源:2014届浙江省高一下学期期中考试理科化学试卷(解析版) 题型:选择题
关于热化学方程式:2H2(g)+O2(g)=2H2O(1),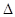 H=-571.6 kJ·mol-1,下列有关叙述不正确的是
H=-571.6 kJ·mol-1,下列有关叙述不正确的是
A.2mol H2完全燃烧生成液态水时放出571.6 kJ的热
B.1mol H2完全燃烧生成液态水时放出285.8kJ的热
C.2个氢分子完全燃烧生成液态水时放出571.6 kJ的热
D.上述热化学方程式可表示为H2(g)+1/2
O2(g)=H2O(1),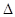 H=-285.8 kJ·mol-1
H=-285.8 kJ·mol-1
查看答案和解析>>
科目: 来源:2014届浙江省高一下学期期中考试理科化学试卷(解析版) 题型:选择题
已知热化学方程式:SO2(g)+
1/2O2(g) 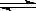 SO3(g) △H =
-98.32kJ/mol,在容器中充入2molSO2 和1molO2充分反应,最终放出的热量为
SO3(g) △H =
-98.32kJ/mol,在容器中充入2molSO2 和1molO2充分反应,最终放出的热量为
A. 小于196.64kJ B. 196.64kJ/mol C. 196.64kJ D. 大于196.64kJ
查看答案和解析>>
科目: 来源:2014届浙江省高一下学期期中考试理科化学试卷(解析版) 题型:选择题
在一定温度下,容器内某一反应中M、N的物质的量随反应时间变化的曲线如图,下列表述中正确的是

A.反应的化学方程式为:2M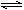 N
N
B.t2时,正逆反应速率相等,达到平衡
C.t3时,正反应速率大于逆反应速率
D.t1时,N的浓度是M浓度的2倍
查看答案和解析>>
科目: 来源:2014届浙江省高一下学期期中考试理科化学试卷(解析版) 题型:选择题
往蓝色的CuSO4溶液中逐滴加入KI溶液可以观察到产生白色沉淀X和生成含有Y物质的棕色溶液。再向反应后的混合物中不断通入SO2气体,并加热,又发现白色沉淀显著增多,溶液逐渐变成无色。则下列分析推理中错误的是
A.白色沉淀X可能是CuSO3 ,Y可能是I2
B.白色沉淀X可能是CuI,Y可能是I2
C.上述实验条件下,物质的氧化性:Cu2+>I2>SO42-
D.上述实验条件下,物质的还原性:SO2 >I->Cu+
查看答案和解析>>
科目: 来源:2014届浙江省高一下学期期中考试理科化学试卷(解析版) 题型:选择题
某合金(仅含铜、铁)中铜和铁的物质的量之和为y mol,其中Cu的物质的量分数为a,将其全部投入50 mL b mo1·L-1的硝酸溶液中,加热使其充分反应(假设NO是唯一的还原产物)。下列说法正确的是
A.若金属有剩余,在溶液中再滴入硫酸后,金属不会再溶解
B.若金属全部溶解,则溶液中一定含有Fe3+
C.若金属全部溶解,且产生336 mL气体(标准状况),则b=0.3
D.当溶液中金属离子只有Fe3+、Cu2+时,则a与b的关系为:b≥80 y (1—a/3)
查看答案和解析>>
科目: 来源:2014届浙江省高一下学期期中考试理科化学试卷(解析版) 题型:填空题
(10分)含硫化合物的种类很多,现有SO2、Na2SO3、H2SO4、CuSO4这4种常见的含硫化合物。回答下列问题:
(1)为进一步减少SO2的污染并变废为宝,我国正在探索在一定条件下用CO还原SO2得到单质硫的方法来除去SO2 。写出该反应的化学方程式: 。
(2)亚硫酸钠和碘酸钾在酸性溶液中发生以下反应:
 —
— 
①配平上面的氧化还原反应方程式.将化学计量数填入方框中。
②其中氧化剂是 ,若反应中有5 mol电子转移,则生成的碘单质是 mol。
(3) 向FeCl3和BaCl2的酸性混合溶液中通入SO2气体,有白色沉淀生成。此沉淀是
A.BaSO4 B.FeS C.BaSO3 D.S
(4)常温下,将铁棒置于浓硫酸中.无明显现象,课本上解释为发生了钝化,但有人认为未发生反应。为验证此过程,某同学经过思考,设计了如下实验:将经浓硫酸处理过的铁棒洗净后置于CuSO4溶液中,若铁棒表面 ,则发生了钝化
查看答案和解析>>
科目: 来源:2014届浙江省高一下学期期中考试理科化学试卷(解析版) 题型:填空题
(4分)已知X和Y是短周期元素中的不同族单质,W、V是化合物,他们有如下反应(式中各物质的系数,反应条件均略去):
X+W  Y+V
Y+V
试写出符合上述题意并满足下列要求的化学方程式:
(1)Y是IA族的单质 ;
(2)Y是IVA族的单质 。
查看答案和解析>>
科目: 来源:2014届浙江省高一下学期期中考试理科化学试卷(解析版) 题型:填空题
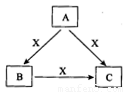
(8分)A、B、C、X是中学化学常见物质,均由短周期元素组成,转化关系如图所示。若A、B、C的焰色反应均呈黄色,水溶液均为碱性;将C加到盐酸中,有无色无味的气体X产生。
(1)写出A的电子式_____________。
(2)将X通入水玻璃溶液中,写出反应的离子方程式___________。
(3)自然界中存在B、C和H2O按一定比例结晶而成的固体。取一定量该固体溶于水配成100mL溶液,测得溶液中金属阳离子的浓度为0.5 mol/L。若取相同质量的固体加热至恒重,剩余固体的质量为__________ g。
(4)写出区分B、C溶液的一种实验方案
查看答案和解析>>
科目: 来源:2014届浙江省高一下学期期中考试理科化学试卷(解析版) 题型:实验题
(12分)某同学做同周期元素性质递变规律实验时,自己设计了一套实验方案,并记录了有关实验现象如下表。
|
实验方案 |
实验现象 |
|
1.用砂纸擦后的镁带与热水反应,再向反应后溶液中滴加酚酞 |
A.浮于水面,熔成一个小球,在水面上无定向移动,随之消失,溶液变红色 |
|
2.向Na2S溶液中滴加新制的氯水 |
B.产生气体,可在空气中燃烧,溶液变成浅红色 |
|
3.钠与滴有酚酞试液的冷水反应 |
C.反应不十分强烈,产生的气体可以在空气中燃烧 |
|
4.镁带与2mol.L-1的盐酸反应 |
D.剧烈反应,产生可燃性气体 |
|
5.铝条与2 mol.L-1的盐酸反应 |
E.生成白色胶状沉淀,既而沉淀消失 |
|
6.向AlCl3溶液滴加NaOH溶液至过量 |
F.生成淡黄色沉淀 |
请你帮助该同学整理并完成实验报告
(1)实验目的: ;
(2)实验用品:仪器:① ② ③ ④ ⑤镊子 ⑥小刀 ⑦玻璃片 ⑧砂纸 ⑨试管夹
药品:钠、镁带、铝条、2 mol.L-1的盐酸、新制的氯水、Na2S溶液、 AlCl3溶液、NaOH溶液等。
(3)实验内容:(填写与实验方案相对应的实验现象)
1 2 3 4 5 6 (用A-F表示);
写出③的离子方程式 ;
(4)实验结论: ;
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com