
科目: 来源:2013届江苏省高二第二学期期中考试化学试卷(解析版) 题型:选择题
一种新燃料电池,一极通入空气,另一极通入丁烷气体;电解质是掺杂氧化钇(Y2O3)的氧化锆(ZrO2)晶体,在熔融状态下能传导O2-。下列对该燃料说法正确的是
A.在熔融电解质中,O2-由负极移向正极
B.电池的总反应是:2C4H10 + 13O2 → 8CO2 + 10H2O
C.通入空气的一极是正极,电极反应为:O2 + 4e- = 2O2-
D.通入丁烷的一极是正极,电极反应为:C4H10 + 26e- + 13O2 = 4CO2 + 5H2O
查看答案和解析>>
科目: 来源:2013届江苏省高二第二学期期中考试化学试卷(解析版) 题型:选择题
某同学设计了一种电解法制取Fe(OH)2的实验装置(如图)。通电后,溶液中产生白色沉淀,且较长时间不变色。下列说法中正确的是
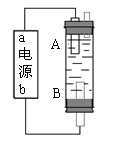
A.电源中“a”为负极,“b”为正极
B. 电解池中的电解液不可以是NaCl溶液
C.B电极发生的反应:2H2O+2e-=H2↑+2OH-
D.A.B两端都必须使用铁作电极
查看答案和解析>>
科目: 来源:2013届江苏省高二第二学期期中考试化学试卷(解析版) 题型:选择题
下列说法正确的是
A.电解饱和食盐水时,阳极的电极反应式为:2Cl--2e-= Cl2 ↑
B.氢氧燃料电池的负极反应式:O2 + 2H2O + 4e- == 4OH-
C.粗铜精炼时,与电源正极相连的是纯铜
D.钢铁发生电化腐蚀的正极反应式:Fe-2e- == Fe2+
查看答案和解析>>
科目: 来源:2013届江苏省高二第二学期期中考试化学试卷(解析版) 题型:选择题
可逆反应2NO2 2NO+O2,在恒容密闭容器中反应,达到平衡状态的标志是
2NO+O2,在恒容密闭容器中反应,达到平衡状态的标志是
①单位时间内生成n molO2的同时生成2n molNO2
②单位时间内生成n molO2 的同时,生成2n mol NO
③NO2.NO.O2 的反应速率的比为2 : 2 : 1的状态
④混合气体的颜色不再改变的状态
⑤混合气体的密度不再改变的状态
⑥ 混合气体的平均相对分子质量不再改变的状态
A.①④⑥ B.②③⑤ C.①③④ D.①②③④⑤⑥
查看答案和解析>>
科目: 来源:2013届江苏省高二第二学期期中考试化学试卷(解析版) 题型:选择题
一定量的盐酸跟过量的铁粉反应时,为了减缓反应速率,且不影响生成氢气的总量,可向盐酸中加入适量的
A.NaOH固体 B.K2SO4溶液 C.CuSO4固体 D.CH3COONa固体
查看答案和解析>>
科目: 来源:2013届江苏省高二第二学期期中考试化学试卷(解析版) 题型:选择题
将质量相等的铜片和铂片插入硫酸铜溶液中,铜片与电源正极相连铂片与电源负极相连,以电流强度1A通电10min,然后反接电源,以电流强度2A继续通电10min。下列表示铜电极.铂电极.电解池中产生气体的质量和电解时间的关系图正确的是

查看答案和解析>>
科目: 来源:2013届江苏省高二第二学期期中考试化学试卷(解析版) 题型:填空题
(12分)某研究性学习小组,为了探究电极与原电池的电解质之间关系,设计了下列实验方案:用铝片、铜片、镁片作电极,分别与下列溶液构成原电池,并接电流表。
(1)若电解质溶液为0.5mol/L硫酸,电极为铜片和铝片,则电流计指针偏向 (填“铝”或“铜”)。铝片上的电极的反应式为 ;
(2)若用浓硝酸作电解质溶液,电极为铜片和铝片,则电流计指针偏向 (填“铝”或“铜”),铝片为 极(填“正”或“负”)。铜极上电极反应式为: ,正极上发生的电极反应式为 ;
(3)若电解质溶液为0.5mol/L氢氧化钠溶液,电极为镁片和铝片,则正极发生的电极反应为 。
通过上述实验探究,你受到的启示是 。
查看答案和解析>>
科目: 来源:2013届江苏省高二第二学期期中考试化学试卷(解析版) 题型:填空题
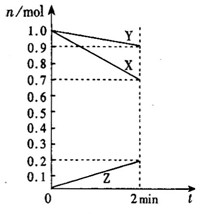
(10分)(1)(4分)某温度时,在2 L容器中,X、Y、Z三种物质的物质的 量随时间变化曲线如图所示。由图中数据分析,该反应的 化学方程式为:____________________________。反应开始至2 min,Z的平均反应速率为 __________。
(2)(6分)取a mol A和b
mol B置于V L容器中,发生可逆反应:aA(g)+bB(g)
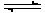 cC(g)+dD(g),1 min后,测得容器内A的浓度为x
mol·L-1,这时B的浓度为: ;C的浓度为: 。在这段时间内反应速率若以物质A的浓度变化来表示,应为__________。
cC(g)+dD(g),1 min后,测得容器内A的浓度为x
mol·L-1,这时B的浓度为: ;C的浓度为: 。在这段时间内反应速率若以物质A的浓度变化来表示,应为__________。
查看答案和解析>>
科目: 来源:2013届江苏省高二第二学期期中考试化学试卷(解析版) 题型:填空题
(12分)火箭推进器中盛有强还原剂液态肼(N2H4)和强氧化剂液态双氧水。当把0.4mol液态肼和0.8mol H2O2混合反应,生成氮气和水蒸气,放出256.7kJ的热量(相当于25℃、101 kPa下测得的热量)。
(1)反应的热化学方程式为 。
(2)又已知H2O(l)=H2O(g) ΔH=+44kJ/mol。则16g液态肼与液态双氧水反应生成液态水时放出的热量是 kJ。
(3)此反应用于火箭推进,除释放大量热和快速产生大量气体外,还有一个很大的优点是
查看答案和解析>>
科目: 来源:2013届江苏省高二第二学期期中考试化学试卷(解析版) 题型:实验题
(14分)铁生锈是比较常见的现象,某实验小组,为研究铁生锈的条件,设计了以下快速.易行的方法:
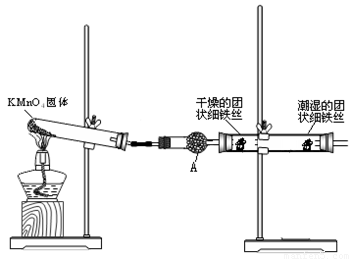
首先检查制氧气装置的气密性,然后按图连接好装置,点燃酒精灯给药品加热,持续3分钟左右,观察到的实验现象为:①直形管中用蒸馏水浸过的光亮铁丝表面颜色变得灰暗,发生锈蚀;②直形管中干燥的铁丝表面依然光亮,没有发生锈蚀;③中潮湿的铁丝依然光亮。
 试回答以下问题:
试回答以下问题:
(1)由于与接触的介质不同,金属腐蚀分成不同类型,本实验中铁生锈属于___________。
能表示其原理的反应方程式为_____________________________________
(2)仪器A的名称为______________,其中装的药品可以是_____ __________,其作用是___________________________________________
(3)由实验可知,该类铁生锈的条件为_______________________________________。决定铁生锈快慢的一个重要因素是_____________________________________________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com