
科目: 来源:2013届广东省高二下学期期末考试理综化学卷(解析版) 题型:选择题
在2L密闭容器内,某气体反应物在2s内由8mol变为7.2mol,则该反应的平均反应速率为 ( )
A.0.4mol/(L·s) B.0.3mol/(L·s) C.0.2mol/(L·s) D.0.1mol/(L·s)
查看答案和解析>>
科目: 来源:2013届广东省高二下学期期末考试理综化学卷(解析版) 题型:选择题
设C+CO2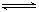 2CO-Q1(吸热反应) 反应速率为 u1, N2+3H2
2CO-Q1(吸热反应) 反应速率为 u1, N2+3H2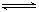 2NH3+Q2(放热反应)反应速率为 u2,对于上述反应,当温度升高时,u1和u2的变化情况为
2NH3+Q2(放热反应)反应速率为 u2,对于上述反应,当温度升高时,u1和u2的变化情况为
A.同时增大 B.同时减小 C.增大,减小 D.减小,增大
查看答案和解析>>
科目: 来源:2013届广东省高二下学期期末考试理综化学卷(解析版) 题型:选择题
可以充分说明反应P(g)+Q(g) R(g)+S(g)在恒温下已达到平衡
R(g)+S(g)在恒温下已达到平衡
A.反应容器内的P、Q、R、S的浓度不随时间改变
B.反应容器内P、Q、R、S四者共存
C.P的生成速率和S的生成速率相等
D.反应容器内的气体总物质的量不随时间变化
查看答案和解析>>
科目: 来源:2013届广东省高二下学期期末考试理综化学卷(解析版) 题型:选择题
在一密闭容器中进行如下反应:2SO2(气)+O2(气) 2SO3(气),已知反应过程中某一时刻SO2、O2、SO3的浓度分别为0.2mol/L、0.1mol/L、0.2mol/L,当反应达平衡时,可能存在的数据是
2SO3(气),已知反应过程中某一时刻SO2、O2、SO3的浓度分别为0.2mol/L、0.1mol/L、0.2mol/L,当反应达平衡时,可能存在的数据是
A.SO2为0.4mol/L、O2为0.2mol/L B.SO2为0.25mol/L
C.SO2、SO3均为0.15mol/L D.SO3为0.25mol/L
查看答案和解析>>
科目: 来源:2013届广东省高二下学期期末考试理综化学卷(解析版) 题型:填空题
(16分)在一定体积的密闭容器中,进行如下化学反应:
CO2(g)+H2(g)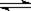 CO(g)+H2O(g),
CO(g)+H2O(g),
其化学平衡常数K和温度t的关系如下表:
|
t℃ |
700 |
800 |
830 |
1000 |
1200 |
|
K |
0.6 |
0.9 |
1.0 |
1.7 |
2.6 |
回答下列问题:
(1)该反应的化学平衡常数表达式为K= 。
(2)该反应为 反应(选填吸热、放热)。
(3)能判断该反应是否达到化学平衡状态的依据是
a.容器中压强不变 b.混合气体中 c(CO)不变
c.v正(H2)=v逆(H2O) d.c(CO2)=c(CO)
(4)某温度下,平衡浓度符合下式: c(CO2)·c(H2)=c(CO)·c(H2O),试判断此时的温度为 ℃。
查看答案和解析>>
科目: 来源:2013届广东省高二下学期期末考试理综化学卷(解析版) 题型:填空题
(16分)在一定条件下,可逆反应:mA+nB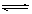 pC达到平衡,若:
pC达到平衡,若:
(1)A、B、C都是气体,减少压强,平衡向正反应方向移动,则m+n和p的关系是 。
(2)A、C是气体,增加B的量,平衡不移动,则B为 态。
(3)A、C是气体,而且m+n=p,增大压强可使平衡发生移动,则平衡移动的方向是 。
(4)加热后,可使C的质量增加,则正反应是 反应(放热或吸热)。
查看答案和解析>>
科目: 来源:2013届广东省高二下学期期末考试理综化学卷(解析版) 题型:选择题
(1)反应A(g)+B(s) C(g);△H<0,在其他条件不变时,改变其中一个条件,则生成C的速率:
C(g);△H<0,在其他条件不变时,改变其中一个条件,则生成C的速率:
①升温___ ;② 增大压强____ ; ③增大容器容积____ ;
④ 加入A___ ; ⑤ 加入B____ ; ⑥ 加正催化剂____ 。
(2)在25℃、101kPa下,1g甲烷燃烧生成CO2和液态水时放热55.6kJ。则表示甲烷燃烧热的热化学方程式为___________________________________________。
(3)北京奥运会“祥云”火炬燃料是丙烷(C3H8),亚特兰大奥运会火炬燃料是丙烯(C3H6),丙烷脱氢可得丙烯。
已知:C3H8(g) CH4(g)+HC
CH4(g)+HC CH(g)+H2(g) △H1=156.6 kJ·mol-1
CH(g)+H2(g) △H1=156.6 kJ·mol-1
CH3CH CH2(g)
CH2(g) CH4(g)+HC
CH4(g)+HC CH(g
) △H2=32.4 kJ·mol-1
CH(g
) △H2=32.4 kJ·mol-1
则相同条件下,反应C3H8(g) CH3CH
CH3CH CH2(g)+H2(g) 的△H=
kJ·mol-1。
CH2(g)+H2(g) 的△H=
kJ·mol-1。
(4)下表中的数据表示破坏1 mol化学键需消耗的能量(即键能,单位为kJ·mol-1):
|
化学键 |
C—H |
C—F |
H—F |
F—F |
|
键能 |
414 |
489 |
565 |
158 |
根据键能数据计算以下反应的反应热△H:
CH4(g)+4F2(g)﹦CF4(g)+4HF(g) △H=______________________
查看答案和解析>>
科目: 来源:2013届广东省高二下学期期末考试理综化学卷(解析版) 题型:简答题
(16分)苯乙烯(C6H5CH=CH2)是生产各种塑料的重要单体,其制备原理是:
C6H5C2H5(g) C6H5CH=CH2(g)+H2 (g) △H=+125kJ·mol-1
C6H5CH=CH2(g)+H2 (g) △H=+125kJ·mol-1
(1)该反应的平衡常数表达式为K= __ _____________ 。随着温度的升高,K值________(填“增大”、“减小”或“不变”,下同)。
(2)实际生产中常以高温水蒸气作为反应体系的稀释剂(稀释剂不参加反应)。C6H5C2H5的平衡转化率与水蒸气的用量、体系总压强关系如下图。

①由上图可得出:
结论一:其他条件不变,水蒸气的用量越大,平衡转化率越______;
结论二:__________________________________________________。
②加入稀释剂能影响C6H5C2H5平衡转化率的原因是:_______________________。
(3)某些工艺中,在反应的中途加入O2和特定的催化剂,有利于提高C6H5C2H5的平衡转化率。试解释其原因:_______________________________________________。
查看答案和解析>>
科目: 来源:2014届广东省高一6月月考理科综合化学试卷(解析版) 题型:选择题
下列关于甲烷及烷烃的说法中错误的是( )
A.甲烷和丙烷互为同系物
B.光照条件下,甲烷与Cl2的反应属于取代反应
C.甲烷能使酸性高锰酸钾溶液褪色
D.烷烃的通式为CnH2n+2
查看答案和解析>>
科目: 来源:2014届广东省高一6月月考理科综合化学试卷(解析版) 题型:选择题
设NA为阿伏加德罗常数,下列说法正确的是( )
A.1 mol Cl2与足量Fe反应,转移的电子数为3NA
B. 1mol·L-1 NaCl溶液含有NA个Na+
C.常温常压下,22.4L CO2中含有NA个CO2分子
D. 在18g 18O2中含有NA个氧原子
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com