
科目: 来源:2013届吉林省高二下学期期末考试化学试卷(解析版) 题型:填空题
(1)、熔点沸点HF HI;原因:
(2)、各种含氧酸HClO、HClO3、H2SO3、HClO4的酸性由强到弱排列为
(3)、下列4种物质熔点沸点由高到低排列为________ (填序号)
①金刚石(C—C)②锗(Ge—Ge)
③晶体硅(Si—Si)④金刚砂(Si—C)
(4)晶体具有规则的几何外形,晶体中最基本的重复单元称之为晶胞。NaCl晶体结构如图所示。

晶体中每个Na+同时吸引着______个Cl-,由这些 Cl-构成的几何构型为 晶体中在每个Cl-周围与它最接近且距离相 等的Cl-共有________个。
(5)某元素的激发态原子的电子排布式为1s 2s
2s 2p
2p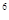 3s
3s 3p
3p 4s
4s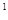 ,则该元素基态原子的电子排布式为
;其最高价氧化物对应的水化物的化学式是
,则该元素基态原子的电子排布式为
;其最高价氧化物对应的水化物的化学式是
(6)某元素原子的价电子构型为3d104S2,它属于第 周期,是 族, 区元素,元素符号是 。该原子核外有 个能级,电子云的形状有 种
查看答案和解析>>
科目: 来源:2013届吉林省高二下学期期末考试化学试卷(解析版) 题型:填空题
已知Ti3+可形成配位数为6的配合物。现有含钛的两种颜色的晶体,一种为紫色,另一种为绿色,但相关实验证明,两种晶体的组成皆为TiCl3·6H2O。为测定这两种晶体的化学式,设计了如下实验:
a.分别取等质量的两种配合物晶体的样品配成待测溶液;
b.分别往待测溶液中滴入AgNO3溶液,均产生白色沉淀;
c.沉淀完全后分别过滤得两份沉淀,经洗涤干燥后称量,发现原绿色晶体的水溶液与AgNO3溶液反应得到的白色沉淀质量为紫色晶体的水溶液反应得到沉淀质量的。则绿色晶体配合物的化学式为 。
查看答案和解析>>
科目: 来源:2013届吉林省高二下学期期末考试化学试卷(解析版) 题型:简答题
溴乙烷在不同溶剂中与NaOH发生不同类型的反应,生成不同的反应产物。某同学依据溴乙烷的性质,用下图实验装置(铁架台、酒精灯略)验证取代反应和消去反应的产物,请你一起参与探究。
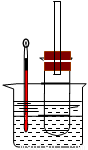
实验操作Ⅰ:在试管中加入5 mL 1 mol/L NaOH溶液和5 mL 溴乙烷,振荡。
实验操作II:将试管如图固定后,水浴加热。
(1)用水浴加热而不直接用酒精灯加热的原因是 _________________。
(2)观察到__________________________现象时,表明溴乙烷与NaOH溶液已完全反应。
(3)鉴定生成物中乙醇的结构,可用的波谱是____________。
(4)为证明溴乙烷在NaOH乙醇溶液中发生的是消去反应,在你设计的实验方案中,需要检验的是______________________,检验的方法是
(需说明:所用的试剂、简单的实验操作及预测产生的实验现象)。
查看答案和解析>>
科目: 来源:2013届吉林省高二下学期期末考试化学试卷(解析版) 题型:填空题
I、下表所列物质(括号内为少量杂质),在B中选择试剂,在C中选择操作的方法。填表(填入序号):
B:(1)NaCl细颗粒;(2)NaOH溶液;(3)水;(4)CaO;(5)饱和Na2CO3;(6)溴水;(7)KMnO4溶液。
C:(1)变性;(2)盐析;(3)蒸馏;(4)分液;(5)结晶;(6)洗气。
|
物质 |
加入试剂 |
操作方法 |
|
①苯(苯甲酸) |
|
|
|
②乙酸乙酯(乙醇) |
|
|
II、1 mol 与足量的NaOH溶液充分反应,消耗
与足量的NaOH溶液充分反应,消耗
NaOH的物质的量为 mol
查看答案和解析>>
科目: 来源:2013届吉林省高二下学期期末考试化学试卷(解析版) 题型:填空题
【 物质结构与性质 】(15分)
(1)已知X、Y、Z为同一短周期的三种元素,其原子的部分电离能(kJ/mol)如下表所示:
|
|
X |
Y |
Z |
|
I1 |
496 |
738 |
577 |
|
I2 |
4562 |
1451 |
1817 |
|
I3 |
6912 |
7733 |
2754 |
|
|
9540 |
10540 |
11578 |
①三种元素电负性大小关系为_______________
②写出Y原子的电子排布式_____________ Y的第一电离能大于Z的第一电离能的原因_______________________
③X晶体采用下列_________(填字母) 堆积方式。




A B C D
(2)N2O的等电子体为:①分子______________,②阴离子______________;由此可知N2O的中心原子的杂化类型为_____________。根据价层电子对互斥模型确定NO2的分子构型为:_____________________________________。
(3)已知铜能形成多种化合物,如硫酸铜的结构如下图所示,

请在图中标出水合铜离子中的配位键.
查看答案和解析>>
科目: 来源:2014届吉林省长春市高一下学期期末考试化学试卷(解析版) 题型:选择题
对于化学反应进行方向的确定,下列说法中正确的是 ( )
A. 温度、压强一定时,放热且熵减小的反应一定能自发进行
B. 温度、压强一定时,焓因素和熵因素共同决定一个化学反应的方向
C. 反应焓变是决定反应能否进行的唯一因素
D. 固体的溶解过程与熵变无关
查看答案和解析>>
科目: 来源:2014届吉林省长春市高一下学期期末考试化学试卷(解析版) 题型:选择题
升高温度,下列数据不一定增大的是( )
A. 化学平衡常数K
B. 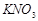 的溶解度s
的溶解度s
C. 化学反应速率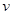 D. 水的离子积常数Kw
D. 水的离子积常数Kw
查看答案和解析>>
科目: 来源:2014届吉林省长春市高一下学期期末考试化学试卷(解析版) 题型:选择题
下列化学用语中正确的是( )
A.核内有8个中子的碳原子为 C
B.HClO的结构式为 H—O—Cl
C. 0.1mol/L的氢硫酸电离方程式为 H2S 2H++S2-
2H++S2-
D.CaCl2的电子式为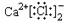
查看答案和解析>>
科目: 来源:2014届吉林省长春市高一下学期期末考试化学试卷(解析版) 题型:选择题
下列说法错误的是( )
A.钢铁发生析氢腐蚀时,负极电极反应是Fe-2e-=Fe2+
B.镀铜铁制品镀层受损后,铁制品比受损前更容易生锈
C.将pH=4的盐酸和醋酸稀释成pH=5的溶液,盐酸所需加入的水多
D.一定温度下,反应MgCl2(l)=Mg(l)+ Cl2(g)的△H>0 △S>0
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com