
科目: 来源:2011-2012年浙江宁波万里国际中学高三第一学期期中考试化学试卷(解析版) 题型:选择题
有一铁的氧化物样品,用5 mol/L的盐酸140mL恰好完全溶解,所得溶液还能吸收标况下0.56L Cl2,使亚铁离子全部变成Fe3+,则该氧化物可能的化学式为
A.Fe2O3 B.Fe3O4 C.Fe4O3 D.Fe5O7
查看答案和解析>>
科目: 来源:2011-2012年浙江宁波万里国际中学高三第一学期期中考试化学试卷(解析版) 题型:填空题
(12分)综合利用海水可以制备食盐、纯碱、金属镁、溴等物质,其流程如下图所示:
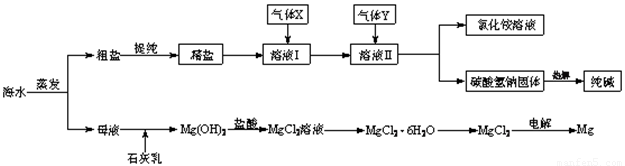
(1)粗盐中含有硫酸钠、氯化镁、氯化钙等可溶性杂质,为除去这些杂质而得精盐,进行如下操作:①溶解;②加过量的BaCl2溶液;③加过量的NaOH溶液;④加过量的Na2CO3溶液;⑤ ;⑥加适量的盐酸;⑦ 。
(2)溶液Ⅱ中发生反应的化学方程式是: 。
(3)Mg(OH)2沉淀中因混有Ca(OH)2,可选用___ ___ 溶液进行洗涤以除之。
(4)高温灼烧六水合氯化镁晶体(MgCl2·6H2O)所得固体是氧化镁,试写出该反应的化学方程式________ __ 。
(5)若在母液中通入氯气可提取海水中的溴,反应的离子方程式为:_____ _______。
查看答案和解析>>
科目: 来源:2011-2012年浙江宁波万里国际中学高三第一学期期中考试化学试卷(解析版) 题型:填空题
(14分)下图中,A、B、C、D、E是单质,G、H、I、F是B、C、D、E分别和A形成的二元化合物。已知:①反应C+G B+H能放出大量的热,该反应曾应用于铁轨的焊接;②I是一种常见的温室气体,它和E可以发生反应:2E+I
B+H能放出大量的热,该反应曾应用于铁轨的焊接;②I是一种常见的温室气体,它和E可以发生反应:2E+I 2F+D,F中E元素的质量分数为60%。
2F+D,F中E元素的质量分数为60%。
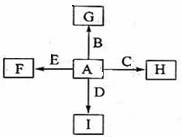
回答问题:
⑴①中反应的化学方程式为 ;
⑵化合物I的电子式为 ,它的空间结构是 ;
⑶将G溶于盐酸,得到的溶液加入一定量的铜粉,写出离子方程式:
⑷C与过量NaOH溶液反应的离子方程式为 ,反应后溶于与过量化合物I反应的离子方程式为 ;
⑸E在I中燃烧观察到的现象是 。
查看答案和解析>>
科目: 来源:2011-2012年浙江宁波万里国际中学高三第一学期期中考试化学试卷(解析版) 题型:实验题
(12分)碱式碳酸镁密度小,是橡胶制品的优良填料。可用复盐MgCO3·(NH4)2CO3·H2O作原料制备。取一定量的含镁复盐放入三颈烧瓶中,并将三颈烧瓶放在恒温水浴锅中加热(如图所示),按一定的液固比加入蒸馏水,开启搅拌器同时加入预定的氨水,待温度到达 40℃时开始热解,此时滴加卤水(氯化镁溶液)并继续滴入氨水,保持10分钟,一段时间后过滤洗涤,滤出的固体在 120℃干燥得到碱式碳酸镁产品。
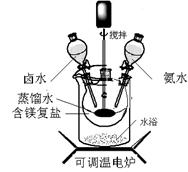
(1)①搅拌的目的是 ,②选择水浴加热方式,其优点是: 。
(2) 40℃复盐开始热解生成MgCO3·3H2O,该反应的化学方程式为: 。
(3)40℃时,开始滴加卤水的目的是
(4)碱式碳酸镁产品中镁的质量分数(ω(Mg)%)越高,产品质量越好,氯的质量分数越高,产品质量越差。分析Cl-含量采用滴定法,先精确称取一定量产品用适量硝酸溶解,经稀释等步骤最终配得一定体积的溶液。
测定实验中除用到天平、烧杯、玻璃棒、锥形瓶、滴定管外,还用到的玻璃仪器有: 。
(5)若已知制得的碱式碳酸镁的质量ag,要确定其组成(不考虑微量杂质),还必需的数据有: 。
①充分灼烧后,剩余固体的质量 ②灼烧时,测算得的二氧化碳的体积(已换算成标准状况) ③灼烧时的温度和时间 ④碱式碳酸镁的密度
查看答案和解析>>
科目: 来源:2011-2012年浙江宁波万里国际中学高三第一学期期中考试化学试卷(解析版) 题型:填空题
(12分) 高铁酸盐在能源、环保等方面有着广泛的用途。湿法、干法制备高铁酸盐的原理如下表所示。
湿法:强碱性介质中,Fe(NO3)3与NaClO反应生成紫红色高铁酸盐溶液
干法:Fe2O3、KNO3、KOH混合加热共熔生成紫红色高铁酸盐和KNO2等产物
(1)工业上用湿法制备高铁酸钾(K2FeO4)的流程如下图所示:

①反应I的化学方程式为 。
②反应II的离子方程式为 。
③加入饱和KOH溶液的目的是 。
(2)高铁酸钾是一种理想的水处理剂,其处理水的原理为 ; ______ ____。
(3)干法制备K2FeO4的反应中,氧化剂与还原剂的物质的量之比为 。
查看答案和解析>>
科目: 来源:2011-2012年浙江宁波万里国际中学高二上学期期中考试文科化学试卷(解析版) 题型:选择题
当光束通过豆浆时,可观察到丁达尔效应,表明豆浆是
A.胶体 B.溶液 C. 悬浊液 D.乳浊液
查看答案和解析>>
科目: 来源:2011-2012年浙江宁波万里国际中学高二上学期期中考试文科化学试卷(解析版) 题型:选择题
欲配制浓度为1.00mol·L-1的氯化钠溶液100mL,用不到的仪器是
A.容量瓶 B.分液漏斗 C.玻璃棒 D.烧杯
查看答案和解析>>
科目: 来源:2011-2012年浙江宁波万里国际中学高二上学期期中考试文科化学试卷(解析版) 题型:选择题
下列金属元素的单质中还原性最强的是
A.K B.Na C.Al D.Mg
查看答案和解析>>
科目: 来源:2011-2012年浙江宁波万里国际中学高二上学期期中考试文科化学试卷(解析版) 题型:选择题
下列物质属于离子化合物的是
A.HCl B.NH3·H2O C.(NH4)2SO4 D.CH3COOH
查看答案和解析>>
科目: 来源:2011-2012年浙江宁波万里国际中学高二上学期期中考试文科化学试卷(解析版) 题型:选择题
下列物质与水反应可生成强电解质的是
A.Na2O2 B.SO2 C.CO2 D.NH3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com