
科目: 来源:2014届江苏省扬州市高一下学期期中考试化学试卷(解析版) 题型:填空题
(9分)某研究性学习小组利用废铜制取CuSO4:
(1) 甲学生进行了下列实验:取含6.4g铜的废铜和10ml 18ml·L-1浓硫酸放在圆底烧瓶中共热,起到反应完毕,最后发现烧瓶中还有铜片剩余。他根据自己所学的化学知识,认为烧瓶中还有较多的硫酸剩余。你认为他的判断是否正确 ,其理由是:
。
 写出相关的化学方程式:
。
写出相关的化学方程式:
。
(2) 乙同学认为甲设计的实验方案不好,他自己设计的思路是:2Cu+O2==2CuO;CuO+H2SO4
==CuSO4+H2O。对比甲的方案,乙同学的优点是:
。
(3) 丙同学采用向含有废铜屑的热的稀H2SO4中,不断通入空气也能制备CuSO4,请写出相关的化学方程式: 。
查看答案和解析>>
科目: 来源:2014届江苏省扬州市高一下学期期中考试化学试卷(解析版) 题型:实验题
(11分) 某校课外活动小组为了探究铜与稀硝酸反应产生的气体主要是NO而设计了下列实验,装置如图所示(加热装置和固定装置均已略去)。图中K为止水夹(处于关闭状态),F是一半空的注射器。

请回答有关问题:
(1) 设计装置A的目的是 ;
为达到此目的,应进行的操作是打开K,且打开分液漏斗活塞,当装置C中产生
时,关闭K。
(2) 在完成(1)中的“操作”后,将装置B中铜丝插入稀硝酸,并微热之,观察到装置B中的
现象是 ;
B中反应的离子方程式为: 。
(3) 装置E和F的作用是 ;为实现此作用,其操作方法是 。
(4) 装置D的作用是吸收多余的氮氧化物,防止污染空气,兼有 的功能。
查看答案和解析>>
科目: 来源:2014届江苏省扬州市高一下学期期中考试化学试卷(解析版) 题型:计算题
(8分)若将32.00g Cu与200 mL一定浓度的硝酸反应,铜完全溶解产生的NO和NO2混合气体在标准状况下的体积为11.2 L。请回答:
(1)NO的体积为 L,NO2的体积为 L。?
(2)产生的气体全部释放后,向溶液中加入V mL a mol/L的NaOH溶液,恰好使溶液中的Cu2+全部转化为沉淀,则原硝酸溶液的浓度为 mol/L。
查看答案和解析>>
科目: 来源:2013届江苏省扬州市高二下学期期中考试化学试卷(解析版) 题型:选择题
江苏省“十二五”规划指出:“加强生态文明建设,发展循环经济,推广低碳技术,推动绿色增长”。下列做法有悖于生态文明建设的是
A.应用高效洁净的能源转换技术,提高能源的利用效率
B.废电池集中填埋
C.多用电子邮件、MSN、QQ等即时通讯工具,少用传真打印机
D.在火电厂推广碳收集和储存技术
查看答案和解析>>
科目: 来源:2013届江苏省扬州市高二下学期期中考试化学试卷(解析版) 题型:选择题
2008年10月8日,美籍华裔科学家钱永健获得2008年度诺贝尔化学奖。16岁时,他凭借一个金属易受硫氰酸盐腐蚀的调查项目,荣获“美国西屋科学天才奖”。下列叙述正确的是
A.金属腐蚀就是金属失去电子被还原的过程
B.将水库中的水闸(钢板)与外加直流电源的负极相连,正极连接一块废铁上可防止水闸被腐蚀
C.合金的熔点都高于它的成分金属,合金的耐腐蚀性也都比其成分金属强
D.铜板上的铁铆钉处在潮湿的空气中直接发生反应:Fe-3e- = Fe3+,继而形成铁锈
查看答案和解析>>
科目: 来源:2013届江苏省扬州市高二下学期期中考试化学试卷(解析版) 题型:选择题
下列反应中,属于氧化还原反应同时又是吸热反应的是
A.Ba(OH)2·8H2O与NH4Cl反应 B.铝与稀盐酸反应
C.灼热的炭与CO2反应 D.甲烷与O2的燃烧反应
查看答案和解析>>
科目: 来源:2013届江苏省扬州市高二下学期期中考试化学试卷(解析版) 题型:选择题
一定条件下,可逆反应N2
+3H2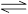 2NH3
△H<0 ,达到平衡后,当单独改变下述条件时,有关叙述错误的是
2NH3
△H<0 ,达到平衡后,当单独改变下述条件时,有关叙述错误的是
A.加催化剂,V正、V逆 都发生变化,且变化的倍数相等
B.加压,V正、V逆 都增大,且V正 增大的倍数大于V逆 增大的倍数
C.降温,V正、V逆 都减小,且V正 减小的倍数小于V逆 减小的倍数
D.增大氮气的浓度,V正、V逆 都增大,且V正 增大倍数大于V逆 增大倍数
查看答案和解析>>
科目: 来源:2013届江苏省扬州市高二下学期期中考试化学试卷(解析版) 题型:选择题
用铁片与稀硫酸反应制取氢气时,下列措施不能使氢气生成速率加大的是
A.加热 B.不用稀硫酸,改用98%浓硫酸
C.滴加少量硫酸铜溶液 D.不用铁片,改用铁粉
查看答案和解析>>
科目: 来源:2013届江苏省扬州市高二下学期期中考试化学试卷(解析版) 题型:选择题
如图1所示,U形管中装入含有紫色石蕊的Na2SO4试液,通直流电,一段时间后U形管内会形成三色“彩虹”的现象,它从左到右颜色的次序是
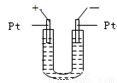
A.蓝、紫、红 B.红、蓝、紫 C.红、紫、蓝 D.蓝、红、紫
查看答案和解析>>
科目: 来源:2013届江苏省扬州市高二下学期期中考试化学试卷(解析版) 题型:选择题
下列描述违背化学原理的是
A.“冰,水为之,而寒于水”说明相同质量的水和冰,水的能量高
B.反应A(g)+3B(g) 2C(g)达平衡后,温度不变,增大压强,平衡正向移动,平衡常数K值增大
2C(g)达平衡后,温度不变,增大压强,平衡正向移动,平衡常数K值增大
C.SO2的催化氧化是一个放热的反应,升高温度,反应速率加快
D.电解饱和食盐水时,阳极的电极反应式为:2Cl--2e-= Cl2 ↑
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com