
科目: 来源:2011-2012年海南省高二下学期期中考试理科化学试卷(解析版) 题型:填空题
(16分) 接触法制硫酸工艺中,其主反应在450℃并有催化剂存在下进行:2SO2(g)+O2(g)? ?2SO3(g) ΔH=-190kJ·mol-1
?2SO3(g) ΔH=-190kJ·mol-1
(1)该热化学反应方程式的意义是_______________________________________________
升高温度上述反应平衡常数____(填“变大”“变小”或“不变”)。
(2)下列描述中能说明上述反应已达平衡的是________。
a.v(O2)正=2v(SO3)逆
b.容器中气体的平均相对分子质量不随时间而变化
c.容器中气体的密度不随时间而变化
d.容器中气体的分子总数不随时间而变化
(3)在一个固定容积为5 L的密闭容器中充入0.20 mol SO2和0.10 mol O2,半分钟后达到平衡,测得容器中含SO3 0.18 mol,则v(O2)=__________mol·L-1·min-1;若继续通入0.20 mol SO2和0.10 mol O2,则平衡________________移动(填“向正反应方向”、“向逆反应方向”或“不”),再次达到平衡后,________mol<n(SO3)<________mol。
查看答案和解析>>
科目: 来源:2011-2012年海南省高二下学期期中考试理科化学试卷(解析版) 题型:填空题
(15分)、对于弱酸,在一定温度下达到电离平衡时,各微粒的浓度存在一种定量的关系。若25℃时有HA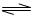 H++A―,则K=
H++A―,则K= 。式中:K为电离平衡常数,只与温度有关,c为各微粒的平衡浓度。下表是几种常见弱酸的电离平衡常数(25℃)。
。式中:K为电离平衡常数,只与温度有关,c为各微粒的平衡浓度。下表是几种常见弱酸的电离平衡常数(25℃)。

回答下列问题:
(1)当升高温度时,K值____(填“变大”“变小”或“不变”)。
(2)在温度相同时,各弱酸的K值不同,那么K值的大小与酸性的相对强弱有何关系? ____ ________。
(3)若把CH3COOH、H2CO3、HCO3-、H2S、HS-、H3PO4、
H2PO4-、HPO42-都看做是酸,其中酸性最强的是_ ,最弱的是_ __。
(4)同一多元弱酸的K1、K2、K3之间存在着数量上的规律,此规律是_____________,产生此规律的原因是_____________ ___。
(5) Na2CO3溶液呈_ _(填“酸性”“碱性”或“中性”),其原因(用离子方程式表示)是_ 。
(6)已知NaH2PO4溶液呈酸性,则该溶液中c(H3PO4)____c(HPO42-)(填“大于”或“小于” )。
查看答案和解析>>
科目: 来源:2011-2012年海南省高二下学期期中考试理科化学试卷(解析版) 题型:填空题
(10分)(1)体积相同、浓度均为0.2mol/L的盐酸和醋酸溶液分别加水稀释10倍,溶液的pH分别变成m和n,则m和n的关系是________,稀释后两溶液中和NaOH的能力_______。
(2)25℃时,pH=3的醋酸溶液与pH=11的氢氧化钠溶液等体积混合,混合后溶液呈_____(填“酸性”“碱性”或“中性”), 混合后溶液中离子浓度由大到小的顺序是_______________________。
(3)25℃时,将VamLpH=1的硫酸溶液与VbmLpH=12的氢氧化钾溶液混合恰好呈中性,则Va:Vb=________。
查看答案和解析>>
科目: 来源:2011-2012年海南省高二下学期期中考试理科化学试卷(解析版) 题型:填空题
(15分)在如图所示的装置中,若通入直流电5min时,铜电极质量增加2.16 g,试回答:
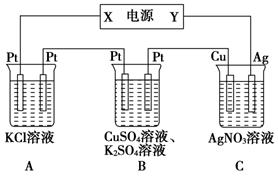
(1) 电源电极X为________极。
(2) pH变化:A________,B________,C________。(填“增大”、“减小”或“不变”)
(3) 通电5 min时,B中共收集224 mL气体(标准状况),溶液体积为200 mL。则通电前CuSO4溶液的物质的量浓度为________(设电解前后溶液体积无变化)。
(4) 若A中KCl溶液的体积也是200 mL,电解后,溶液的pH为________(设电解前后溶液体积无变化)。
查看答案和解析>>
科目: 来源:2011-2012年湖南岳阳等四县一中高二第六次质检化学试卷(解析版) 题型:选择题
下列物质中按照纯净物,混合物,电解质和非电解质的顺序排列的是
A.盐酸,水煤气,醋酸,干冰 B.冰醋酸,盐酸,硫酸钠,乙醇
C.苛性钠,石灰石,铁,硫酸钡 D.胆矾,漂白粉,氯化钾,氯气
查看答案和解析>>
科目: 来源:2011-2012年湖南岳阳等四县一中高二第六次质检化学试卷(解析版) 题型:选择题
某学生做完实验以后,采用以下方法分别清洗所用仪器:
(1)用稀硝酸清洗做过银镜反应的试管;
(2)用酒精清洗做过碘升华的烧杯;
(3)用浓盐酸清洗做过高锰酸钾分解实验的试管;
(4)用盐酸清洗长期存放过三氯化铁溶液的试剂瓶;
(5)用氢氧化钠溶液清洗盛过苯酚的试管。你认为他的操作:
A.(2)不对 B.(3)、(4)不对 C.(4)、(5)不对 D.全部正确
查看答案和解析>>
科目: 来源:2011-2012年湖南岳阳等四县一中高二第六次质检化学试卷(解析版) 题型:选择题
有一种气体在标准状况下体积是4.48升,质量是14.2g,则该气体的摩尔质量是
A.28.4 B.28.4g·mol-1 C.71 D.71g·mol-1
查看答案和解析>>
科目: 来源:2011-2012年湖南岳阳等四县一中高二第六次质检化学试卷(解析版) 题型:选择题
在一定温度下,反应A2(g)+B2(g)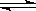 2AB(g)达到平衡的标志是
2AB(g)达到平衡的标志是
A.单位时间生成 n 摩尔的A2同时生成 n 摩尔的AB
B.容器内的总压不随时间变化
C.单位时间生成 2n 摩尔的AB同时生成 n 摩尔的B2
D.单位时间生成 n 摩尔的A2同时生成 n 摩尔的B2
查看答案和解析>>
科目: 来源:2011-2012年湖南岳阳等四县一中高二第六次质检化学试卷(解析版) 题型:选择题
99毫升0.1 mol/L盐酸和101毫升0.05 mol/L氢氧化钡溶液相混和后,溶液的pH值为
A.1.7 B.10.7 C.11 D.11.3
查看答案和解析>>
科目: 来源:2011-2012年湖南岳阳等四县一中高二第六次质检化学试卷(解析版) 题型:选择题
下列叙述中,可以说明金属甲的活动性比金属乙的活动性强的是
A.在氧化-还原反应中,甲原子失去的电子比乙原子失去的电子多
B.同价态的阳离子,甲比乙的氧化性强
C.甲能跟稀盐酸反应放出氢气而乙不能
D.甲原子的最外层电子数比乙原子的最外层电子数少
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com