
科目: 来源:2014届辽宁省高一下学期期中考试化学试卷(解析版) 题型:选择题
为说明氯比硫的非金属性强,下列事实可作为依据的是
A.HCl的水溶性强于H2S B.H2S 中的S 元素能被 Cl2氧化
C.氯的最高价为+7价 D.HClO的氧化性强于H2SO4
查看答案和解析>>
科目: 来源:2014届辽宁省高一下学期期中考试化学试卷(解析版) 题型:选择题
镁、锂在元素周期表中具有特殊的“对角线”位置关系,它们的性质相似。例如,它们的单质在过量氧气中燃烧时均只生成正常的氧化物等,有关锂的性质叙述正确的是( )
A.Li2SO4难溶于水 B.Li与水剧烈反应
C.LiOH是易溶于水,受热不分解的强碱 D.Li2CO3受热分解,生成Li2O和CO2
查看答案和解析>>
科目: 来源:2014届辽宁省高一下学期期中考试化学试卷(解析版) 题型:选择题
晶体硼是由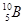 和
和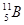 两种同位素构成的。已知5.4克晶体硼(B)全部氢化生成B2H6 (硼烷)气体时,可得标准状况下5.6L硼烷,则晶体硼中
两种同位素构成的。已知5.4克晶体硼(B)全部氢化生成B2H6 (硼烷)气体时,可得标准状况下5.6L硼烷,则晶体硼中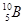 和
和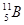 两种核素的原子个数比是
两种核素的原子个数比是
A.1:1 B.1:3 C.1:4 D.1:2
查看答案和解析>>
科目: 来源:2014届辽宁省高一下学期期中考试化学试卷(解析版) 题型:选择题
火箭推进器常以联氨(N2H4) 为燃料、过氧化氢为助燃剂。已知下列各物质反应的热化学方程式:N2H4(g)+O2(g)=N2(g)+2H2O(g) ΔH1=-533.23 kJ·mol-1
H2O(g)=H2O (l) DH2=–44 kJ·mol-1
2H2O2(l)=2H2O(l)+ O2(g) DH3=–196.4 kJ·mol-1
则联氨与过氧化氢反应的热化学方程式可表示为( )
A.N2H4(g)+2H2O2(l)= N2(g)+4H2O(l) ΔH=+817.63 kJ·mol-1
B.N2H4(g)+2H2O2(l)= N2(g)+4H2O(g) ΔH=-641.63 kJ·mol-1
C.N2H4(g)+2H2O2(l)= N2(g)+4H2O(l) ΔH=-641.63 kJ·mol-1
D.N2H4(g)+2H2O2(l)= N2(g)+4H2O(g) ΔH=-817.63 kJ·mol-1
查看答案和解析>>
科目: 来源:2014届辽宁省高一下学期期中考试化学试卷(解析版) 题型:选择题
一种新型燃料电池,一极通入空气,另一极通入甲烷气体;电解质是掺杂氧化钇(Y2O3)的氧化锆(ZrO2)晶体,在熔融状态下能传导O2-.下列对该燃料电池说法正确的是( )
A.在熔融电解质中,O2-由负极移向正极
B.在外电路,电流从甲烷所通电极流向空气所通电极
C.通入空气的一极是正极,电极反应为:O2-4e-=2O2-
D.通入甲烷的一极是负极,电极反应为: CH4-8e-+4O2-=CO2+2H2O
查看答案和解析>>
科目: 来源:2014届辽宁省高一下学期期中考试化学试卷(解析版) 题型:选择题
可逆反应N2+3H2 2NH3的正、逆反应速率可用各反应物或生成物浓度的变化来表示。下列各关系中能说明反应已达到平衡状态的是
2NH3的正、逆反应速率可用各反应物或生成物浓度的变化来表示。下列各关系中能说明反应已达到平衡状态的是
A、1个N≡N键断裂的同时,有3个H—H键断裂
B、N2、H2、NH3的分子数之比为1︰3︰2
C、反应体系中N2和NH3的物质的量之比不变
D、3v正(H2)=2v逆(NH3)
查看答案和解析>>
科目: 来源:2014届辽宁省高一下学期期中考试化学试卷(解析版) 题型:选择题
将2mol
C气体在2 L的容器中混合并在一定条件下发生如下反应:2C(气) 2A(气)+B(气)。若经2 s(秒)后测得C的浓度为0.6 mol·L-1,现有下列几种说法:
2A(气)+B(气)。若经2 s(秒)后测得C的浓度为0.6 mol·L-1,现有下列几种说法:
①用物质A表示的反应平均速率为0.3 mol·L-1·s-1 ②用物质B表示的反应的平均速率为0.1 mol·L-1·s-1③2 s时物质C的转化率为40% ④2 s时物质B的浓度为0.2 mol·L-1
其中正确的是( )
A. ①③ B. ①④ C. ②③ D. ②③④
查看答案和解析>>
科目: 来源:2014届辽宁省高一下学期期中考试化学试卷(解析版) 题型:选择题
可逆反应∶2NO2 2NO+O2在恒容密闭容器中反应,达到平衡状态的标志是
( )
2NO+O2在恒容密闭容器中反应,达到平衡状态的标志是
( )
A.单位时间内生成n molO2的同时生成2n molNO
B.用NO2、NO、O2 的物质的量浓度变化表示的反应速率的比为2 : 2 : 1的状态
C.混合气体的密度不再改变的状态
D.混合气体的平均相对分子质量不再改变的状态
查看答案和解析>>
科目: 来源:2014届辽宁省高一下学期期中考试化学试卷(解析版) 题型:选择题
在一定温度下,容器内某一反应中M.N的物质的量随反应时间变化的曲线如图,下列表述中正确的是

A.反应的化学方程式为: N 2M
2M
B.t2时,正逆反应速率相等,达到平衡
C.t3时,正反应速率大于逆反应速率
D.t1时,N的浓度是M浓度的2倍
查看答案和解析>>
科目: 来源:2014届辽宁省高一下学期期中考试化学试卷(解析版) 题型:实验题
(8分)用一定浓度的稀盐酸与稀NaOH溶液在左下图所示的装置中进行中和反应,通过测定反应过程中所放出的热量可计算中和热。已知强酸与强碱的中和热为57.3KJ/mol,水的比热容为4.2J/(g·℃),有关热量与比热容的计算公式:Q=m×c×△t(Q为热量,m为物质的质量,c为比热容,△t物质温度的变化值)
回答下列问题:
(1)从实验装置上看,图中尚缺少的一种玻璃用品是:
(2)将V1 mL 1.0 mol/L HCl溶液和V2 mL未知浓度的NaOH溶液混合均匀后测量并记录溶液温度,实验结果如图所示(实验中始终保持V1+V2=50 mL)。

下列叙述正确的是
A.做该实验时环境温度为22 ℃ B.该实验表明化学能可以转化为热能
C.NaOH溶液的浓度约是1.00 mol/L D.该实验表明有水生成的反应都是放热反应
(3)V1=30mL时HCl和NaOH恰好反应,根据题中所给数据算出的温度变化值约为
(保留整数,计算时可将稀溶液的密度及比热容看成与水近似相同,且溶液混合时体积变化忽略不计);而根据上图的温度变化可读出温度变化值约7 ℃;两者相比所测结果偏低,造成如此现象的原因有:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com