
科目: 来源:2011-2012学年江苏省南通市通州区高三4月查漏补缺专项检测化学试卷(解析版) 题型:选择题
某同学设计如下实验测量m g铜银合金样品中铜的质量分数:

下列说法中不正确的是
A.收集到的V L气体为 NO
B.过滤用到的玻璃仪器是:烧杯、漏斗、玻璃棒
C.操作Ⅱ应是洗涤
D.铜的质量分数为: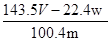 ×100%
×100%
查看答案和解析>>
科目: 来源:2011-2012学年江苏省南通市通州区高三4月查漏补缺专项检测化学试卷(解析版) 题型:选择题
下列图像表达正确的是

A.图①表示25℃时,用0.1mol·L-1盐酸滴定20mL 0.1mol·L-1NaOH溶液
B.图②表示常温下,等量锌粉与足量的等体积等浓度的盐酸反应
C.图③表示向CaCl2和盐酸的混合溶液中滴加Na2CO3溶液
D.图④表示向盐酸和醋酸混合溶液中滴入氨水
查看答案和解析>>
科目: 来源:2011-2012学年江苏省南通市通州区高三4月查漏补缺专项检测化学试卷(解析版) 题型:选择题
CPAE是蜂胶的主要活性成分,也可由咖啡酸合成

下列说法不正确的是
A.咖啡酸分子中所有原子可能处在同一个平面上
B.可用金属Na检测上述反应是否残留苯乙醇
C.1 mol 苯乙醇在O2中完全燃烧,需消耗10 mol O2
D.1 mol CPAE与足量的NaOH溶液反应,最多消耗3 mol NaOH
查看答案和解析>>
科目: 来源:2011-2012学年江苏省南通市通州区高三4月查漏补缺专项检测化学试卷(解析版) 题型:选择题
下列判断中,正确的是( )
A.30%和H2O2溶液中加入MnO2可制得O2,MnO2做氧化剂
B.SO2和CO2都属于酸性氧化物,Na2O和Al2O3都属于碱性氧化物[
C.在NH4Cl水溶液中,既存在水解平衡,又存在电离平衡
D.O2在放电条件下生成O3属于化学变化,煤干馏得到焦炭属于物理变化
查看答案和解析>>
科目: 来源:2011-2012学年江苏省南通市通州区高三4月查漏补缺专项检测化学试卷(解析版) 题型:选择题
图1是在金属锌板上贴上一张用某溶液浸湿的滤纸,图2是NaBH4/H2O2燃料电池,则下列说法正确的是
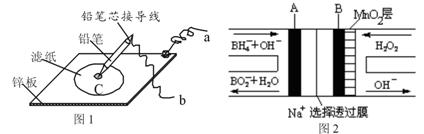
A.图2电池放电过程中,Na+从正极区向负极区迁移
B.图2电池负极区的电极反应为BH4-― 8e- + 8OH-=BO2- + 6H2O
C.若用硫酸钠和酚酞的混合溶液浸湿滤纸,用导线将a、b直接相连,则铅笔芯C点处出现红色
D.若用KI淀粉溶液浸湿滤纸,用导线将a、b与A、B电极相连,铅笔芯C点处出现蓝色,则b接的是A电极
查看答案和解析>>
科目: 来源:2011-2012学年江苏省南通市通州区高三4月查漏补缺专项检测化学试卷(解析版) 题型:选择题
常温下,下列各溶液的叙述中正确的是
A.pH=7的醋酸钠和醋酸混合液中:c(Na+)= c(CH3COO-)
B.0.1mol/L的醋酸的pH=a,0.01mol/L的醋酸的pH=b,则a+1>b
C.0.1mol/L的醋酸钠溶液20mL与0.1mol/L盐酸10mL混合后溶液显酸性
c (CH3COO-)>c (Cl-)>c (H+)>c (CH3COOH)
D.已知酸性HF>CH3COOH,pH相等的NaF与CH3COOK溶液中,
[c(Na+)-c(F一)]<[c(K+)-c(CH3COO一)]
查看答案和解析>>
科目: 来源:2011-2012学年江苏省南通市通州区高三4月查漏补缺专项检测化学试卷(解析版) 题型:选择题
如图所示,隔板I固定不动,活塞Ⅱ可自由移动,M、N两个容器中均发生反应:A(g) + 3B(g)  2C(g) ΔH=-192
kJ·mol-1。向M、N中,都通入x mol A和y mol B的混合气体,初始M、N容积相同,保持温度不变。下列说法正确的是
2C(g) ΔH=-192
kJ·mol-1。向M、N中,都通入x mol A和y mol B的混合气体,初始M、N容积相同,保持温度不变。下列说法正确的是
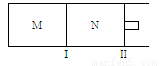
A.若平衡时A气体在两容器中的体积分数相等,则x一定等于y
B.若x∶y=1∶2,则平衡时,M中的转化率:A>B
C.若x∶y=1∶3,当M中放出热量172.8 kJ时,A的转化率为90%
D.若x=1.2,y=1,N中达到平衡时体积为2 L,含有C 0.4 mol,再通入0.36 mol A时,v(正)<v(逆)
查看答案和解析>>
科目: 来源:2011-2012学年江苏省南通市通州区高三4月查漏补缺专项检测化学试卷(解析版) 题型:实验题
(13分)实验室用下列方法测定某水样中O2的含量。

(1)实验原理
用如图所示装置,使溶解在水中的O2在碱性条件下将Mn2+氧化成MnO(OH)2,反应的离子方程式为 。
再用I-将生成的MnO(OH)2再还原为Mn2+,反应的离子方程式为: MnO(OH)2+2I—+4H+=Mn2++I2+3H2O。
然后用Na2S2O3 标准溶液滴定生成的I2,反应方程式为: I2+2Na2S2O3=2NaI+Na2S4O6。
(2)实验步骤
① 打开止水夹a 和b,从A 处向装置内鼓入过量N2,此操作的目的是 ;
② 用注射器抽取某水样20.00 mL从A 处注入锥形瓶;
③ 再分别从A 处注入含m mol NaOH溶液及过量的MnSO4 溶液;
④ 完成上述操作后,关闭a、b,将锥形瓶中溶液充分振荡;
⑤ 打开止水夹a、b,分别从A 处注人足量NaI溶液及含n mol H2SO4的硫酸溶液;
⑥ 重复④ 的操作。
⑦ 取下锥形瓶,向其中加入2~3滴 作指示剂;
⑧ 用0.005 mol · L—1Na2S2O3 滴定至终点。
(3)数据分析
①若滴定过程中消耗的Na2S2O3 标准溶液体积为3.90 mL,则此水样中氧(O2)的含量为 (单位:mg·L—1)。
②若未用Na2S2O3标准溶液润洗滴定管,则测得水样中O2的含量将 (填“偏大”、“偏小”或“不变”)。
③实验要求加入适量的H2SO4使溶液接近中性,其原因是 。
查看答案和解析>>
科目: 来源:2011-2012学年江苏省南通市通州区高三4月查漏补缺专项检测化学试卷(解析版) 题型:填空题
(15分)4-硫醚基喹唑啉类化合物是一种具有应用前景的抑菌药物,其合成路线如下:
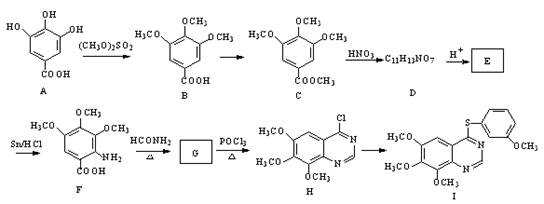
已知: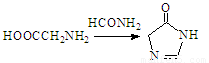
(1)A中含氧官能团的名称是 ;E→F的应类型为 。
(2) C的一种同分异构体X,X是苯的衍生物,苯环上有四个取代基,其中3个为甲氧基(-OCH3),在苯环上的位置与C相同,每摩X最多能与2 mol NaOH反应。X的结构简式为 。
(3)写出C→D的化学方程式 。
(4)物质G的结构简式为 。
(5)利用题给相关信息,以甲苯、HCONH2为原料,合成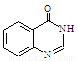 。合成过程中无机试剂任选;合成路线流程图示例为:
。合成过程中无机试剂任选;合成路线流程图示例为: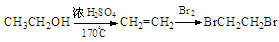
提示:
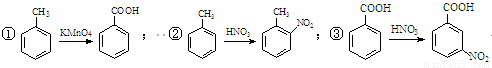
查看答案和解析>>
科目: 来源:2011-2012学年江苏省南通市通州区高三4月查漏补缺专项检测化学试卷(解析版) 题型:计算题
(12分)氯化硫酰(SO2Cl2)主要用作氯化剂。它是一种无色液体,熔点—54.1℃,沸点69.1℃,遇水生成硫酸和氯化氢。氯化硫酰可用干燥的二氧化硫和氯气在活性炭催化剂存在下反应制取:SO2(g)+Cl2(g) SO2Cl2(l)
△H=—97.3kJ/mol
SO2Cl2(l)
△H=—97.3kJ/mol
⑴为了提高上述反应中Cl2的平衡转化率,下列措施合理的是 (用编号填空)。
A.缩小容器体积 B.使用催化剂 C.增加SO2浓度 D.升高温度
(2)300℃时,体积为1 L的密闭容器中充入16.20 g SO2Cl2,达到平衡时容器中含SO2 7.616 g,则300℃时合成SO2Cl2反应的平衡常数为 。
(3)已知某温度下,已知Ksp(AgCl)=2.0×10-10,Ksp(Ag2SO4)=1.6×10-5,在SO2Cl2溶于水所得溶液中逐滴加入AgNO3稀溶液,当Ag+浓度为0.1mol/L时,浑浊液中Cl-浓度与SO42- 浓度之比为 。
⑷将(2)所得的平衡混合气溶于足量的BaCl2溶液中,计算最终生成沉淀的质量是多少(写出计算过程)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com