
科目: 来源:2011-2012年福建漳州芗城中学高二下学期期中考试理科化学试卷(解析版) 题型:选择题
下列说法错误的是( )
A.1.5g CH3+中含有的电子数为0.8NA B.Cu元素在元素周期表的ds区
C.s轨道呈圆形,p轨道呈哑铃形 D.DNA中的碱基互补配对是通过氢键来实现的
【解析】CH3+中含有的电子8,1.5g CH3+是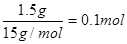 ,所以A正确。铜属于第IB,位于ds区,B正确。P轨道是纺锤形的,C是错误的。蛋白质含有氮元素,可以形成氢键,D正确。所以答案选C
,所以A正确。铜属于第IB,位于ds区,B正确。P轨道是纺锤形的,C是错误的。蛋白质含有氮元素,可以形成氢键,D正确。所以答案选C
查看答案和解析>>
科目: 来源:2011-2012年福建漳州芗城中学高二下学期期中考试理科化学试卷(解析版) 题型:选择题
下列说法中错误的是( )
A.根据对角线规则,铍和铝的性质具有相似性
B.P4和CH4都是正四面体分子且键角都为109o28ˊ
C.元素电负性越大的原子,吸引电子的能力越强
D.在H3O+和NH4+ 中都存在配位键
【解析】P4的键角是60°的,B不正确。所以答案选B。
查看答案和解析>>
科目: 来源:2011-2012年福建漳州芗城中学高二下学期期中考试理科化学试卷(解析版) 题型:选择题
根据键能数据估算CH4 (g)+4F2 (g) =CF4+4HF(g)的反应热ΔH为( )
|
化学键 |
C—H |
C—F |
H—F |
F—F |
|
键能/(kJ/mol) |
414 |
489 |
565 |
155[ |
A.–1940 kJ · mol-1 B.1940 kJ · mol-1 C.–485 kJ · mol-1 D.485 kJ · mol-1
【解析】反应热就是断键所吸收和能量和成键所放出的能量的差值。因此该反应的反应热△H为4×414 kJ/mol+4×155 kJ/mol-4×489 kJ/mol-4×565 kJ/mol=-1940 kJ/mol,所以正确的答案是A。
查看答案和解析>>
科目: 来源:2011-2012年福建漳州芗城中学高二下学期期中考试理科化学试卷(解析版) 题型:选择题
已知X、Y、Z三种元素组成的化合物是离子晶体,其晶胞如图所示,则下面表示该化合物的化学式正确的是( )

A.ZXY3 B.ZX2Y6 C.ZX4Y8 D.ZX8Y12
【解析】X原子位于立方体的8个顶点上,所以晶胞中含有的X是8×1/8=1。Y原子全部位于棱上,所以晶胞中含有的Y是12×1/4=3。Z全部位于中心,全部属于该晶胞,所以该化合物的化学式为ZXY3,选项A正确。答案是A。
查看答案和解析>>
科目: 来源:2011-2012年福建漳州芗城中学高二下学期期中考试理科化学试卷(解析版) 题型:选择题
用价层电子对互斥理论(VSEPR)预测H2S和COCl2的立体结构,两个结论都正确的是 ( )
A.直线形;三角锥形 B.V形;三角锥形
C.直线形;平面三角形 D.V形;平面三角形
【解析】H2S分子中中心原子的孤电子对数为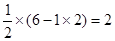 ,这说明H2S分子中中心原子4对电子对,其中2对是孤电子对,所以其结构是V型的。COCl2中中心原子的孤电子对数为
,这说明H2S分子中中心原子4对电子对,其中2对是孤电子对,所以其结构是V型的。COCl2中中心原子的孤电子对数为
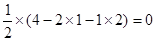 ,因此COCl2中的电子对数为3,是平面三角形结构。答案选D。
,因此COCl2中的电子对数为3,是平面三角形结构。答案选D。
查看答案和解析>>
科目: 来源:2011-2012年福建漳州芗城中学高二下学期期中考试理科化学试卷(解析版) 题型:选择题
已知氯化铝易溶于苯和乙醚,其熔点为190℃,则下列结论错误的是( )
A.氯化铝是电解质 B.固体氯化铝是分子晶体
C.可用电解熔融氯化铝的办法制取金属铝 D.氯化铝为非极性分子
【解析】根据氯化铝的物理性质可知,氯化铝是共价化合物,形成的晶体是分子晶体。苯和乙醚均是非极性分子,根据相似相溶原理知氯化铝也是非极性分子。氯化铝溶于水可以导电,但在熔融状态下不能导电,所以选项C是错误的,答案选C。
查看答案和解析>>
科目: 来源:2011-2012年福建漳州芗城中学高二下学期期中考试理科化学试卷(解析版) 题型:选择题
两种短周期元素组成的化合物中,原子个数比为1:3,若两种元素的原子序数分别为a和b,则a和b的关系可能是( )
① a=b+5 ② a+b=8 ③ a+b=30 ④ a=b+8
A.①②③④ B.②③④ C.②③ D.③④
【解析】本题可以采用排除法筛选。①可以是C2H6,②可以是NH3,③可以是AlCl3,④可以是SO3。所以正确的答案是A。
查看答案和解析>>
科目: 来源:2011-2012年福建漳州芗城中学高二下学期期中考试理科化学试卷(解析版) 题型:选择题
如图是元素周期表的一部分,关于元素X、Y、Z的叙述正确的是( )

①X的气态氢化物与Y的最高价氧化物对应的水化物能发生反应生成盐;② Z的单质常温下是液体,可与铁粉反应;③ Z的原子序数比Y大19;④Z所在的周期中含有32种元素。
A. ①②③④ B. ①②③ C.只有①④ D.只有③
【解析】考查元素周期表的结构。根据元素在周期表中的位置可知X是N、Y是S、Z是Br、R是He。氨气和硫酸反应生成硫酸铵,①正确。单质溴在常温下是液体和铁反应生成溴化铁,②正确。Br的原子序数是35,S的原子序数是16,二者相差19,③正确。Br是第四周期元素,该周期含有18种元素。所以正确的答案是B。
查看答案和解析>>
科目: 来源:2011-2012年福建漳州芗城中学高二下学期期中考试理科化学试卷(解析版) 题型:选择题
氯化二硫(S2Cl2)是广泛用于橡胶工业的硫化剂,其分子结构如下图所示。常温下S2Cl2是一种橙黄色的液体,遇水易水解,并产生能使品红褪色的气体。下列说法错误的是 ( )
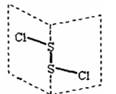
A.S2Cl2的结构式为Cl-S-S-Cl
B.S2Cl2为含有极性键和非极性键的非极性分子
C.S2Br2与S2Cl2结构相似,熔沸点:S2Br2>S2Cl2
D.S2Cl2与H2O反应的化学方程式可能为: 2S2Cl2+2H2O=SO2↑+3S↓+4HCl
【解析】根据氯化二硫的结构示意图可判断,硫和硫之间形成的是非极性键,硫和氯之间形成的是极性键,但氯化二硫不是直线型结构,因此属于极性分子,形成的晶体是分子晶体,所以A正确,B不正确。S2Br2与S2Cl2结构相似,所以S2Br2也是分子晶体,但S2Br2的相对分子质量比S2Cl2的大,因此C正确。能使品红褪色的气体是二氧化硫,而在S2Cl2中硫的化合价是+1价,所以S2Cl2和水的反应是氧化还原反应。由于二氧化硫是氧化产物,所以还应该有还原产物单质硫生成,孤选项D也正确。答案是B。
查看答案和解析>>
科目: 来源:2011-2012年福建漳州芗城中学高二下学期期中考试理科化学试卷(解析版) 题型:填空题
(17分)A、 B、C、D为四种元素,A原子的1S轨道为半充满;在元素周期表中,B的电负性最大;C2+的电子排布式和Ar相同;D的原子序数为24。
(1)判断元素:A 、B 、C 、D 。
(2)以上这四种元素中,属于d区的是______________________(填元素符号)。
(3)C在周期表中的位置为________周期________族。
(4)写出CB2的电子式 。
(5)元素D的化合物(DO2Cl2)在有机合成中可作氧化剂或氯化剂,能与许多有机物反应。请回答下列问题:
①与D同周期的所有元素的基态原子中最外层电子数与D原子相同的元素还有__________(填元素符号
②DO2Cl2常温下为深红色液体,能与CCl4、CS2等互溶,据此可判断DO2Cl2是__________(填“极性”或“非极性”)分子。
【解析】考查元素周期表的结构和核外电子的排布规律。1S轨道为半充满的是氢元素,即A是H。电负性最大的就是非金属性最强的,所以B是F。C2+的电子排布式和Ar相同,Ar的原子序数是18,所以C是Ca。原子序数为24的是Cr,则D是Cr。由于Cr最后填入的单质在d轨道上,所以Cr属于d区;CaF2是由离子键形成的离子化合物,其电子式为 ;因为半充满或全场满是稳定的,所以Cr的最外层电子是1,与之相等的还有K和Cu;CCl4、CS2是非极性分子,根据相似相溶原理可判断DO2Cl2也是非极性分子。
;因为半充满或全场满是稳定的,所以Cr的最外层电子是1,与之相等的还有K和Cu;CCl4、CS2是非极性分子,根据相似相溶原理可判断DO2Cl2也是非极性分子。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com