
科目: 来源:2011-2012学年江苏省高三3月双周练习(二)化学试卷(解析版) 题型:选择题
设NA为阿伏加德罗常数的值,下列叙述正确的是
A.含有NA个NO2、N2O4分子的混合气体降低温度,混合气体的分子数目小于NA
B.常温常压和光照条件下,33.6 LCl2与3.0g H2反应,生成的HCl分子数目为3NA
C.1.68 g Fe和足量水蒸气反应,转移的电子数目为0.09NA
D.一定条件下,1 mol N2和3 mol H2充分反应,生成物中含N—H键数目为6NA
查看答案和解析>>
科目: 来源:2011-2012学年江苏省高三3月双周练习(二)化学试卷(解析版) 题型:选择题
下列实验的解释或结论不正确的是
|
选项
|
实验
|
解释或结论
|
|
A
|
用激光笔照射水玻璃溶液,有丁达尔现象 |
SiO32-水解生成硅酸胶体 |
|
B |
在新制的氯水中加入碳酸钙粉末,充分搅拌 |
氯水中HClO的物质的量增加 |
|
C |
向包有Na2O2的脱脂棉滴少量水,脱脂棉燃烧 |
Na2O2与H2O反应放热并有O2生成 |
|
D |
向某溶液中加入稀盐酸,再加入硝酸钡溶液生 成白色沉淀 |
原溶液中一定存在SO42- |
查看答案和解析>>
科目: 来源:2011-2012学年江苏省高三3月双周练习(二)化学试卷(解析版) 题型:选择题
下列说法正确的是
A.在漂白粉中滴入70%的硫酸,立刻产生黄绿色气体,说明硫酸具有还原性
B.粗锌与稀硫酸反应比纯锌快,说明粗锌反应时形成了原电池
C.硬水含有Ca2+、Mg2+、HCO3-、SO42-,煮沸可以完全除去其中的Ca2+、Mg2+
D.pH相同的两种一元酸HA溶液和HB溶液与足量Zn反应,HA比HB反应速率快,说明HA酸性更强
查看答案和解析>>
科目: 来源:2011-2012学年江苏省高三3月双周练习(二)化学试卷(解析版) 题型:选择题
α,β,γ和δ四种生育三烯酚是构成维生素E的主要物质,下列叙述中不正确的是

A.α和δ两种生育三烯酚互为同系物,β和γ两种生育三烯酚互为同分异构体
B.四种生育三烯酚的结构中均不存在手性碳原子
C.四种生育三烯酚均能使三氯化铁溶液显紫色
D.1molα-生育三烯酚与溴的四氯化碳溶液发生反应,理论上最多可消耗3molBr2
查看答案和解析>>
科目: 来源:2011-2012学年江苏省高三3月双周练习(二)化学试卷(解析版) 题型:选择题
如下图所示,其中甲池的总反应式为:2CH3OH+3O2+4KOH=2K2CO3+6H2O

下列说法正确的是[
A.甲池是电能转化为化学能的装置,乙、丙池是化学能转化电能的装置
B.甲池通入CH3OH的电极反应为CH3OH-6e-+2H2O=2CO32-+8H+
C.反应一段时间后,向乙池中加入一定量Cu(OH)2固体,能使CuSO4溶液恢复到原浓度
D.甲池中消耗280 mL(标准状况下)O2,此时丙池中理论上最多产生1.45g固体
查看答案和解析>>
科目: 来源:2011-2012学年江苏省高三3月双周练习(二)化学试卷(解析版) 题型:选择题
下列溶液中有关物质的量浓度关系正确的是
A.pH=2的醋酸溶液与pH=12的NaOH溶液等体积混合:
c (Na+)>c (CH3COO-)>c(H+)>c(OH-)
B.向NH4HSO4溶液中滴加等物质的量的NaOH形成的溶液中:
c(Na+) = c(SO42-) >c(NH4+) >c(H+) >c(OH-)
C.0.1 mol·L-1Na2CO3溶液与0.1mol·L-1NaHCO3,溶液等体积混合所得溶液:
c(CO32-)+2c(OH-)=c(HCO3- )+c(H2CO3)+2c(H+)
D.相同温度下,pH相等的Na2CO3溶液、C6H5ONa(苯酚钠)溶液、NaOH溶液:c(C6H5ONa)>c(Na2CO3)>c(NaOH)
查看答案和解析>>
科目: 来源:2011-2012学年江苏省高三3月双周练习(二)化学试卷(解析版) 题型:选择题
如图I所示,甲、乙之间的隔板K和活塞F都可以左右移动,甲中充入2 molA和1 mol B,乙中充入2 mol C和1 mol He,此时K停在0处。在一定条件下发生反应:2A(g)+B(g) 2C(g),反应达到平衡后,再恢复至原温度,则下列说法正确的是
2C(g),反应达到平衡后,再恢复至原温度,则下列说法正确的是

A.达到平衡时,隔板K最终停留在刻度0与-2之间
B.若达到平衡时,隔板K最终停留在刻度-l处,则乙中C的转化率小于50%
C.若达到平衡时,隔板K最终停留在靠近刻度-2处,则乙中F最终停留刻度大于4
D.若图Ⅱ中x轴表示时间,则y轴可表示甲、乙两容器中气体的总物质的量或A的物质的量
查看答案和解析>>
科目: 来源:2011-2012学年江苏省高三3月双周练习(二)化学试卷(解析版) 题型:选择题
a mol FeS与b mol FeO投入到V L、c mol·L-1的稀硝酸溶液中充分反应,产生NO气体,所得澄清溶液的成分可看作是Fe(NO3)3、H2SO4的混合液,则反应中未被还原的硝酸可能为( )

查看答案和解析>>
科目: 来源:2011-2012学年江苏省高三3月双周练习(二)化学试卷(解析版) 题型:填空题
(20分)聚合氯化铝是一种新型、高效絮凝剂和净水剂,其单体是液态的碱式氯化铝[Al2(OH)nCl6-n]。本实验采用铝盐溶液水解絮凝法制备碱式氯化铝。其制备原料为分布广、价格廉的高岭 土,化学组成为:Al2O3(25%~34%)、SiO2(40%~50%)、Fe2O3(0.5%~3.0%)以及少量杂质和水分。已知氧化铝有多种不同的结构,化学性质也有差异,且一定条件下可相互转化;高岭土中的氧化铝难溶于酸。制备碱式氯化铝的实验流程如下:
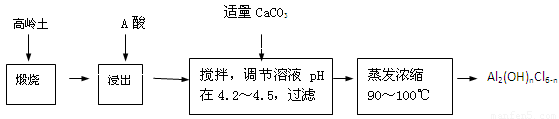
已知:Fe3+、Al3+以氢氧化物形式完全沉淀时,溶液的pH分别为3.2、5.2。
根据流程图回答下列问题:
(1)“煅烧”的目的是_______________________________________________。
(2)“浸出”过程中发生反应的离子方程式为_______________________________。
(3)“浸出”选用的酸为_______。配制质量分数15%的A酸需要200mL30%的A酸(密度约为1.15g/cm3)和_______g蒸馏水,配制用到的仪器有烧杯、玻璃棒、______________。
(4)为提高铝的浸出率,可采取的措施有 _______________(要求写出三条)。
(5)“调节溶液pH在4.2~4.5”的过程中,除添加必要的试剂,还需借助的实验用品是_________________;“蒸发浓缩”需保持温度在90~100℃,控制温度的实验方法是___________ ______。
(6)实验中制备碱式氯化铝反应的化学方程式为_________________
查看答案和解析>>
科目: 来源:2011-2012学年江苏省高三3月双周练习(二)化学试卷(解析版) 题型:填空题
(10分)下图中的反应①是重要的电化学工业反应,反应②可用于制备新型消毒净水剂Na2FeO4。常温下B、C为气态单质,G是当代社会使用量最大的金属,其余均为化合物。(反应时加入或生成的水,以及生成沉淀I时的其他产物均已略去) 。

请回答下列问题:
(1)L的电子式为_______________。
(2)J溶液蒸干灼烧得到的物质是(填化学式) _______________。
(3)反应①的化学方程式是____________________________________。
(4)反应②的离子方程式是____________________________________。
(5)Na2FeO4能起到消毒净水的原理是 。(用文字叙述)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com