
科目: 来源:2013届浙江省高二下学期期中考试化学试卷(解析版) 题型:选择题
可逆反应①X(g)+2Y(g)  2Z(g)、②2M(g)
2Z(g)、②2M(g)  N(g)+P(g)分别在密闭容器的两个反应室中进行,反应室之间有无摩擦、可滑动的密封隔板。反应开始和达到平衡状态时有关物理量的变化如图所示:
N(g)+P(g)分别在密闭容器的两个反应室中进行,反应室之间有无摩擦、可滑动的密封隔板。反应开始和达到平衡状态时有关物理量的变化如图所示:

下列判断正确的是( )
A.反应①的正反应是吸热反应
B.达平衡(Ⅰ)时体系的压强与反应开始时体系的压强之比为14:15
C.达平衡(Ⅱ)时,X的转化率为5/6
D.在平衡(Ⅰ)和平衡(Ⅱ)中,M的体积分数相等
查看答案和解析>>
科目: 来源:2013届浙江省高二下学期期中考试化学试卷(解析版) 题型:填空题
(6分)设计出燃料电池使汽油氧化直接产生电流是对21世纪最富有挑战性的课题之一。最近有人制造了一种燃料电池,一个电极通入空气,另一电极通入汽油蒸气,电池的电解质是掺杂了Y2O3的ZrO2晶体,它在高温下能传导O2-离子。回答如下问题:
(1)以壬烷(C9H20)代表汽油,这个电池放电时发生的化学反应的化学方程式是:
(2)这个电池的正极发生的反应是:
负极发生的反应是:
固体电解质里的O2-的移动方向是:
向外电路释放电子的电极是:
查看答案和解析>>
科目: 来源:2013届浙江省高二下学期期中考试化学试卷(解析版) 题型:填空题
(9分)一定条件下,在一容积可变的密闭容器中,反应: 过程中的能量变化如图所示。反应过程中,A、B、C的物质的量(mol)的变化如下表:
过程中的能量变化如图所示。反应过程中,A、B、C的物质的量(mol)的变化如下表:

|
时间(min) |
0 |
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
|
n(A) |
2.00 |
1.90 |
1.82 |
1.76 |
1.64 |
1.54 |
1.50 |
1.50 |
1.50 |
|
n(B) |
1.00 |
0.95 |
0.91 |
0.88 |
0.82 |
0.77 |
0.75 |
0.75 |
0.75 |
|
n(C) |
0 |
0.10 |
0.18 |
0.24 |
0.36 |
0.46 |
0.50 |
0.50 |
0.50 |
回答下列问题:
(1)反应 的正反应△H (填“大于”或“小于”)0。
的正反应△H (填“大于”或“小于”)0。
(2)该反应平衡时,下列说法不正确的是
(A)气体的密度不再改变 (B)A的物质的量浓度不变
(C)放出或吸收的热量不再变化 (D)v正(A)=v逆(A)=0
(3)toC时,在一容积为2L的恒容密闭容器内加入0.4molA和0.6molB,在一定条件下发生反应,反应中C的物质的量浓度变化情况如下图:

①该温度下,反应: 的平衡常数K=
。
的平衡常数K=
。
②反应进行到1分钟时B物质的量为 。
③在第5min时,将容器的体积缩小一半后,若在第8min达到新的平衡时A的总转化率为75%,请在上图中画出第5min到新平衡时C的物质的量浓度的变化曲线。
查看答案和解析>>
科目: 来源:2013届浙江省高二下学期期中考试化学试卷(解析版) 题型:实验题
(9分)某化学兴趣小组在学习了电解质的有关知识后,老师提出了一个“电解质水溶液导电能力的强弱的影响因素”的课题。让该小组来完成课题的研究,已知HCl在水中能完全电离。
(1)该小组同学首先用密度为1.049 g·cm-3的乙酸(CH3COOH)和质量分数为36.5%,密度为1.18 g·cm-3的浓盐酸分别配制1 mol/L CH3COOH溶液和1 mol/L HCl溶液各500 mL,则他们应该量取乙酸和浓盐酸的体积分别为 和 ;
(2)某同学在配制500 mL 1 mol/L的CH3COOH溶液时,向容量瓶中转移溶液时操作如图所示,图中的错误有 ;

(3)他们首先用下图所示装置测1 mol/L的CH3COOH溶液和1 mol/L HCl溶液的导电能力,接通电源后发现与HCl溶液相连的灯泡较亮,有同学认为乙酸是弱电解质,你 (填“同意”或“不同意”)他的观点,通过该现象你得到的结论是

(4)他们又用上述装置测物质的量浓度相同的CuSO4溶液和NaOH溶液的导电能力,接通电源后发现与CuSO4溶液相连的灯泡较亮,有同学认为NaOH是弱电解质,你 (填“同意”或“不同意”)他的观点,通过该现象你得到的结论是 ;
(5)通过上述探究实验,你能得到的结论是
查看答案和解析>>
科目: 来源:2013届浙江省高二下学期期中考试化学试卷(解析版) 题型:填空题
(13分)材料1:铁及其化合物在工农业、生活中有广泛的应用。高铁酸钾(K2FeO4)具有极强的氧化性,是一种优良的水处理剂。
(1)已知:4FeO42-+10H2O 4Fe(OH)3+8OH-+3O2。
4Fe(OH)3+8OH-+3O2。
K2FeO4在处理水的过程中所起的作用有 。
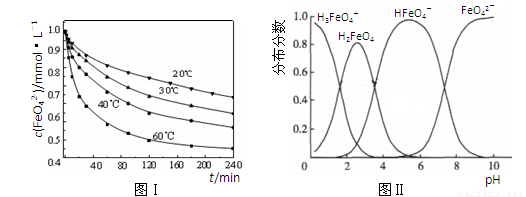
(2)将适量K2FeO4溶解于pH=4.74的溶液中,配制成c(FeO42-) =1.0 mmol·L-1的试样,将试样分别置于20℃、30℃、40℃和60℃的恒温水浴中,测定c(FeO42-)的变化,结果见图Ⅰ。该实验的目的是 ;发生反应的△H 0(填“>”、“<”或“=”)。
(3)FeO42-在水溶液中的存在形态如图Ⅱ所示。下列说法正确的是 (填字母)。
A.不论溶液酸碱性如何变化,铁元素都有4种存在形态
B.向pH=10的这种溶液中加硫酸至pH=2,HFeO4-的分布分数逐渐增大
C.向pH=6的这种溶液中加KOH溶液,发生反应的离子方程式为:
HFeO4-+OH-=FeO42-+H2O
材料2:化合物KxFe(C2O4) y·zH2O(Fe为+3价)是一种光敏感材料,实验室可以用如下方法制备这种材料并测定其组成。
I.制备:

(4)结晶时应将饱和溶液在黑暗处等待晶体的析出,这样操作的原因是 。
(5)操作Ⅲ的名称是 。
Ⅱ.组成测定:
称取0.491g实验所得晶体(假设是纯净物)置于锥形瓶中,加足量蒸馏水和稀H2SO4。将C2O42-完全转化为H2C2O4,用0.10mol·L-1KMnO4溶液进行滴定,消耗KMnO4溶液12.00mL时恰好反应;再加入适量的还原剂,将Fe3+完全转化为Fe2+,用KMnO4溶液继续滴定,当Fe2+完全氧化时,用去KMnO4溶液2.00mL。相关反应如下:
2KMnO4+5H2C2O4+3H2SO4=2MnSO4+K2SO4+10CO2↑+8H2O
MnO4-+5Fe2++8H+=Mn2++5Fe3++4H2O
(6)配制250mL 0.10mol·L-1KMnO4溶液及上述滴定实验中所需的玻璃仪器除烧杯、玻璃棒、胶头滴管、量筒、锥形瓶外还有 和 。两个滴定中到达终点时溶液颜色为 色,且30秒内不变色。
(7)通过计算,求此光敏材料的化学式 。
查看答案和解析>>
科目: 来源:2013届浙江省高二下学期期中考试化学试卷(解析版) 题型:填空题
(10分)(1)反应Fe(s)+CO2(g) FeO(s)+CO(g) △H1,平衡常数为K1
FeO(s)+CO(g) △H1,平衡常数为K1
反应Fe(s)+H2O(g) FeO(s)+H2(g)
△H2,平衡常数为K2
FeO(s)+H2(g)
△H2,平衡常数为K2
在不同温度时K1、K2的值如下表:
|
|
700℃ |
900℃ |
|
K1 |
1.47 |
2.15 |
|
K2 |
2.38 |
1.67 |
①反应 CO2(g) + H2(g) CO(g) + H2O(g) △H ,平衡常数K,则△H= (用△H1和△H2表示),K= (用K1和K2表示),且由上述计算可知,反应CO2(g)
+ H2(g)
CO(g) + H2O(g) △H ,平衡常数K,则△H= (用△H1和△H2表示),K= (用K1和K2表示),且由上述计算可知,反应CO2(g)
+ H2(g) CO(g) + H2O(g)是
反应(填“吸热”或“放热”)。
CO(g) + H2O(g)是
反应(填“吸热”或“放热”)。
②能判断CO2(g)
+ H2(g) CO(g) + H2O(g)达到化学平衡状态的依据是 (填序号)。
CO(g) + H2O(g)达到化学平衡状态的依据是 (填序号)。
A.容器中压强不变 B.混合气体中c(CO)不变
C.v正(H2)= v逆(H2O) D.c(CO)= c(CO2)
(2)一定温度下,向某密闭容器中加入足量铁粉并充入一定量的CO2气体,发生反应Fe(s)+CO2(g) FeO(s)+CO(g)
△H > 0,CO2的浓度与时间的关系如图所示:
FeO(s)+CO(g)
△H > 0,CO2的浓度与时间的关系如图所示:

① 该条件下反应的平衡常数为 ;若铁粉足量,CO2的起始浓度为2.0 mol·L-1,则平衡时CO2的浓度 mol·L-1。
②下列措施中能使平衡时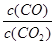 增大的是
(填序号)
增大的是
(填序号)
A.升高温度 B.增大压强
C.充入一定量的CO2 D.再加入一定量铁粉
查看答案和解析>>
科目: 来源:2013届浙江省高二下学期期中考试化学试卷(解析版) 题型:填空题
(8分)下列反应在210℃时达到平衡:
①PCl5(g) PCl3(g)+Cl2(g);△H1>0
K1=1mol·L—1
PCl3(g)+Cl2(g);△H1>0
K1=1mol·L—1
②CO(g)+Cl2(g) COCl2(g);△H2<0
K2=5×104L·mol—1
COCl2(g);△H2<0
K2=5×104L·mol—1
③COCl2(g) CO(g)+Cl2(g) △H3
K3
CO(g)+Cl2(g) △H3
K3
④2SO2(g)+O2(g) 2SO3(g);△H4<0
2SO3(g);△H4<0
(1)反应③的平衡常数K3为 。
(2)要使反应①和反应②的K数值相等,可采取的措施是 (填序号)。
A.降低反应①、②体系中Cl2浓度 B.反应①、②选择不同的催化剂
C.反应①、反应②同时升高温度 D.反应①、反应②同时降低温度
E.反应①降低温度,反应②维持210℃
(3)在甲、乙两容器中分别发生反应④,甲恒容、乙恒压,温度相同且恒定。起始时甲中加入0.02molSO2和0.01molO2,乙中加入0.02molSO3气体,开始时两容器压强相等,最后分别达到平衡。下列有关它们达到平衡状态后的叙述正确的是 (填序号)。
A.体积:甲可能小于乙 B.SO3的物质的量:甲一定小于乙
C.压强:甲可能大于乙 D.浓度比c(SO2)/c(SO3):甲一定小于乙
(4)丙容器为容积不变的反应容器,要求通过调节体系的温度使反应④达到平衡时,保持容器内气体总物质的量为15mol。现向容器中加入xmolSO2,6.5mol O2,2.0molSO3。
①若x=5.5,需要 (填“降低”“升高”或“保持”)体系温度,使反应在平衡时达到题设要求;
②欲使起始反应维持向逆反应方向移动,则x的取值范围为 。
查看答案和解析>>
科目: 来源:2013届浙江省温州市高二期中考试化学试卷(解析版) 题型:选择题
下列叙述正确的是( )
A.强电解质都是离子化合物,因此NaCl是离子化合物
B.醋酸溶液的导电能力可能比硫酸溶液强
C.SO3溶于水,其水溶液能导电,故SO3是电解质
D.硫磺是单质,不导电,因此硫磺是非电解质
查看答案和解析>>
科目: 来源:2013届浙江省温州市高二期中考试化学试卷(解析版) 题型:选择题
下列描述违背化学原理的是( )
A.“冰,水为之,而寒于水”说明相同质量的水和冰,水的能量高
B.反应A(g)+3B(g) 2C(g)达平衡后,温度不变,增大压强,平衡正向移动,平衡常数K值增大
2C(g)达平衡后,温度不变,增大压强,平衡正向移动,平衡常数K值增大
C.SO2的催化氧化是一个放热的反应,升高温度,反应速率加快
D.电解饱和食盐水时,阳极的电极反应式为:2Cl- -2e-= Cl2 ↑
查看答案和解析>>
科目: 来源:2013届浙江省温州市高二期中考试化学试卷(解析版) 题型:选择题
广义的水解观点认为:无论是盐的水解还是非盐的水解,其最终结果是反应中各物质和水分别离解成两部分,然后两两重新组合成新的物质。根据上述观点,说法不正确的是( )
A.BaO2的水解产物是Ba(OH)2和H2O2 B.PCl3的水解产物是HClO和H3PO4
C.A14C3的水解产物是Al(OH)3和CH4 D.CH3COCl的水解产物是两种酸
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com