
科目: 来源:2011-2012学年重庆市高三上学期期中考试理科综合试题(化学部分) 题型:选择题
根据下列实验现象,所得结论正确的是( )

|
实验 |
实验现象 |
结论 |
|
A. |
左烧杯中镁表面有气泡,右边烧杯中铜表面有气泡 |
活动性:Al>Mg>Cu |
|
B. |
左边棉花变为橙色,右边棉花变为蓝色 |
氧化性:Cl2>Br2>I2 |
|
C. |
左边溶液产生黄色沉淀,右边溶液产生黄色沉淀 |
氧化性:Cl2>Br2>S |
|
D. |
锥形瓶中有气体产生,烧杯中液体变浑浊 |
非金属性:S>C>Si |
查看答案和解析>>
科目: 来源:2011-2012学年重庆市高三上学期期中考试理科综合试题(化学部分) 题型:选择题
已知晶体硅的燃烧热为989KJ/mol,且断裂1molSi-Si、Si-O需吸收的能量分别为176KJ, 460KJ,则1molO=O断裂时吸收的能量为( )
A .499KJ B .2477 KJ C. 245 KJ D.1557 KJ
查看答案和解析>>
科目: 来源:2011-2012学年重庆市高三上学期期中考试理科综合试题(化学部分) 题型:选择题
将16. 0g铜与100 mL一定浓度硝酸反应,铜完全溶解产生NO和NO2混合气体在标准状况下体积为11.2 L。待产生的气体全部释放后,向溶液中加入100mL、bmol / L NaOH溶液,恰好使溶液中的Cu2+ 全部转化成沉淀,则原硝酸溶液的浓度一定为( )
A. 1.0 mol / L B.(b+5)mol / L C.10mol / L D.无法计算
查看答案和解析>>
科目: 来源:2011-2012学年重庆市高三上学期期中考试理科综合试题(化学部分) 题型:填空题
(16分)A、B、C、D、E、F、G是七种短周期主族元素,它们的原子序数依次增大,其中在元素周期表中A的原子半径最小,B和F、C和G分别是同一主族元素,含有D元素的物质焰色反应为黄色,G元素的最外层电子数是次外层电子数的3/4。又知B元素的最外层电子数是内层电子数的2倍,D、E、G三者的最高价氧化物的水化物两两皆能反应。请回答:
(1)A与C形成的原子个数比为1:1的化合物的电子式为 ,该物质含
键;它与GC2反应的化学方程式为
(2)D、E两者氧化物的水化物反应的离子方程式为 ;
(3)B、F的最高价氧化物 (填化学式)的沸点高,理由是
(4)A、C、G间可以形成甲、乙两种负一价双原子阴离子,甲有18个电子,乙有10个电子,则甲与乙反应的离子方程式为 。
查看答案和解析>>
科目: 来源:2011-2012学年重庆市高三上学期期中考试理科综合试题(化学部分) 题型:实验题
(15分)从固体混合物A出发可以发生如下框图所示的一系列变化。
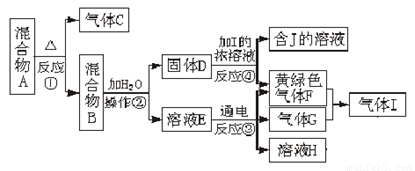
(1)在实验室,气体C的检验方法是 。 (2)操作②的名称是 ,该操作所使用的玻璃仪器有 。
(3)写出下列反应的离子方程式:
反应③ ;
反应④ 。
(4) 实验中多余的气体I必须吸收,以免污染空气。下图是实验室用NaOH吸收气体I的装置,为防止产生倒吸现象,不合理的装置是 (填序号)。
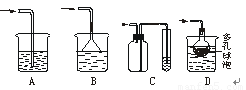
查看答案和解析>>
科目: 来源:2011-2012学年重庆市高三上学期期中考试理科综合试题(化学部分) 题型:填空题
(11分)雄黄(As4S4)和雌黄(As2S3)是提取砷的主要矿物原料,二者在自然界中共生。根据题意完成下列填空:
(1) As2S3和SnCl2在盐酸中反应转化为As4S4和SnCl4并放出H2S气体。写出该反应
并配平
(2)上述反应中的氧化剂是 ,反应产生的气体可用 吸收。
(3) As2S3和HNO3有如下反应:
3As2S3+ 10H++ 28NO3— + 4H2O=6H3AsO4+9SO42— +28NO↑
若生成2mol H3AsO4,则反应中转移电子的物质的量为 mol。若将该反应设计成一原电池,则NO应该在 (填“正极”或“负极”)附近逸出。
查看答案和解析>>
科目: 来源:2011-2012学年重庆市高三上学期期中考试理科综合试题(化学部分) 题型:实验题
(18分)测定SO2转化成SO3的转化率可以用下图装置,装置中烧瓶内发生的化学反应方程式为:Na2SO3(s)+H2SO4(85%)=Na2SO4+H2O+SO2↑。
(已知SO3的熔点是16.8℃,沸点是44.8℃)
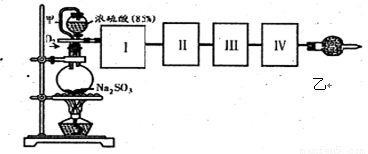
(1)装置中甲管的作用是 ;
乙装置的作用是 。
(2)根据实验需要,应该在I、II、Ⅲ、IV处连接合适的装置,请从下图A~E装置中选择最适合装置并将其序号填放下面的空格中。I、Ⅱ、Ⅲ、Ⅳ处连接的装置分别是 、 、 、 。
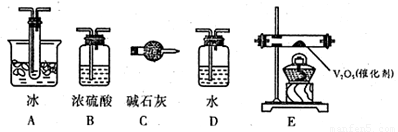
(3)为使SO2有较高的转化率,实验中加热催化剂与滴加浓硫酸的顺序中,应采取的操作是 ,若用大火加热烧瓶时,SO2的转化率会 (填“升高”、“不变”或“降低”)。
(4)将SO2通入含1 mol氯酸的溶液中,可生成一种强酸和一种氧化物,并有6.02×1023个电子转移,则该反应的化学方程式为 。
(5)用nmolNa2SO3粉末与足量浓硫酸进行此实验,当反应结束时,继续通入O2一段时间后,测得装置Ⅳ增重了mg,则实验中SO2的转化率为 。(用含m、n的代数式填写)
查看答案和解析>>
科目: 来源:2011-2012学年重庆市高三9月月考理科综合试题(化学部分) 题型:选择题
美国科学家用有机分子和球形笼状分子C60首次制成了“纳米车”(如图),每辆“纳米车”是用一个有机分子和4个球形笼状分子“组装”而成。“纳米车”可以用来运输单个的有机分子,生产复杂的材料和药物,成为“纳米生产”中的有用工具。下列说法正确的是
A.我们可以直接用肉眼清晰地看到这种“纳米车”的运动
B.“纳米车”的诞生,说明人类操纵分子的技术进入一个新阶段
C.C60是一种新型化合物
D.C60熔点比金刚石熔点高
查看答案和解析>>
科目: 来源:2011-2012学年重庆市高三9月月考理科综合试题(化学部分) 题型:选择题
关节炎的病因主要是在关节滑液中形成了尿酸钠(NaUr)晶体,主要反应为: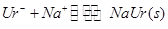 ,第一次关节炎发作往往在冬季,有关该反应的说法正确的是
,第一次关节炎发作往往在冬季,有关该反应的说法正确的是
A.正反应是吸热反应 B.正反应是放热反应
C.升高温度平衡向正反应方向移动 D.以上说法都不正确
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com