
科目: 来源:2011-2012学年福建省晋江市四校高三第二次联合考试化学试卷 题型:选择题
根据表中给出的几种物质的熔、沸点数据,判断下列有关说法中错误的是( )
|
|
NaCl |
MgCl2 |
AlCl3 |
SiCl4 |
单质B |
|
熔点 |
810 ℃ |
710℃ |
190℃ |
—68℃ |
2 300℃ |
|
沸点 |
1465℃ |
1 418℃ |
182℃ |
57℃ |
2 500℃ |
A.SiCl4是分子晶体 B.单质B可能是原子晶体
C.AlCl3加热能升华 D.NaCl中键的强度比MgCl2的小
查看答案和解析>>
科目: 来源:2011-2012学年福建省晋江市四校高三第二次联合考试化学试卷 题型:选择题
LiAlH4
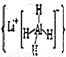 、LiH遇水均能剧烈分解释放出H2,LiAlH4在125℃时分解为
、LiH遇水均能剧烈分解释放出H2,LiAlH4在125℃时分解为
LiH、H2和Al。下列说法不正确的是( )
A.LiH与D2O反应,所得氢气的摩尔质量为4g/mol
B.1mol LiAlH4 125℃完全分解,转移电子数为3NA
C.LiAlH4溶于适量水得到无色溶液,则化学方程式为:LiAlH4+2H2O== LiAlO2+4H2↑
D.LiAlH4与乙醛作用生成乙醇,LiAlH4作还原剂
查看答案和解析>>
科目: 来源:2011-2012学年福建省晋江市四校高三第二次联合考试化学试卷 题型:选择题
相同温度下,在体积相等的三个恒容密闭容器中发生可逆反应:
N2(g) + 3H2(g) 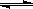 2NH3(g) △H=-92.4 kJ/mol。
2NH3(g) △H=-92.4 kJ/mol。
实验测得起始、平衡时的有关数据如下表:
|
容器编号 |
起始时各物质物质的量/mol |
平衡时反应中的能量变化 |
||
|
N2 |
H2 |
NH3 |
||
|
① |
1 |
3 |
0 |
放出热量a kJ |
|
② |
2 |
3 |
0 |
放出热量b kJ |
|
③ |
2 |
6 |
0 |
放出热量c kJ |
下列叙述正确的是( )
A.放出热量关系:a < b < 92.4
B.三个容器内反应的平衡常数:③ > ① > ②
C.达平衡时氨气的体积分数:① > ③
D.N2的转化率:② > ① > ③
查看答案和解析>>
科目: 来源:2011-2012学年福建省晋江市四校高三第二次联合考试化学试卷 题型:选择题
CuCO3 和Cu2(OH)2CO3的混合物34.6 g,可恰好完全溶解于300mL、2 mol·L-1的盐酸溶液中,若加热分解等量的这种混合物可得CuO固体质量为( )
A.16.0 g B.19.2 g C.24.0 g D.30.6 g
查看答案和解析>>
科目: 来源:2011-2012学年福建省晋江市四校高三第二次联合考试化学试卷 题型:选择题
钠氯化镍蓄电池是一种新型的电动汽车蓄电池,其正极MCl2中的M代表Ni、Fe、Ca、Cr、Mn、Cu等一系列金属,其中NiCl2的效果最好。而负极的活性物质是液态金属钠。正、负极活性物质被一种只允许Na+迁移的β-Al2O3固体电解质陶瓷管分隔,由于正极是固态多孔金属氧化物,所以还需要添加NaAlCl4熔盐在正极处作第二电解质,在正、负极之间传导钠离子。下列有关钠氯化镍蓄电池的说法错误的是 ( )
A.电池放电时的总反应为2Na+NiCl2===Ni+2NaCl
B.充电时阳极的电极反应为Na++e-===Na
C.放电时正极的电极反应为Ni2++2e-===Ni
D.该电池被称为绿色电池,最大原因是从废弃电池中可以
方便地回收较纯的镍,其他产物对环境没有影响
查看答案和解析>>
科目: 来源:2011-2012学年福建省晋江市四校高三第二次联合考试化学试卷 题型:选择题
铅的冶炼大致过程如下:
①富集:将方铅矿(PbS)进行浮选;②焙烧:2PbS+3O2  2PbO+2SO2;
2PbO+2SO2;
③制粗铅:PbO+C Pb+CO;PbO+CO
Pb+CO;PbO+CO Pb+CO2。
Pb+CO2。
下列说法正确的是 ( )
A.浮选法富集方铅矿的过程属于化学变化
B.方铅矿焙烧反应中,PbS是还原剂,发生还原反应
C.过程②中,制取1molPbO共转移2mol电子
D.将1molPbS冶炼成Pb理论上至少需要6g碳
查看答案和解析>>
科目: 来源:2011-2012学年福建省晋江市四校高三第二次联合考试化学试卷 题型:选择题
已知反应:2 E (l)  U (l) 。取等量的E,分别在20℃、50℃测得E的转化率随时间变化的关系曲线(Y-t)如图所示。则下列说法正确的是(
)
U (l) 。取等量的E,分别在20℃、50℃测得E的转化率随时间变化的关系曲线(Y-t)如图所示。则下列说法正确的是(
)
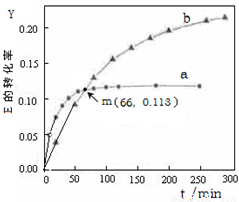
A.该反应的∆H > 0
B.b代表50℃下E的Y-t曲线
C.m点(66,0.113)时有: ∆n (E,20℃) = ∆n (E,50℃)
D.升高温度可以缩短达到平衡的时间,提高E的转化率
查看答案和解析>>
科目: 来源:2011-2012学年福建省晋江市四校高三第二次联合考试化学试卷 题型:填空题
(10分)已知:A、B、C、D四种短周期元素原子序数依次增大,A与D的原子序数之和等于B与C的原子序数之和,由D元素组成的单质在通常状况下呈黄绿色,B、C、D三种元素位于同一周期,B、C、D三种元素的最高价氧化物对应的水化物分别为X、Y、Z,X、Y、Z可两两相互反应生成盐和水,试推断并用相应的化学用语回答下列问题。
(1)D元素原子的结构示意图为 ;
(2)Y与C元素的最高价氧化物可以发生反应,该反应的离子方程式为
;
(3)A、B、C三种元素的原子半径由小到大的顺序为 ;
(4)A与D两元素的气态氢化物之间可以反应生成一种盐,该盐的水溶液呈 (填“酸”、“碱”或“中”)性,该水溶液中各离子浓度由小到大的顺序为 。
查看答案和解析>>
科目: 来源:2011-2012学年福建省晋江市四校高三第二次联合考试化学试卷 题型:填空题
(12分)铁及其化合物在生活、生产中有广泛应用。请回答下列问题:
(1)黄铁矿(FeS2)是生产硫酸和冶炼钢铁的重要原料。其中一个反应为
3FeS2+8O2  6SO2+Fe3O4,有3 molFeS2参加反应,转移
mol电子。
6SO2+Fe3O4,有3 molFeS2参加反应,转移
mol电子。
(2)氯化铁溶液常用作印刷电路铜板腐蚀剂,反应的离子方程式为 ;从腐蚀废液回收得到金属铜,还需要的试剂是 。
(3)与明矾相似,硫酸铁也可用作净水剂,在使用时发现硫酸铁并不能使酸性废水中的悬浮物沉降除去,其原因是
(4)钢铁的电化腐蚀简单示意图如下,将该图稍作修改即可成为钢铁电化学防护的简单示意图,请在下图虚线框内作出修改,并用箭头标出电子流动方向。

查看答案和解析>>
科目: 来源:2011-2012学年福建省晋江市四校高三第二次联合考试化学试卷 题型:填空题
(12分)甲、乙、丙三种物质都含有A元素,只有甲是单质,其转化关系如下:
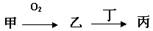
(1)若乙是目前世界倡导需减少排放的温室气体,丁也含有A元素。则含有7个中子的核素A可用符号表示为 ,丁溶液呈碱性的原因用离子方程式表示为 ;已知:在常温常压下,1mol甲和一氧化碳分别与充足的氧气反应放出的热量分别是393.5kJ、283.0kJ。试写出甲与乙相互反应的热化学方程式______________ 。
(2)若A是非金属元素,其次外层电子是最外层电子数的2倍,则乙在现代通讯中可用于制造 ,写出一个有丙参加的、能证明碳的非金属性强于A的化学方程式 ;
(3)若甲是生活中最常用的过渡金属单质,其在点燃条件与氧气反应生成乙。若丁是稀盐酸,则乙→丙的化学方程式为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com