
科目: 来源:2011-2012学年福建省高三第一学期联合命题考试化学试卷 题型:填空题
(10分)氯气是氯碱工业的主要产品之一,它是一种常用的消毒剂,其消毒原理是与水反应生成了次氯酸:
Cl2 + H2O  HCl + HClO K=4.5×10-4
HCl + HClO K=4.5×10-4
次氯酸的强氧化性能杀死水中的病菌(不直接用次氯酸为自来水消毒是因为次氯酸易分解,且毒性较大)。但是,由于氯气贮运不方便,且具有一定的危险性,目前正逐渐被其它性能优越的消毒产品所替代。请回答:
(1)氯碱工业生产氯气的化学方程式为 。
(2)84消毒液(主要成分为NaClO)与氯气相比具有贮运方便等优点,用氯气与烧碱溶液反应制备84消毒液的离子方程式为 。
(3)二氧化氯是一种高效、广谱、安全的杀菌、保鲜剂。我国科学家研发了用氯气氧化亚氯酸钠(NaClO2)固体制备二氧化氯的方法,其化学方程式为 。
(4)一位同学设计了一套用浓盐酸和KMnO4固体制取少量氯气并比较氯气与碘单质的氧
化性强弱的微型装置(如图)。
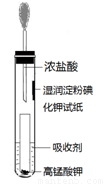
①下列溶液能吸收Cl2的是 (填字母序号)。
A. 饱和食盐水 B. 饱和Na2SO3溶液
C. 饱和NaOH溶液 D. 浓硫酸
②能说明Cl2的氧化性强于I2的实验现象是
。
查看答案和解析>>
科目: 来源:2011-2012学年福建省高三第一学期联合命题考试化学试卷 题型:填空题
(10分)“低碳循环”引起各国的高度重视,而如何降低大气中CO2的含量及有效地开发利用CO2,引起了全世界的普遍重视。所以“低碳经济”正成为科学家研究的主要课题
(1)用电弧法合成的储氢纳米碳管常伴有大量的碳纳米颗粒(杂质),这种颗粒可用如下氧化法提纯,请完成该反应的化学方程式:
___ C+ ___ KMnO4+6 H2SO4 = ____CO2↑+ ____MnSO4 + ____K2SO4+ 6H2O
(2)将不同量的CO(g)和H2O(g)分别通入到体积为2L的恒容密闭容器中,进行反应
CO(g)+H2O(g) CO2(g)+H2(g),得到如下二组数据:
CO2(g)+H2(g),得到如下二组数据:
|
实验组 |
温度℃ |
起始量/mol |
平衡量/mol |
达到平衡所需时间/min |
||
|
CO |
H2O |
H2 |
CO |
|||
|
1 |
650 |
4 |
2 |
1.6 |
2.4 |
6 |
|
2 |
900 |
2 |
1 |
0.4 |
1.6 |
3 |
①实验1中以v (CO2) 表示的反应速率为 (保留小数点后二位数,下同)。
②实验2条件下平衡常数K=_________,该反应为 (填“吸”或“放”)热反应。
(3)已知在常温常压下:
① 2CH3OH(l) + 3O2(g) = 2CO2(g) + 4H2O(g) ΔH = -1275.6 kJ/mol
② 2CO (g)+ O2(g) = 2CO2(g) ΔH = -566.0 kJ/mol
③ H2O(g) = H2O(l) ΔH = -44.0 kJ/mol
写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式:
⑷某实验小组依据甲醇燃烧的反应原理,设计如右图所示的电池装置。

① 该电池正极的电极反应为
。
②该电池工作时,溶液中的OH-向______极移动。
查看答案和解析>>
科目: 来源:2011-2012学年福建省高三第一学期联合命题考试化学试卷 题型:填空题
(10分)(1)常温下,某水溶液M中存在的离子有:Na+、A2-、HA-、H+、OH-,存在的分子有H2O、H2A。根据题意回答下列问题:
①写出酸H2A的电离方程式__________________________。
②若溶液M由2 mol·L-1NaHA溶液与2mol·L-1NaOH溶液等体积混合而得,则溶液M的pH ____7 (填“>”、“<”或“=”);溶液M中各微粒的浓度关系正确的是 。
A.c(Na+)>c(A2-)>c(OH-) >c(H+)
B. c(HA-) +c(H2A) +c(H+)=c(OH-)
C.c(A2-)+c(HA-) +c(H2A)=1 mol·L-1
D. c(A2-)+c(HA-)+c(OH-)=c(Na+)+c(H+)
(2)室温时,氢氧化钙的溶度积KSP =4.7×10-6, 室温时将9 mL0.02 mol·L—1的氯化钙溶液与1 mL pH=13的氢氧化钠溶液混合后(溶液体积可直接加和),溶液中___ 沉淀析出(填“有”或“无”)。
(3) 某校课外活动小组为测定已部分脱水的生石膏的组成(xCaSO4·yH2O),做如下实验:将固体加热,经测量剩余固体质量随时间变化如图所示。
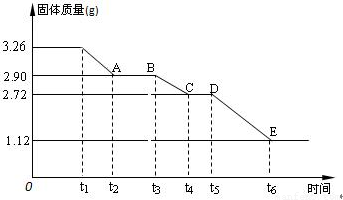
则x:y= 。t2~t3时间段固体的化学式为 。t5~t6时间段固体质量减轻的原因是产生了两种气体,其中一种能使品红溶液褪色。则该时间所发生反应的化学方程式为 。
查看答案和解析>>
科目: 来源:2011-2012学年福建省高三第一学期联合命题考试化学试卷 题型:实验题
(9分) 实验室用铜制取硫酸铜,将适量硝酸分多次加入到铜粉与稀硫酸的混合物中,加热使之反应完全,通过蒸发、结晶得到硫酸铜晶体。
(1)为了节约原料,硫酸和硝酸的物质的量之比最佳为____________;
为了吸收该反应中产生的尾气,可选择的最佳装置是_______________。
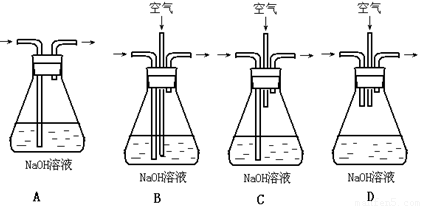
(2)为符合绿色化学的要求,某研究性学习小组进行如下设计:
方案1:以空气为氧化剂。将铜粉在仪器N中反复灼烧,使铜与空气充分反应生成氧化铜,再将氧化铜与稀硫酸反应。
方案2:将空气或氧气直接通入到铜粉与稀硫酸的混合物中,发现在常温下几乎不反应。向反应液中加少量FeSO4,再通入空气或氧气,即发生反应,生成硫酸铜。反应完全后,加物质甲调节pH ,铁元素全部转化为Fe(OH)3沉淀(一般认为铁离子的浓度下降到10-5 mol·L-1,就认为沉淀完全),然后过滤、浓缩、结晶。
(已知:Ksp[Cu(OH)2]≈10-22, Ksp[Fe(OH)3]≈10-38)
请回答下列问题:
①方案1中的N仪器名称是 ______________。
②为了使铁元素全部沉淀,应调节pH至少为_________。
③方案2中甲物质可选用的是________________________。
A.CaO B.NaOH C.CuCO3 D.Cu2(OH)2CO3 E.Fe2(SO4)3
④反应中加入少量FeSO4可加速铜的氧化,用离子方程式解释其原因___________________________________ _____________________________________。
查看答案和解析>>
科目: 来源:2011-2012学年福建省高三第一学期联合命题考试化学试卷 题型:填空题
【物质结构与性质】
X、Y、Z、W是原子序数依次增大的前四周期元素,已知:
①X元素原子的最外层电子数是次外层的2倍;
②Y元素原子的p轨道上有2个未成对电子;
③Z元素在同一短周期元素中的原子半径最大;
④W元素原子的最外层电子数与Z相同,其余各电子层均充满电子。
请回答下列问题:
(1)X、Y、Z三种元素的第一电离能从小到大的顺序是 (用元素符号表示,下同);
(2)W元素原子核外电子排布式是 ;
(3)Z元素与氢元素形成的化合物熔点比Y元素的氢化物熔点高,原因是 ;
(4)X的一种氢化物相对分子质量为42,分子中含有σ键和π键的个数比为8︰1,则该分子中X原子的杂化类型是 和 。
(5)Y的最简单氢化物可以和W2+形成配位键,而X的最简单氢化物则不行,其原因是 。
查看答案和解析>>
科目: 来源:2011-2012学年福建省高三第一学期联合命题考试化学试卷 题型:填空题
【有机化学基础】
Ⅰ.对羟基肉桂酸是一种强效的导电材料,在液晶显示器工业中近年来研究广泛。其结构简式如图所示:

(1)该有机物具有的官能团名称是 (写出其中的两种)
(2)该有机物能发生的反应类型是(填写代号) 。
A.酯化反应 B.消去反应 C.加成反应 D.水解反应
Ⅱ.芳香族化合物C10H10O2有如下的转化关系:

已知E能使Br2/CCl4溶液褪色。请回答下列问题:
(3)请写出A的结构简式: 。
(4)若有机物F与C互为同分异构体,则与有机物B互为同系物的F的同分异构体有
种。
(5)请写出B→C反应的化学反应方程式 。
查看答案和解析>>
科目: 来源:2011-2012学年福建省宁德市高三毕业班质量检查化学试卷 题型:选择题
2011年世界气候大会在南非德班召开,气候变化和环境问题再度引发全球关注。以下做法有利于保护环境的是 ( )
A.野外焚烧垃圾 B.使用一次性木质筷子
C.大量使用化肥、农药 D.推广使用散装水泥
查看答案和解析>>
科目: 来源:2011-2012学年福建省宁德市高三毕业班质量检查化学试卷 题型:选择题
设NA为阿伏加德罗常数的值,下列叙述正确的是 ( )
A.1 L 0.1 mol·L-1的CuCl2溶液中含Cu2+为0.1NA
B.标准状况下,22.4 L CCl4含CCl4分子为NA
C.1mol H3O+含质子数为10 NA
D.1molNa2O和Na2O2混合物中含阴离子的总数为NA
查看答案和解析>>
科目: 来源:2011-2012学年福建省宁德市高三毕业班质量检查化学试卷 题型:选择题
下列叙述正确的是 ( )
A.含金属元素的离子一定是阳离子
B.金属阳离子被还原一定得到金属单质
C.共价化合物中只含共价键
D.1H、2H、3H互为同素异形体
查看答案和解析>>
科目: 来源:2011-2012学年福建省宁德市高三毕业班质量检查化学试卷 题型:选择题
在溶液中一定能大量共存的离子组是 ( )
A.K+、Ca2+、Cl—、SO2-4 B.Na+、K+、Cl—、CO2—3
C.Na+、OH—、Cl—、HCO—3 D.H+、Fe3+、SO2—4、I—
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com