
科目: 来源:2011-2012学年浙江省高三第一学期期末考试化学试卷 题型:选择题
某FeSO4、Fe2(SO4)3、H2SO4的混合溶液100mL,已知溶液中阳离子的浓度相同(不考虑水解),且SO42-的物质的量浓度为6 mol·L-1,则此溶液最多可溶解铁粉的质量为
A.11.2 g B.16.8 g C.19.6 g D.22.4 g
查看答案和解析>>
科目: 来源:2011-2012学年浙江省高三第一学期期末考试化学试卷 题型:填空题
(9分)A、B、C、D、E五种短周期元素,它们的原子序数依次增大。B原子的最外层电子数是其次外层电子数的2倍;A的一种原子中,质量数与质子数之差为零。D元素的原子最外层电子数为m,次外层电子数为n;E元素的原子L层电子数为m+n,M层电子数为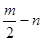 。请回答下列问题:
。请回答下列问题:
(1)B元素是____________,D元素在周期表中的位置是_____________________;
(2)C与E形成的化合物E3C属于________晶体(填“原子”、“离子”或“分子”);
(3)由A、D、E元素组成的化合物中存在的作用力是_________________________;
(4)写出一个E和D形成的化合物与水反应的化学方程式_______________________;
(5)C的最高价氧化物对应的水化物与其氢化物反应生成一种盐X,X的水溶液显________性(填“酸”、“碱”或“中”),其原因用离子方程式表示:___________
__________________________。
查看答案和解析>>
科目: 来源:2011-2012学年浙江省高三第一学期期末考试化学试卷 题型:填空题
(9分)甲、丙、丁是由短周期元素组成的物质,它们之间存在如下转化关系。
甲 + H2O → 丙 + 丁
(1)转化关系中所涉及的反应为非氧化还原反应。
①若甲是一种钠盐,丁为两性氢氧化物,则甲的化学式为 ,丁的酸式电离方程式为 。
②若甲是由N和Cl元素组成的化合物,其分子结构模型如右图所示, 丙具有漂白性。则甲中Cl元素的化合价是 ,丁与H2O有相同的电子总数,则丁的电子式为

(2)转化关系中所涉及的反应为氧化还原反应。
①若甲和丙是同主族元素组成的单质,且组成甲的元素位于第三周期,此反应的离子方程式是 。
②若丙和丁都可在一定条件下还原CuO,此反应的化学方程式是 。
查看答案和解析>>
科目: 来源:2011-2012学年浙江省高三第一学期期末考试化学试卷 题型:填空题
(11分)在汽车上安装三效催化转化器,可使汽车尾气中的主要污染物(CO、NOx、碳氢化合物)进行相互反应,生成无毒物质,减少汽车尾气污染。
(1)已知:N2(g)+ O2(g)=2NO(g) △H=+180.5 kJ·mol-1
2C(s)+ O2(g)=2CO(g) △H=-221.0 kJ·mol-1
C(s)+ O2(g)=CO2(g) △H=-393.5 kJ·mol-1
①尾气转化的反应之一:2NO(g)+2CO(g)=N2(g)+2CO2(g) △H= 。
②已知:N2、O2分子中化学键的键能分别是946 kJ·mol—1、497 kJ·mol—1,则NO分子中化学键的键能为 kJ·mol—1。
(2)某研究性学习小组在技术人员的指导下,在某温度时,按下列流程探究某种催化剂作用下的反应速率,用气体传感器测得不同时间的NO和CO浓度如表:
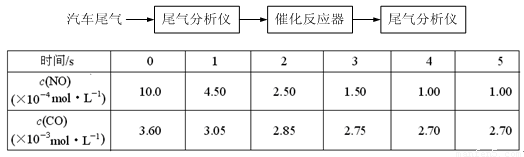
请回答下列问题(均不考虑温度变化对催化剂催化效率的影响):
①前3s内的平均反应速率v (N2) = _________________________。
②在该温度下,反应的平衡常数K = 。(只写出计算结果)
③该可逆反应△S 0(填“>”、“<”或“=”),在_______________(填“高温”、“低温”或“任何温度”)下能自发进行。
(3)CO分析仪以燃料电池为工作原理,其装置如图所示,该电池中电解质为氧化钇-氧化钠,其中O2-可以在固体介质NASICON中自由移动。下列说法错误的是
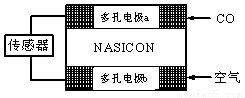
A.负极的电极反应式为:
CO+O2—―2e-=CO2
B.工作时电极b作正极,O2-由电极a流向电极b
C.工作时电子由电极a通过传感器流向电极b
D.传感器中通过的电流越大,尾气中CO的含量越高
查看答案和解析>>
科目: 来源:2011-2012学年浙江省高三第一学期期末考试化学试卷 题型:实验题
(11分)过氧化氢是重要的氧化剂和还原剂,常用于消毒、杀菌、漂白等。某化学兴趣小组同学围绕着过氧化氢开展了调查研究与实验。
Ⅰ.调查
(1)通过查阅资料,发现过氧化氢的沸点为152.1℃,而相对分子质量相同的硫化氢的沸点为-60.4℃,造成两者沸点差异大的主要原因是 ;
(2) 资料显示,过氧化氢制备目前最常用的是乙基蒽醌法,其主要过程可以用如图所示,写出此过程的总反应方程式是 。

Ⅱ.不稳定性实验研究
(3)为了探究温度、催化剂等外界条件对H2O2的分解速率的影响,某兴趣小组同学设计了如下三组实验,部分实验数据已经填在下面表中。
|
实验编号 |
T/℃ |
H2O2初始浓度/ mol·L-1 |
FeCl3初始浓度/ mol·L-1 |
|
Ⅰ |
20 |
1.0 |
|
|
Ⅱ |
50 |
1.0 |
0 |
|
Ⅲ |
50 |
|
0.1 |
①实验Ⅰ、Ⅱ研究温度对分解速率的影响,则实验Ⅰ中FeCl3初始浓度应为 mol·L-1,实验Ⅱ、Ⅲ研究催化剂对分解速率的影响,则实验Ⅲ中H2O2初始浓度应为 mol·L-1。
②三组实验中分解速率最快的是 (填编号)。
Ⅲ.过氧化氢含量的实验测定
兴趣小组同学用0.1000 mol·L-1酸性高锰酸钾标准溶液滴定试样中过氧化氢的含量,反应原理为:2MnO4-+5H2O2+6H+ =2Mn2++8H2O+ 5O2
(4)滴定到达终点的现象是__________________________________________________。
(5)用移液管吸取25.00mL试样置于锥形瓶中,重复滴定四次,每次消耗的 KMnO4标准溶液体积如下表所示:
|
|
第一次 |
第二次 |
第三次 |
第四次 |
|
体积(mL) |
17.10 |
18.10 |
18.00 |
17.90 |
计算试样中过氧化氢的浓度为 mol·L-1。
(6)若滴定前尖嘴中有气泡,滴定后消失,则测定结果 (“偏高”或“偏低”或“不变”)。
查看答案和解析>>
科目: 来源:2011-2012学年浙江省高三第一学期期末考试化学试卷 题型:实验题
(10分)高锰酸钾是深紫色的针状晶体,是最常用的氧化剂之一,工业上以软锰矿(主要成分是MnO2)为原料制备高锰酸钾。下面是实验室制取高锰酸钾的过程:

①称取15g固体KOH和8g固体KClO3,导入坩埚内,混合均匀,小火加热,并用铁棒搅拌。待混合物熔融后,一面搅拌,一面将10gMnO2粉末分批加入。随着反应的进行,熔融物的粘度逐渐增大,此时用力搅拌,待反应物干涸后,再强热5~10min。
②待熔体冷却后,从坩埚内取出,放入250mL烧杯中,用80mL蒸馏水分批浸取,并不断搅拌,加热以促进其溶解。趁热减压过滤浸取液,即可得到墨绿色的K2MnO4溶液。
③将K2MnO4溶液倒入烧杯中,加热至60℃,按如图所示进行电解。阳极是光滑的镍片,卷成圆筒状,阴极为粗铁丝。接通直流电源,高锰酸钾在阳极析出沉于烧杯底部,溶液由墨绿色逐渐转为紫红色,电解1h后,停止通电,取出电极。在冷水中冷却电解液,使结晶完全,用玻璃砂布氏漏斗将晶体抽干,称重,计算产率。
回答下列问题:
(1)步骤①发生的反应方程式为______________________________
(2)步骤①中共熔时要选择__________坩埚(填“铁”、“陶瓷”或“石英”)。
(3)写出步骤③中发生的电极反应式:
阳极____________________________ 阴极________________________
(4)实验中用到抽滤操作,抽滤装置如下图所示,仪器B的名称是___________。抽滤完毕,吸滤瓶内的液体从_____________________倒出。步骤③抽滤时使用玻璃砂布氏漏斗的原因是_________________________________________________

查看答案和解析>>
科目: 来源:2011-2012学年浙江省高三第一学期期末考试化学试卷 题型:计算题
(6分)2011年6月,云南曲靖陆良化工实业有限公司5000多吨工业废料铬渣非法倾倒导致当地严重污染。+6价铬易被人体吸收,可致癌;+3价铬不易被人体吸收,毒性小。工业含铬废水的处理方法之一是将含+6价铬的废水放入电解槽内,用铁作阳极,加入适量的NaCl后进行电解:阳极区生成的Fe2+和Cr2O72-发生反应,生成的Fe3+和Cr3+在阴极区与OH-结合生成Fe(OH)3和Cr(OH)3沉淀除去。
(已知:常温下Ksp Fe(OH)3=2.6×10-39,Ksp Cr(OH)3=6.0×10-31)
(1)若阳极铁质量减少16.8g,则理论上被还原的Cr2O72-的物质的量为 mol。
(2)已知电解后的溶液中c(Fe3+)为2.6×10-13 mol·L-1,则溶液中Cr3+浓度为 mol·L-1。
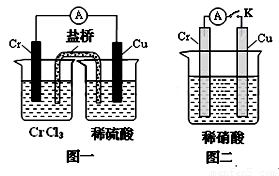
(3)在下图装置中,观察到图一装置铜电极上产生大量的无色气泡,而在图二装置中当开关K断开时,铬电极无现象,K闭合时,铬电极上产生大量无色气体,并变成红棕色气体。根据上述现象试推测金属铬的两个重要化学性质 、 。
查看答案和解析>>
科目: 来源:2011-2012学年浙江省富阳市高三上学期期中考试化学试卷 题型:选择题
绿色化学是从源头上防止污染产生或将化学过程对环境的负面影响降低到最低限度的化学。不仅化工生产应遵循绿色化学的原则,化学实验也应遵循绿色化学原则,实现原料和过程的绿色化。下列实验或实验过程遵循绿色化学原则的是
A.用过量的氯气进行性质实验 B.用双氧水代替高锰酸钾制氧气
C.用溴水代替碘水进行萃取实验 D.用铜粉代替铜丝进行Cu和浓HNO3的反应
查看答案和解析>>
科目: 来源:2011-2012学年浙江省富阳市高三上学期期中考试化学试卷 题型:选择题
下列实验过程中,始终无明显现象的是:
A.NO2通入FeSO4溶液中 B.CO2通入CaCl2溶液中
C.NH3通入AlCl3溶液中 D.SO2通入已酸化的Ba (NO3) 2溶液中
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com