
科目: 来源:2011-2012学年沈阳铁路实验中学高三上学期第三次月考化学试卷 题型:选择题
下列有关化学反应速率的说法中,正确的是 ( )
A.100 mL 2 mol/L的盐酸与锌反应时,加入适量的氯化钠溶液,生成氢气的速率不变
B.用铁片和稀硫酸反应制取氢气时,改用铁片和浓硫酸可以加快产生氢气的速率
C.二氧化硫的催化氧化是一个放热反应,所以升高温度,反应速率减慢
D.汽车尾气中的CO和NO可以缓慢反应生成N2和CO2,减小压强,反应速率减慢
查看答案和解析>>
科目: 来源:2011-2012学年沈阳铁路实验中学高三上学期第三次月考化学试卷 题型:选择题
在0.1mol/L的CH3COOH溶液中存在如下电离平衡:CH3COOH
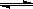 CH3COO-+H+ 对于该平衡,下列叙述正确的是( )
CH3COO-+H+ 对于该平衡,下列叙述正确的是( )
A.加入少量NaOH固体,平衡向逆反应方向移动
B.升高温度,平衡向正反应方向移动
C.加入水,CH3COOH的电离程度变大,溶液中c(H+)一定增大
D.加入少量CH3COONa固体,平衡向正反应方向移动
查看答案和解析>>
科目: 来源:2011-2012学年沈阳铁路实验中学高三上学期第三次月考化学试卷 题型:选择题
常温下,向等物质的量浓度的两种一元酸的盐溶液中,分别通入少量的CO2,发生如下
反应:NaA+CO2+H2O===HA+NaHCO3 2NaB+CO2+H2O===2HB+Na2CO3,则等物质的量浓度的HA和HB在水中电离出H+的能力大小关系是 ( )
A.HA较强 B.HB较强
C.两者一样 D.无法比较
查看答案和解析>>
科目: 来源:2011-2012学年沈阳铁路实验中学高三上学期第三次月考化学试卷 题型:选择题
MOH和ROH两种一元碱的溶液分别加水稀释时,pH变化如下图所示。下列叙述中正
确的是 ( )
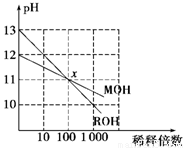
A.在x点时,ROH完全电离
B.在x点时,c(M+)>c(R+)
C.MOH是一种强碱
D.稀释前,c(ROH)=10c(MOH)
查看答案和解析>>
科目: 来源:2011-2012学年沈阳铁路实验中学高三上学期第三次月考化学试卷 题型:选择题
将pH=13的NaOH溶液平均分成两份,一份加适量水,另一份加入与该NaOH溶液物质的量浓度相同的适量硫酸后,pH都降低了1,则加入的水与硫酸的体积比为( )
A.10:1 B.11:1 C.20:1 D.21:1
查看答案和解析>>
科目: 来源:2011-2012学年沈阳铁路实验中学高三上学期第三次月考化学试卷 题型:填空题
在80℃时,0.40mol的N2O4气体充入 2L已经抽空的固定容积的密闭容器中,隔一段时间对该容器内的物质进行分析,得到如下数据:
|
时间(s) n(mol) |
0 |
20 |
40 |
60 |
80 |
100 |
|
n(N2O4) |
0.40 |
a |
0.20 |
c |
d |
e |
|
n(NO2) |
0.00 |
0.24 |
b |
0.52 |
0.60 |
0.60 |
(1)计算20s—40s内用N2O4表示的平均反应速率为 。
(2)计算在 80℃时该反应的平衡常数K 。
(3)能判断该反应是否已达化学平衡状态的依据是________________。
a.容器中压强不变
b.混合气体中c(N2O4)不变
c.v正(NO2)=v逆(N2O4)
d.混合气体密度不变
e.混合气体的平均摩尔质量不变
f.c(N2O4)= c(NO2)
(4)反应进行至100s后将反应混合物的温度降低,混合气体的颜色 (填“变浅”、“变深”或“不变”)。
(5)要增大该反应的K值,可采取的措施有(填序号) ,若要重新达到平衡时,使[NO2]/[N2O4]值变小,可采取的措施有(填序号) 。
A.增大N2O4的起始浓度 B.向混合气体中通入NO2
C.使用高效催化剂 D.升高温度
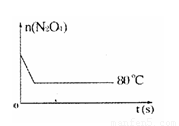
(6)如右图是 80℃时容器中N2O4物质的量的变化曲线,请在该图中补画出该反应在 60℃时N2O4物质的量的变化曲线。
查看答案和解析>>
科目: 来源:2011-2012学年沈阳铁路实验中学高三上学期第三次月考化学试卷 题型:实验题
为了证明一水合氨是弱电解质,甲、乙、丙、丁四位同学利用下面的
试剂进行实验:0.10 mol·L-1氨水、NH4Cl晶体、醋酸铵晶体、酚酞试剂、pH试纸、蒸
馏水。
(1)甲用pH试纸测出0.10 mol·L-1氨水的pH为10,据此他认定一水合氨是弱电解质,你认为这一结论________(填“正确”、“不正确”或“无法确定”),并说明理由____________________________________。
(2)乙取出10 mL 0.10 mol·L-1氨水,用pH试纸测出其pH为a,然后用蒸馏水稀释至
1 000 mL,再用pH试纸测出其pH为b,他认为只要a、b满足如下关系________(用等式或不等式表示)就可以确认一水合氨是弱电解质。
(3)丙取出10 mL 0.10 mol·L-1氨水,滴入2滴酚酞试液,显粉红色,再加入CH3COONH4晶体少量,颜色变浅;你认为这一方法能否证明一水合氨是弱电解质,________(填“能”或“否”)。
(4)丁同学的方案最可能是(答出实验操作方法、现象与结论)_____________________。
丁同学的方案的原理为(用离子方程式表示)_____________________。
查看答案和解析>>
科目: 来源:2011-2012学年沈阳铁路实验中学高三上学期第三次月考化学试卷 题型:填空题
合成氨工业的核心反应是:
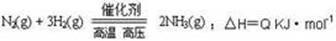
能量变化如右图,回答下列问题:
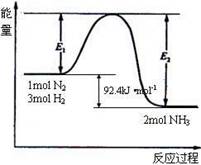
(1)在反应体系中加入催化剂,反应速率增大,E1和E2的变化是:E1 ,E2 (填“增大”、“减小”、“不变”)
(2)在500℃、2×107Pa和催化剂条件下向一密闭容器中充入0.5mol N2和1.5mol H2,充分反应后,放出的热量 (填“<”、“>”或“=”)46.2kJ;
(3)关于该反应的下列说法中,正确的是 。
A.△H>0,△S>0 B.△H>0,△S< 0 C.△H<0,△S>0 D.△H<0,△S<0(4)将一定量的N2(g)和H2(g)放入 1L密闭容器中,在500℃、2×107Pa下达到平衡,测得N2为0.10mol,H2为0.30mol,NH3为0.10mol。计算该条件下达到平衡时H2转化为NH3的转化率 。若升高温度,K值变化 (填“增大”、“减小”或“不变”)。
(5)在上述(4)反应条件的密闭容器中,欲提高合成氨中H2的转化率,下列措施可行的是 (填字母)。
A.向容器中按原比例再充入原料气 B.向容器中再充入惰性气体
C.改变反应的催化剂 D.分离出氨
查看答案和解析>>
科目: 来源:2011-2012学年河北省高三上学期第二次月考化学试卷 题型:选择题
下列变化中不属于氮的固定的是
A.豆科植物的根瘤菌把氮气变为NH3
B.闪电时,空气中的O2 和N2化合成NO
C.工业上将NH3与CO2在高温高压下制成[CO(NH2)2]
D.工业上用N2和H2合成NH3
查看答案和解析>>
科目: 来源:2011-2012学年河北省高三上学期第二次月考化学试卷 题型:选择题
下列关于浓硫酸和稀硫酸的叙述中,正确的是
A.加热时都能与铜发生反应
B.硫元素的化合价都是+6价
C.都能作为气体的干燥剂
D.常温时都能与铁发生反应,有大量气泡冒出
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com